微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W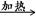 X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑
④X+Ca(OH)2―→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是:W:________、X:________、Y:________、Z:________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式),还原剂是________(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:①离子方程式:__________________________。②化学方程式:_______________________。
参考答案:(1)NaHCO3 Na2CO3 NaOH Na2O2
(2)②③ Na2O2 Na2O2?(3)Ca2++CO32-=CaCO3↓
Ca(OH)2+K2CO3=2KOH+CaCO3↓(其他合理答案也给分)
本题解析:W X+H2O+CO2↑,则W是碳酸氢钠,X是碳酸钠;Z+CO2―→X+O2,则Z是过氧化钠;Z+H2O―→Y+O2↑,则Y是氢氧化钠。
X+H2O+CO2↑,则W是碳酸氢钠,X是碳酸钠;Z+CO2―→X+O2,则Z是过氧化钠;Z+H2O―→Y+O2↑,则Y是氢氧化钠。
(1)W、X、Y、Z的化学式分别是NaHCO3、Na2CO3、NaOH、Na2O2。
(2)凡是有元素化合价升降的反应均是氧化还原反应,据此可知②Na2O2+CO2―→Na2CO3+O2、③Na2O2+H2O―→NaOH+O2↑氧元素的化合价发生变化,属于氧化还原反应,即答案选②③;其中均是过氧化钠中的氧元素发变化,即氧元素化合价部分从-1价升高到0价,部分降低到-2价,属于过氧化钠既是氧化剂,也是还原剂。
(3)碳酸钠和氢氧化钙反应的离子方程式为Ca2++CO32-=CaCO3↓;可溶性碳酸盐也能和氢氧化钙反应生成碳酸钙白色沉淀,例如Ca(OH)2+K2CO3=2KOH+CaCO3↓。
本题难度:简单
2、选择题 下列反应的离子方程式正确的是
A.亚硫酸钠溶液中加入硝酸:SO32-+2H+=H2O+SO2↑
B.铜片跟浓硝酸反应:Cu + 2NO3-+4H+=Cu2++2NO2↑+2H2O
C.0.1molFeBr2中通入0.1mol Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2 +6Cl-
20070309
D.硫化钠的水解:S2-+2H2O H2S+2OH-
H2S+2OH-
参考答案:B
本题解析:略
本题难度:简单
3、填空题 (6分)已知0.1 mol/L的NaHSO4溶液中H+的物质的量浓度为0.1mo1/L,请回答下列问题:
(1)写出NaHSO4在水溶液中电离的方程式?。
(2)若将NaHSO4与Ba (OH)2在溶液中按物质的量之比为2:1混合,化学反应的离子方程式是?。
参考答案:(6分)(1)NaHSO4=Na++H++SO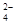 (2)2H++ SO
(2)2H++ SO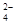 +Ba2++2OH—=2H2O+BaSO4↓
+Ba2++2OH—=2H2O+BaSO4↓
本题解析:
(1)硫酸氢钠在水溶液中完全电离出三种离子,即NaHSO4=Na++H++SO42-;
(2)NaHSO4与Ba (OH)2在溶液中按物质的量之比为2:1混合时,酸碱恰好中和,实质?是:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O。
本题难度:一般
4、选择题 下列离子方程式中,正确的是(? )?
A.向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO 反应完全
反应完全
2Ba2++ 4OH—+ Al3+ + 2SO
 +2H2O
+2H2O
B.向Mg(HCO3)2溶液中加入过量的NaOH溶液
Mg2++2HCO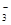 +4OH—
+4OH— +2H2O
+2H2O
C.足量的CO2通入饱和碳酸钠溶液中:CO2+CO +H2O
+H2O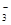
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++2NO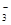
参考答案:B
本题解析:选项A不正确,当SO42-完全沉淀时,其余生成物是氢氧化铝和氨水;选项C不正确,因为碳酸氢钠的溶解度小于碳酸钠的,所以溶液中有晶体析出;选项D不正确,电子的得失不守恒,答案选B。
本题难度:一般
5、选择题 下列离子方程式正确的是
A.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
B.明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
C.Mg(HCO3)2溶液中加入过量石灰水:
Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
D.向100 mL 0.1 mol/L的FeBr2溶液中通入0.012 mol Cl2: