��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��ȷ����
A����С�մ���Һ�м��������Һ��HCO3����H��
B�����ᱽ����������Һˮԡ���ȵĻ�ѧ����ʽ��

C��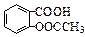 �������ռ�Һ��ˮ�⣺
�������ռ�Һ��ˮ�⣺
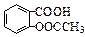 ��2OH��eq o(sup 9(����
��2OH��eq o(sup 9(���� ��CH3COO����2H2O
��CH3COO����2H2O
D����C6H5ONa��Һ��ͨ������CO2��2C6H5O����CO2��H2O 2C6H5OH��CO2��3
2C6H5OH��CO2��3
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��ȷ���ǣ�������
A������ˮ��Ӧ��2Na+2H2O�T2Na++2OH-+H2��
B�������������ᷴӦ��O2-+2H+�TH2O
C��CaCO3����Һ��ͨCO2��C032-+CO2+H2O�T2HCO3-
D��С�մ���Һ��NaOH��Һ��ϣ�HCO3-+OH-�TCO32-+H2O
�ο��𰸣�A������ˮ��Ӧ�����������ƺ����������ӷ�ӦΪ2Na+2H2O�T2Na++2OH-+H2������A��ȷ��
B�������ƺ����ᷴӦ�����Ȼ��ƺ�ˮ�����ӷ�ӦΪNa2O+2H+�TH2O+2Na+����B����
C��CaCO3����Һ��ͨCO2��Ӧ����̼����ƣ����ӷ�ӦΪCaC03+CO2+H2O�TCa2++2HCO3-����C����
D��С�մ���Һ��NaOH��Һ��Ӧ����̼���ƺ�ˮ�����ӷ�ӦΪHCO3-+OH-�TCO32-+H2O����D��ȷ��
��ѡAD��
���������
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ����ȷ����
A����FeCl3��Һ��ʴӡˢ��·�壺Fe3++Cu=Fe2++Cu2+
B��������������ʵ���Ũ�ȵ�NaHCO3��Һ��Ca(OH)2��Һ��ϣ�HCO3-+Ca2++OH��=CaCO3��+H2O
C����ϡ�����м���ͭ�ۣ�Cu + 2H+ = Cu2+ + H2��
D����AlCl3��Һ�м��������ˮ��Al3++3OH��=Al(OH)3 ��
�ο��𰸣�B
���������A������ʽ��ɲ��غ㣬����B����ȷ��C��������ʵ�����������D����ˮ��������ʣ�����
�����Ѷȣ�һ��
4��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ�ǣ�������
A����������Һ�м��������ˮ Al3++3OH��=Al��OH��3��
B��̼������Һ�м������ʯ��ˮ Ca��OH��2+CO32��=CaCO3��+2OH��
C���������������Һ��ͨ������ Cl2+2OH��=ClO��+Cl��+H2O
D��ϡ�����м������� 2Fe+6H+=2Fe3++3H2��
�ο��𰸣�C
���������A����Ӧ����������������������泥�
B������ʯ��ˮӦд��������ʽ��
C����Ӧ�����Ȼ��ơ��������ơ�ˮ��
D����Ӧ��������������������
�⣺A����������Һ�м��������ˮ�����ӷ�ӦΪAl3++3NH3��H2O=Al��OH��3��+3NH4+����A����
B��̼������Һ�м������ʯ��ˮ�����ӷ�ӦΪCa2++CO32��=CaCO3������B����
C���������������Һ��ͨ�����������ӷ�ӦΪCl2+2OH��=ClO��+Cl��+H2O����C��ȷ��
D��ϡ�����м������۵����ӷ�ӦΪFe+2H+=Fe2++H2������D����
��ѡC��
���������⿼�����ӷ�Ӧ����ʽ����д����ȷ�����Ļ�ѧ��Ӧ�����ӷ�Ӧ����ʽ����д�������� �����Ŀ�ѶȲ���
�����Ѷȣ�һ��
5�������
(1)����Cl2ͨ��FeI2(aq)�У���Ӧ�����ӷ���ʽ��?��
(2)����Cl2ͨ��FeI2(aq)�У���Ӧ�����ӷ���ʽ��?��
(3)��1.2 mol Cl2ͨ�뺬��FeI2 1.0 mol��ˮ��Һ�У�?��
�ο��𰸣�(1)2I����Cl2====2Cl����I2
(2)2Fe2����4I����3Cl2====6Cl����2Fe3����2I2
(3)2Fe2����10I����6Cl2====2Fe3����5I2��12Cl��
�����������ԭ��ǿ�ģ�����Ҫʧ���ӣ���(1)��ֻ��I��ʧ���ӣ���(2)��I����Fe2����ʧ���ӣ�����ȫ����������(3)��I��ȫ����������Fe2�����ֱ�������
n(����I����Cl2)= n(I��)="1.0" mol
n(I��)="1.0" mol
n(����Fe2����Cl2)=n��(Cl2)��n(����I����Cl2)="0.2" mol
n(��������Fe2��)="0.4" mol
n��(I��)��n��(Fe3��)��n��(Cl2)="2.0" mol��0.4 mol��1.2 mol=5��1��3��
�ݴˣ���д�����ӷ���ʽ��
�����Ѷȣ�һ��