| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《pH计算》高频试题巩固(2017年最新版)(二)
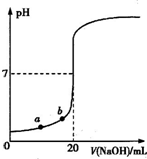 参考答案:A.a点时加入NaOH较少,溶液中c(H+)较大,c(H+)越大,水的电离程度越小,则有水电离出的氢离子浓度:a<b,故A错误; 本题解析: 本题难度:简单 2、选择题 常温下,将0.06mol/L的H2SO4溶液和0.10mol/L的NaOH等体积混合后,溶液的pH为( ? ) 参考答案:B 本题解析: 本题难度:一般 3、填空题 在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示。请回答下列问题 参考答案:(1)1×10-12 mol2・L-2;高于;曲线Ⅱ所代表的离子积比曲线Ⅰ的小,由于水的电离过程是吸热过程,温度越高,水的离子积越大,故曲线Ⅱ代表的温度低 本题解析: 本题难度:一般 4、选择题 将0.5L 0.1mol?L-1Fe2(SO4)3溶液与1L0.6mol?L-1氨水溶液完全混合并过滤,溶液总体积不变,则所得溶液的pH与下列选项符合的是( ) 参考答案:两溶液混合后,发生反应Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,0.5L 0.1mol?L-1Fe2(SO4)3溶液中n(Fe3+)=2×0.5L×0.1mol?L-1=0.1mol,1L0.6mol?L-1氨水中n(NH3)=1L×0.6mol?L-1=0.6mol,由方程式可知,0.1molFe3+完全反应,消耗0.3molNH3,剩余0.3molNH3,反应后溶液为氨水、硫酸铵的混合溶液,氨水的浓度为0.3mol1.5L=0.2mol/L,硫酸铵抑制氨水的电离,故混合溶液的pH值小于0.2mol?L-1氨水溶液的pH值, 本题解析: 本题难度:一般 5、简答题 试计算25℃时(Kw=1×10-14),50mL0.005mol/LH2SO4中: 参考答案:(1)c(H+)=2c(H2SO4)=2×0.005mol/L=0.01mol/L, 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点大全《铝》答题技.. | |