微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下图表示水中c(H+)和c(OH-)的关系,下列判断错误的是(?)
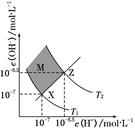
A.两条曲线间任意点均有c(H+)×c(OH-)=KW
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T1<T2
D.XZ线上任意点均有pH=7
参考答案:D
本题解析:本题重点考查水的离子积,意在考查考生对图像的分析能力以及对水的离子积的理解和应用能力。根据水的离子积定义可知A项正确;XZ线上任意点都存在c(H+)=c(OH-),所以M区域内任意点均有c(H+)<c(OH-),所以B项正确;因为图像显示T1时水的离子积小于T2时水的离子积,而水的电离程度随温度升高而增大,所以C项正确;XZ线上只有X点的pH=7,所以D项错误。
本题难度:简单
2、选择题 下列事实能说明氨水是弱电解质的是
[? ]
A.氨水与氯化铝溶液反应产生氢氧化铝沉淀
B.用氨水做导电实验,灯泡很暗
C.0.1mol/L的氨水的pH<13
D.氯化铵溶液的pH<7
参考答案:CD
本题解析:
本题难度:简单
3、选择题 将浓度为0.1 mol・L-1 HF溶液加水不断稀释,下列各量始终保持增大的是(? )
A.c(H+)
B.Ka(HF)
C.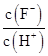
D.
参考答案:D
本题解析:A项,弱酸稀释时,电离平衡正向移动,溶液中n(H+)增大,但c(H+)减小,A错误;B项,弱酸的Ka只与温度有关,温度不变,Ka不变,B错误;C项,因为在同一溶液中,所以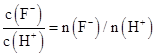 ,随溶液的稀释,弱酸对水的电离的抑制作用减弱,水电离出的H+逐渐增多,所以
,随溶液的稀释,弱酸对水的电离的抑制作用减弱,水电离出的H+逐渐增多,所以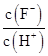 逐渐减小,C错误;D项,在同一溶液中,
逐渐减小,C错误;D项,在同一溶液中,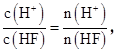 随溶液的稀释,HF的电离平衡正向移动,n(H+)增大,n(HF)减小,所以
随溶液的稀释,HF的电离平衡正向移动,n(H+)增大,n(HF)减小,所以 始终保持增大,D项正确。
始终保持增大,D项正确。
本题难度:一般
4、填空题 物质在水溶液中存在的电离平衡、水解平衡和沉淀溶解平衡,都可看作化学平衡。请根据所学知识回答:
(1)在0.1mo1・L-1的NaHSO3溶液中存在的各种平衡体系为(用离子方程式表示): 、 、 。
已知该溶液中有关微粒浓度由大到小的顺序为:c(Na+)>c(HSO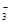 )>c(SO
)>c(SO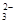 )>c(H2SO3)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由: .
)>c(H2SO3)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由: .
(2)常温下,某水溶液中存在的离子有:Na+、A―、H+、OH―,若该溶液由0.1mo1.L-1的HA溶液和0.1mol.L-1的NaOH溶液等体积混合而得,则溶液的pH (填“大于”、“小于”或“等于”)7,理由是 。
参考答案:(1) H2O H++OH- ; HSO3-
H++OH- ; HSO3- H++SO32-; HSO3-+H2O
H++SO32-; HSO3-+H2O H2SO3+OH- ; 大于; 在NaHSO3溶液中存在HSO3-的电离(HSO3-
H2SO3+OH- ; 大于; 在NaHSO3溶液中存在HSO3-的电离(HSO3- H++SO32-)和水解(HSO3-+H2O
H++SO32-)和水解(HSO3-+H2O H2SO3+OH-),由题给信息c(SO32-)>c(H2SO3)知电离比水解程度大,所以c(H+)>c(OH-) (回答出电离大于水解即可);
H2SO3+OH-),由题给信息c(SO32-)>c(H2SO3)知电离比水解程度大,所以c(H+)>c(OH-) (回答出电离大于水解即可);
(2)大于或等于;若HA是强酸,pH=7,若HA是弱酸,pH>7。
本题解析:(1)在0.1mo1・L-1的NaHSO3溶液中存在的各种平衡体系有电离平衡:H2O H++OH- ; HSO3-
H++OH- ; HSO3- H++SO32-和水解平衡:HSO3-+H2O
H++SO32-和水解平衡:HSO3-+H2O H2SO3+OH-。由于在该溶液中有关微粒浓度由大到小的顺序为:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3),说明HSO3-电离作用大于水解作用。因为在溶液中在NaHSO3溶液中存在HSO3-的电离(HSO3-
H2SO3+OH-。由于在该溶液中有关微粒浓度由大到小的顺序为:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3),说明HSO3-电离作用大于水解作用。因为在溶液中在NaHSO3溶液中存在HSO3-的电离(HSO3- H++SO32-)和水解(HSO3-+H2O
H++SO32-)和水解(HSO3-+H2O H2SO3+OH-),由题给信息c(SO32-)>c(H2SO3)知电离比水解程度大,所以c(H+)>c(OH-)。(2)若HA为强酸,则c(H+)=c(OH-).溶液显中性,pH=7;若HA为弱酸,则c(H+)<c(OH-).溶液显碱性,pH>7。
H2SO3+OH-),由题给信息c(SO32-)>c(H2SO3)知电离比水解程度大,所以c(H+)>c(OH-)。(2)若HA为强酸,则c(H+)=c(OH-).溶液显中性,pH=7;若HA为弱酸,则c(H+)<c(OH-).溶液显碱性,pH>7。
考点:考查多元弱酸的酸式盐溶液中的平衡及离子浓度的大小比较、溶液的酸碱性的知识。
本题难度:困难
5、选择题 已达电离平衡的0.1mol/L的醋酸溶液中,为提高醋酸的电离程度,同时使溶液的pH值降低,应采取的措施是
[? ]
A. 加一定量水
B. 加热
C. 加入盐酸
D. 加入冰醋酸
参考答案:B
本题解析:
本题难度:一般