��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������������Ӱ��ܶ෴Ӧ�����з�Ӧ�У��ܹ���Ӱ����������
A���Ҵ��������������Ӧ
B�������������ķ�Ӧ
C�����������ķ�Ӧ
D��������ķֽ�
�ο��𰸣�D
���������Aѡ�Ӧ���������ڼ��ȣ�Ũ�����������������½��С�Bѡ�����ڵ�ȼ������½��С�Cѡ�����ڵ�ȼ������¡�Dѡ�������ȶ��ڹ��յ������������ȷֽ⡣���Դ�ѡD
�����Ѷȣ���
2������� ��6�֣���ˮ�к��ж��ֳɷ֣�������ж�����ʣ�������ˮ�ֱ�����ͼ�������ʷ����ķ�Ӧ��գ�a��b��c��d�غϲ��ִ������ʼ䷴Ӧ������ˮ����������֤����ˮ����Ư���Ե���??(�a������b������c����d��)��C�����е������� ?��b�����е����ӷ���ʽΪ??��a�����еĻ�ѧ����ʽΪ ?��

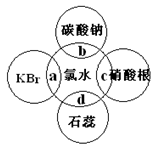
�ο��𰸣�d�� �а�ɫ�������� 2H����CO32����H2O��CO2��2Br����Cl 2��2Cl�� �� Br2
�����������ˮ�е�HClO��ǿ�����ԣ�һ����Ӧ����Ư��ʱ��HClO��ǿ�����Խ���ɫ������������ɫ���ʣ���������ˮ��ʹʯ����Һ�ȱ�죬����ɫ���ʴ�Ϊ��d����ˮ����Cl-������AgNO3��Һ�а�ɫ�������ɣ�����AgCl�������ʴ�Ϊ���а�ɫ�������ɣ���ˮ�к���HCl��HClO���������ԣ���CO32-��Ӧ���ɶ�����̼���壬��Ӧ�����ӷ���ʽΪCO32-+2H+=CO2��+H2O��Cl2��������ˮ����Ҫ�ɷ֣�����ǿ�����ԣ���KBr����������ԭ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ2KBr+Cl2 �T2KCl+Br2���ʴ�Ϊ��CO32-+2H+=CO2��+H2O�� 2KBr+Cl2 �T2KCl+Br2��
���������⿼�����������ʣ���Ŀ�ѶȲ���ע����ˮ�ijɷֺ����ʣ�ע�ػ���֪ʶ�Ļ��ۡ�
�����Ѷȣ�һ��
3�������� ��500mL 0.1 mol��L-1��FeCl2��Һ��ͨ��һ����Cl2������Ӧ��������Һϡ�͵�1 L����ȡ�� ϡ��Һ����������AgNO3��Һ���õ�2.009g������
ϡ��Һ����������AgNO3��Һ���õ�2.009g������
��1��ԭ��Һ�б�������Fe2+�����ʵ���Ϊ__________mol��
��2������ʣ���Fe2+ȫ���������������0.5 m ol��L-1��ϡ����_________ mL��
�ο��𰸣�(4 ��)��1��0.04? (2)26.7
�����������1�����ɵİ�ɫ�������Ȼ��������ʵ�����2.009g��143.5g/mol��0.014mol
����Һ�������ӵ����ʵ�����0.014mol��10��0.14mol
ԭ��Һ�е���������0.5L��0.1mol/L��2��0.1mol
���Բμӷ�Ӧ�������ǣ�0.14mol��0.1mol����2��0.02mol
����ݵ��ӵ�ʧ�غ��֪ԭ��Һ�б�������Fe2+�����ʵ���Ϊ0.02mol��2��0.04mol
��2��ʣ�������������0.5L��0.1mol/L��0.04mol��0.01mol
����ݷ�Ӧ�ķ���ʽ3Fe2����NO3����4H��=3Fe3����NO����2H2O��֪
��Ҫ��������ʵ�����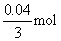
����Ҫ����������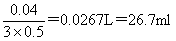
�����������Ǹ߿��еij������ͺͿ��㣬�����е��Ѷȵ����⡣�����ۺ���ǿ����ע�ض�ѧ������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ�������������������Ӧ������������Ĺؼ�����ȷ��Ӧԭ����Ȼ������ڸ����غ㷨������ʽ���㼴�ɡ�
�����Ѷȣ�һ��
4������� ijУ��ѧ�о���ѧϰС������������ʺ���;�����˵���������˽���������Ӧ�� ������Ư�ס�ˮ���ɱ����������ԭ����
(1) ��������ˮ������Ư�ס�������ԭ����_______����Ӧ�����ӷ���ʽΪ_______ ��
(2) ͨ��ʹ��Ư��Һ(NaClO��Һ)��Ư��������������������_____(д��һ���)��
(3) ��һ������ʯ������ͨ��һ����������������ǡ����ȫ��Ӧ (�����ķ�Ӧ��Ϊ���ȷ�Ӧ���������������к���Cl-�� ClO-��ClO3-���ֺ���Ԫ�ص����ӣ�����ClO-��ClO3-������ �ӵ����ʵ�����n)�뷴Ӧʱ�䣨t)�ı仯��������ͼ��ʾ��
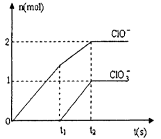
��O-t1ʱ���ڣ�Ca(OH)2��Cl2������Ӧ�Ļ�ѧ����ʽΪ_______��
��t2ʱ��Ca(OH)2��Cl2������Ӧ���ܵĻ�ѧ����ʽΪ_______
�۸�ʯ�����к���Ca(OH)2��������_______g��
�ο��𰸣���9�֣�
��1��������ˮ��Ӧ����ǿ�����ԵĴ����ᣨ1�֣���? Cl2+H2O=HClO+H++ClO-��1�֣� ��
��2��NaClO���ȶ������ڴ�������䣨1�֣���
��3����2Ca(OH)2��2Cl2��Ca(C1O)2��CaCl2��2H2O��2�֣���
��10Ca(OH)2��10Cl2��2Ca(C1O)2��Ca(C1O3)2��7CaCl2��10H2O��2�֣���
��370 g?��2�֣�
���������(1)������ˮ��Ӧ���ɴ����ᣬ��������к�ǿ�������ԣ�����������ˮ������Ư�ס�������ԭ����������ˮ��Ӧ����ǿ�����ԵĴ����ᣬ��Ӧ�����ӷ���ʽΪCl2+H2O=HClO+H++ClO-��
(2)�����ж����Ҳ�����ʹ�ã���ͨ��ʹ��Ư��Һ(NaClO��Һ)��Ư��������������������NaClO���ȶ������ڴ�������䡣
(3) ����ͼ�������t1ʱ��û��ClO3-�������ɣ���O-t1ʱ���ڣ�Ca(OH)2��Cl2������Ӧ�Ļ�ѧ����ʽΪ2Ca(OH)2��2Cl2��Ca(C1O)2��CaCl2��2H2O��
����ͼ�������t2ʱ��ClO-��ClO3-�������ɣ���t2ʱ��Ca(OH)2��Cl2������Ӧ���ܵĻ�ѧ����ʽΪ10Ca(OH)2��10Cl2��2Ca(C1O)2��Ca(C1O3)2��7CaCl2��10H2O��
���ɻ�ѧ���̼���ø�ʯ�����к���Ca(OH)2��������370 g��
���������⿼��������������ʵ����֪ʶ����Ŀ�Ѷ��еȣ�����ѧ���Ի���֪ʶ�����ճ̶Ⱥͼ���������
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��ʾ������ʢ����Һ�ٺ���Һ�ڵ��Թ��У�ͨ���������X�����բ١��ھ��г������ɵ���
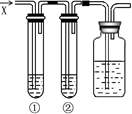
ѡ��
| X
| ����Һ
| ����Һ
|
A
| Cl2
| Na2SO3
| Na2S
|
B
| SO2
| Na2SiO3
| Ba(NO3)2
|
C
| NH3
| AgNO3
| AlCl3
|
D
| HCl
| CuSO4
| NaAlO2
|
?
�ο��𰸣�B
���������A�������ܰ�Na2SO3����ΪNa2SO4û�г�������Na2S����ΪS����������B��H2SO3����ǿ�ڹ��ᣬ���Ժ�Na2SiO3��Ӧ���ɹ��������H2SO3��Ba(NO3)2����������ԭ��Ӧ����BaSO4��������ȷ��C����AgNO3��Һ��ͨ������İ����õ�������Һ��ͨ��AlCl3��Ӧ����Al(OH)3����������D��HCl��CuSO4����Ӧ����NaAlO2��ͨ�������HCl����AlCl3������
�����Ѷȣ�һ��