微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 常温下某液态有机物A 10.6g和标况下30LO2完全反应,只生成CO2和液态水,将剩余的气体先通过浓硫酸浓硫酸增重9g,再将剩余的气体通过足量的碱石灰,气体减少17.92L(标况),已知该有机物蒸气相对于相同状况下氢气密度为53。
(1)求该有机物A的分子式(要有计算过程)
(2)又已知该有机物A的核磁共振氢谱中显示有两个峰,且面积之比为3:2。写出A的结构简式并命名
参考答案:(1)C8H10(2)该有机物是对二甲基苯,结构简式为 。
。
本题解析:考查有机物有机物分子式及结构简式的判断和计算。有机物分子式的确定,一般首先确定最简式,然后根据相对分子质量再确定分子式,最后根据性质确定结构简式。浓硫酸增重9g,说明生成物水的质量是9g。再将剩余的气体通过足量的碱石灰,气体减少17.92L,说明CO2的体积是17.92L。在相同条件下,气体的密度之比是相对分子质量之比,因此可以根据和氢气的相对密度来计算其相对分子质量。
(1)有机物蒸气相对于相同状况下氢气密度为53
所以该有机物的相对分子质量是53×2=106
因此10.6gA的物质的量为
剩余的气体先通过浓硫酸浓硫酸增重9g
所以燃烧产物水是9g,物质的量为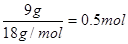
根据氢原子守恒可知有机物中氢原子的个数是10
再将剩余的气体通过足量的碱石灰,气体减少17.92L
S所以CO2的体积是17.92L,物质的量为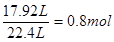
根据碳原子守恒可知有机物中碳原子的个数是8
因为12×8+10=106
所以该有机物不含氧原子
因此分子式为C8H10
(2)根据分子式及物理性质可知该有机物应该属于苯的同系物。又因为A的核磁共振氢谱中显示有两个峰,且面积之比为3:2,所以该有机物是对二甲基苯,结构简式为 。
。
本题难度:一般
2、实验题 化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。图中所列装置是用燃烧法确定有机物分子式常用的装置。(每一组仪器只能使用一次)


回答下列问题:
(1)产生的氧气按从左到右流向,所选择的装置各导管的连接顺序是_____ 。
(2)C装置中浓硫酸的作用是_____ 。
(3)D装置中MnO2的作用是_____ 。
(4)若准确称取7.2 g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加22 g,B管质量增加10.8 g,则该有机物的最简式为_____ 。
(5)要确定该有机物的分子式,则_____ (填“是”或“不”)需要测定其他数据,若能确定其分子式,若其一氯代物只有一种,则其结构简式为_____ 。
参考答案:(1)g→f,e→h,i→c,d→a(2)吸收水分,得到干燥纯净的O2(3)作催化剂,加快产生O2的速率(4)C5H12 (5)不 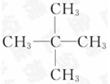
本题解析:据实验目的和各装置的作用推知整套装置为D→C→E→B→A,各导管接口顺序为g→f,e→h,i→c,d→a。其中D为O2发生装置(MnO2作催化剂),C中浓H2SO4作用是吸收水分,得到干燥纯净的O2,E为有机物燃烧装置,B中CaCl2吸收反应生成的H2O,A中NaOH吸收反应生成的CO2。m(CO2)="22" g,n(CO2)="0.5" mol,m(H2O)="10.8" g,则n(H2O)="0.6" mol,则m(C)+m(H)="12×0.5+0.6×2×1=7.2" g,所以该有机物的最简式为C∶H=0.5∶(0.6×2)=5∶12,即C5H12,因最简式中氢原子数已达饱和,故C5H12就是其分子式,若其一氯代物只有一种,则其结构简式为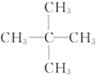 。
。
本题难度:一般
3、选择题 下列说法正确的(?)
A.提纯粗苯甲酸的实验中,加热溶解后,除去不溶性杂质时应充分冷却后过滤
B.分子式为C4H8O2的有机物能在酸性条件下水解成两种产物,其中一种产物能被氧化成另一种产物,则符合条件的有机物有3种
C.沸点比较:1,2,3-丙三醇 > 乙二醇 > 丙烷>乙醇 >乙烷
D.在碱性条件下,将0.1mol的CH3COO18C2H5完全水解,所得乙醇分子中氧原子内含中子的物质的量为1mol
参考答案:D
本题解析:A、苯甲酸趁热过滤除去杂质,冷却后苯甲酸成晶体析出,错误;B、C4H8O2的有机物能在酸性条件下水解成两种产物,其中一种产物能被氧化成另一种产物,说明碳原子数相同则只能为乙酸乙酯,错误;C、含有羟基的有机物,分子之间有氢键,因此含羟基个数越多,沸点越高,含碳原子数越多,沸点越高,因此1,2,3-丙三醇>乙二醇>乙醇>丙烷>乙烷,错误;D、发生酯化反应原理,酸脱羟基醇脱氢,水解时,CH3COO18C2H5完全水解生成乙酸和HO18C2H5,氧原子质量数为18,则含10个中子,正确。
本题难度:简单
4、选择题 下列实验现象预测正确的是()
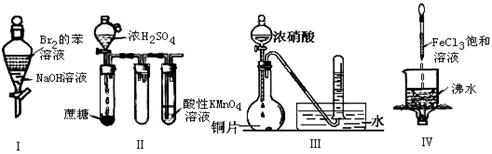
A.实验I:振荡后静置,下层溶液颜色变浅,上层溶液颜色保持不变
B.实验II:酸性KMnO4溶液中出现气泡,但颜色保持不变
C.实验III:向烧瓶中滴加浓硝酸,试管中收集到的气体与烧瓶中的气体颜色相同
D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
参考答案:D
本题解析:溴单质能溶解在氢氧化钠溶液中,颜色都是无色的,A不正确。浓硫酸在炭化蔗糖的过程中会产生SO2气体,高锰酸钾溶液能氧化SO2,B不正确。浓硝酸的还原产物是NO2,是红棕色。但NO2溶于水会生成无色的NO,C不正确。D中属于氢氧化铁胶体的丁达尔效应,正确,所以答案选D。
本题难度:一般
5、实验题 某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题:
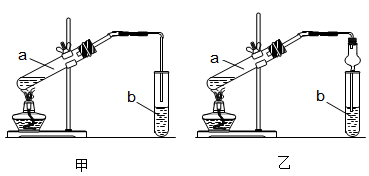
(1)试管a中反应的化学方程式: ?。
(2)试管b中盛放的试剂是?。
(3)实验时混合乙醇和浓硫酸的方法是?
(4)甲装置试管b中导管未伸入液面下的原因是?;乙装置中球形干燥管的作用是 ①??②??③?。
(5)试管b中溶液的主要用途是:?
参考答案:(1)CH3CH2OH + CH3COOH CH3COO CH2CH3+H2O? (2分)
CH3COO CH2CH3+H2O? (2分)
(2)饱和碳酸钠溶液(1分)
(3)先加入一定量的乙醇,然后边振荡边缓慢的加入浓硫酸并不断振荡 (每空1分,共2分)
(4)①防止出现倒吸②使冷凝效果更好③导气(各1分,3分)
(5)除去乙酸乙酯中含有的少量乙酸和乙醇,有利于闻到乙酸乙酯的香味。降低乙酸乙酯的溶解度,便于分层析出。(1分)
本题解析:(1)a是制取乙酸乙酯的,方程式为CH3CH2OH + CH3COOH CH3COO CH2CH3+H2O。
CH3COO CH2CH3+H2O。
(2)由于生成的乙酸乙酯中含有乙酸和乙醇,所以要除杂,可选择饱和碳酸钠溶液。
(3)由于浓硫酸稀释会放出大量的热,且其密度大于水的,所以先加入一定量的乙醇,然后边振荡边缓慢的加入浓硫酸并不断振荡。
(4)乙醇和乙酸都是和水互溶的,所以为防止出现倒吸,不能插入溶液中。乙装置中球形干燥管。除了可以防止倒吸以外,还可以使冷凝效果更好,同时兼起导气作用。
(5)碳酸钠的主要作用是除去乙酸乙酯中含有的少量乙酸和乙醇,有利于闻到乙酸乙酯的香味。降低乙酸乙酯的溶解度,便于分层析出。
本题难度:一般