微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素。少量A与水反应完全水解但不发生氧化或还原反应,所有反应产物均可溶于水。将A配成水溶液稀释后分成几份,分别加入一系列0.1mol/L的试剂,现象如下:
①加入硝酸酸化的硝酸银,产生白色沉淀;
②加入氯化钡溶液,无沉淀产生;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀。
⑴由①判断组成该化合物的元素中,肯定存在的卤素有?,由②判断A与水反应后生成的溶液中肯定不存在的离子有? 。由③判断A与水反应后生成的溶液中肯定存在的离子有? .
。由③判断A与水反应后生成的溶液中肯定存在的离子有? .
⑵要确定该化合物的分子式,称取11.90gA溶于水稀释至250.00mL,取25.00mL溶液加入足量的高锰酸钾和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重为2.33g。试确定A的化学式,写出计算推理过程。
2、简答题 (1)为了除去下列物质中的少量杂质(括号内位杂质).请在空白处填入适当的试剂:
| 物质 | 试剂 | 物质 | 试剂
CuO(Al2O3)
______
Si02(CaO)
______
NaHCO3溶液(Na2CO3)
______
Fe(Al)
______
|
(2)在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中.此反应若转移了0.3mol的电子,则生成氯气______L(标准状况下)
3、实验题 (16分)某白色粉末其成分可能是碳酸钠和亚硫酸钠的一种或两种组成。请完成对该白色粉末成分的探究:
限选实验仪器:药匙、试管、单孔塞、导管、玻璃棒、滴管、带铁夹的铁架台。
限选实验试剂:1 mol・L-1H2SO4、3%H2O2、澄清石灰水、品红试液。
(1)提出合理假设
假设1:该白色粉末成分为亚硫酸钠;
假设2:该白色粉末成分为碳酸钠;
假设3: ? 。
(2)设计实验方案证明(1)的假设
(3)实验过程
根据(2)的实验方案,进行实验。写出实验操作步骤、预期现象与结论。
实验操作
| 预期现象与结论
|
步骤1:检查装置气密性(略)
| ?
|
步骤2:
| ?
|
步骤3:
| ?
4、选择题 下列各组混合物中能够使用分液漏斗分离的是( )
A.苯和水
B.乙醇和乙酸
C.乙酸和乙酸乙酯
D.汽油和柴油
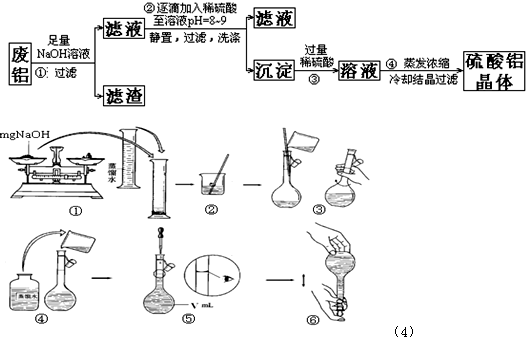
5、简答题 某化学兴趣小组以含铁的废铝为原料制备硫酸铝晶体,设计如下的实验方案:请回答以下问题:
(1)上述实验中多次用到过滤操作,该操作中要用到的玻璃仪器有______;
(2)步骤②中有洗涤沉淀的操作,如何判断沉淀已洗涤干净:______;
(3)评价步骤②的操作中难以控制之处______,请你提出一个合理而比较容易操作的实验方案(药品可任选)______,该反应的分子方程式为:______;
(4)步骤①中使用的NaOH溶液以4mol/L为宜.某同学称量mgNaOH固体配制V?m?L?4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号)______.
|