解释(用离子方程式表示)
滴加KSCN溶液后,溶液
______(填“变”或“不变”)红色
______(填“能”或“不能”)确定反应后的固体混合物中含有+3价的Fe
①______
②______
参考答案:(1)根据装置图中仪器形状和用途判断仪器名称为球形干燥管,烧瓶中加入碎瓷片防止加热暴沸,
故答案为:球形干燥管,碎瓷片;
(2)①高温铁和水蒸气反应,所以装置A处加热产生水蒸气,再点燃B装置处的酒精灯,甲中导气管位置错误,排水量气不能排除水,不可以测量生成氢气的体积,乙丙丁都可以利用装置测定生成气体的体积,
故答案为:A,B,甲;
②称取1.0g铁粉与适量石棉绒混合,然后加热反应一段时间.若测出的气体体积在标准状况下为44.8mL,生成的气体是氢气,物质的量为0.002mol,依据反应的化学方程式得到反应铁的质量:
3Fe+4H2O高温.Fe3O4+4H2,则铁粉的转化率为
3×56g 4mol
m 0.002mol
m=0.084g,铁粉的转化率=0.084g1.0g×100%=8.4%,
故答案为:8.4%;
(3)为了证明反应后的固体混合物中含有+3价的Fe,取出少量混合物于试管中,加入足量的盐酸,溶解,过滤.向滤液中滴加KSCN溶液,观察溶液的颜色变化分析铁离子的存在,铁离子遇硫氰酸钾溶液会变血红色;铁剩余会在溶液中和铁离子反应生成亚铁离子,依据溶液颜色分析离子存在,血红色说明一定含三价铁离子,不变血红色,不能证明一定不含有铁离子;
现象结论解释(用离子方程式表示)不变不能①Fe3O4+8H+=Fe2++2Fe3++4H2O
②Fe+2Fe3+=3Fe2+故答案为:现象结论解释(用离子方程式表示)不变不能①Fe3O4+8H+=Fe2++2Fe3++4H2O
②Fe+2Fe3+=3Fe2+
本题解析:
本题难度:一般
3、实验题 为了确定CH3COOH、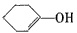 及H2CO3 的酸性强弱,有人设计了如下图所示的装置进行实验:? 及H2CO3 的酸性强弱,有人设计了如下图所示的装置进行实验:?
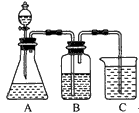
(1)若锥形瓶中装有一易溶于水的正盐固体,则A中发生反应的离子方程式为 ___________。
(2)装置B中盛放的试剂是_________,它的作用是____________ 。
(3)实验中观察到C中出现的主要现象是_____________。
参考答案:(1)2CH3COOH+CO32-→2CH3COO-+CO2↑+H2O
(2)饱和NaHCO3溶液 ;除去CO2中混有的CH3COOH
(3)C中溶液变浑浊
本题解析:
本题难度:一般
4、实验题 ?以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中央持和加热装置略去),分别研究SO2和Cl2的性质
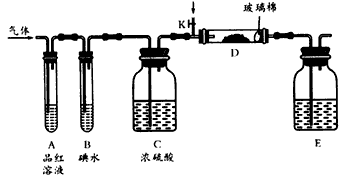
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?_______(填“相同”或“不相同”);若装置D中装的是V2O3(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为___________________________。
②SO2通入B中,溶液颜色褪去,则该反应的离子方程式为_______________________。
③E中的试剂为__________(填化学式)。
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)_____________,仍然无法观察到沉淀产生。
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;若Cl2与含X的溶液完全反应后,得澄清 溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式_______________________
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如下图,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为____极,其电极反应式为
_________________;电池的总反应式_______________

(5)实验是化学研究的基础,关于下列各装置图的叙述正确的是__________。(填序号)
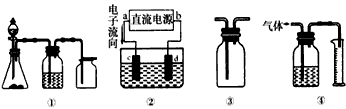
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正极,d为阳极
C.装置③可用于收集H2、NH3、Cl2、HCl、NO2等
D.装置④能用于测量气体体积
(6)用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中正确的是__________。(填序号)
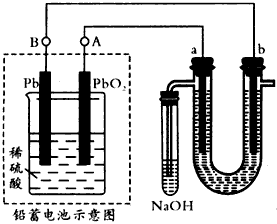
A.铅蓄电池负极的反应式为:Pb -2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
参考答案:(1)①相同;2SO2+O2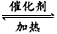 2SO3;②SO2+I2+2H2O=4H++2I-+SO42-;③NaOH(其他合理答案也可) 2SO3;②SO2+I2+2H2O=4H++2I-+SO42-;③NaOH(其他合理答案也可)
(2)B
(3)4Cl2+S2O32-+5H2O =2SO42-+8Cl-+10H+
(4)负;SO2-2e-+2H2O=4H++SO42-;2SO2+O2+2H2O=2H2SO4
(5)C
(6)D
本题解析:
本题难度:困难
5、实验题 碳酸氢铵是一种重要的铵盐。实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱。完成下列填空:
(1)二氧化碳通入氨水的过程中,先有________晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体。
(2)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠。实验步骤依次为:①粗盐溶解;②加入试剂至沉淀完全,煮沸;③_______;④加入盐酸调pH;⑤加入__________;⑥过滤;⑦灼烧,冷却,称重。
(3)上述步骤②中所加入的试剂为_____________、____________。
(4)上述步骤④中加盐酸调pH的目的是________________________。
参考答案:(6分)每空1分(1)(NH4)2CO3? (2)过滤;NH4HCO3 ?(3)Na2CO3; NaOH? (4)除去过量的Na2CO3
本题解析:(1)二氧化碳通入氨水的过程中,由于开始氨水是过量的,则先有(NH4)2CO3析出。
(2)Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,将生成的碳酸钙和氢氧化镁沉淀过滤后除去,然后加入盐酸酸化,以及除去过量的碳酸钠。最后在滤液中加入碳酸氢铵,生成碳酸氢钠和氯化铵。将过滤后得到的碳酸氢钠加热分解即生成碳酸钠。
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
本题难度:一般
|