��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���й���������ԭ��Ӧ�е��й�˵����ȷ���ǣ�������
A����������������������
B��Ԫ���ɻ���̬��Ϊ����̬ʱ����Ԫ��һ������ԭ
C����Щ���ֽⷴӦ����������ԭ��Ӧ
D������������������ԭ��Ӧ��һ������ԭ��
�ο��𰸣�A��������ԭ��Ӧ�л�ԭ��������������������Ӧ���������������ǻ�ԭ������A����
B��Ԫ�ػ��ϼۿ������ߵõ�����̬���ʣ���ǽ������ʵ����ɣ�ʵ������������Ҳ���Խ��͵õ�����̬���ʣ�����������Ʊ�����������ͭ��Ӧ����ͭ���ʣ���B����
C�����ֽⷴӦ�����ֻ����ﷴӦͨ�������ɷ������������ֻ�����ķ�Ӧ����������Ԫ�ػ��ϼ۱仯�����ֽⷴӦһ��������������ԭ��Ӧ����C����
D������Ԫ�����ۣ��������ʷ���������ԭ��Ӧʱ��Ԫ�ػ��ϼ�һ����������ԭ��������������������ԭ��Ӧ��һ������ԭ������D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
2��ѡ���� ��֪?6FeSO4+2KNO3+4H2SO4�TK2SO4+3Fe2��SO4��3+2NO��+4H2O�������ж���ȷ���ǣ�������
A��������Ӧ��KNO3�ǻ�ԭ��
B����Ӧ��H2SO4��������
C��������Ӧ��Fe2+���������������������˻�ԭ��
D��������0.1mol NOʱ����������Ӧת�Ƶ��ӵ����ʵ���Ϊ0.3mol
�ο��𰸣�A����KNO3��NԪ�صĻ��ϼ۽��ͣ���KNO3Ϊ����������A����
B����H2SO4�и�Ԫ�صĻ��ϼ��ڷ�Ӧǰ���䣬��������������B����
C����Ӧ��ֻ��FeԪ�صĻ��ϼ����ߣ���������Ӧ��Fe2+ֻ�����˻�ԭ�ԣ���C����
D������0.1molNOʱ����������Ӧת�Ƶ��ӵ����ʵ���Ϊ0.1mol����5-2��=0.3mol����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
3��ѡ���� ���;�ˮ��-������أ�K2FeO4��Ϊ����ɫ���壬������ˮ����ҵ���Ʊ�K2FeO4�ij��÷���֮һ�Ǵ�����������������2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O
��Na2FeO4+2KOH�TK2FeO4+2NaOH������˵������ȷ���ǣ�������
A����Ӧ��Ϊ������ԭ��Ӧ����Ӧ��Ϊ���ֽⷴӦ
B����Ӧ�������������뻹ԭ�������ʵ���֮��Ϊ2��9
C����Ӧ�ڵIJ���K2FeO4��FeΪ+6�ۣ�����ǿ�����ԣ���ɱ������
D������2molFeCl3������Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ6mol
�ο��𰸣�A����Ӧ��Fe��ClԪ�ػ��ϼ۷����仯��Ϊ������ԭ��Ӧ����Ӧ��Ԫ�ػ��ϼ�û�з����仯��Ϊ���ֽⷴӦ����A��ȷ��
B����Ӧ2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O�У�NaClOΪ��������FeCl3Ϊ��ԭ�����ɷ���ʽ��֪�����������뻹ԭ�������ʵ���֮��Ϊ2��3����B����
C���ɻ��ϼ۴�����Ϊ0��ԭ���֪K2FeO4��FeΪ+6�ۣ�����ǿ�����ԣ���ɱ����������C��ȷ��
D����Ӧ2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O�У�FeԪ�ػ��ϼ����ߣ���+3�����ߵ�+6�ۣ�������2mol FeCl3������Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ6 mol����D��ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
4������� �������Ũ������һ���¶��·�Ӧ�������̻�ɫ���ױ���������ȣ���Ӧ�Ļ�ѧ����ʽΪ��
2KClO3+4HCl��Ũ���T2KCl+2ClO2��+Cl2��+2H2O
��1����˫���ű�ʾ������Ӧ�е���ת�Ƶķ������Ŀ______��
��2��Ũ�����ڸ÷�Ӧ�б��ֵ�������______������ţ���
��ֻ�л�ԭ��?�ڻ�ԭ�Ժ�����?��ֻ��������?�������Ժ�����
��3��������Ӧ����0.2?mol?Cl2ʱ��ת�Ƶĵ�����ԼΪ______��
�ο��𰸣���1��KClO3��ClԪ����+5�۽���Ϊ+4�ۣ�HCl��ClԪ����-1������Ϊ0����Ӧ��ת��2e-����˫���ű�ʾ��Ӧ�е���ת�Ƶķ������Ŀ
Ϊ
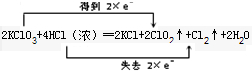
���ʴ�Ϊ��

��
��2���ɷ�Ӧ��֪��HCl�в���ClԪ�صĻ��ϼ����ߣ����ֻ�ԭ�ԣ����ֻ��ϼ۲��������α������ԣ��ʴ�Ϊ���ڣ�
��3���ɷ�Ӧ��֪������1molCl2ʱ��ת��2mol���ӣ������0.2?molCl2ʱ��ת�Ƶĵ�����ԼΪ0.4��6.02��1023=2.408��1023���ʴ�Ϊ��2.408��1023��
���������
�����Ѷȣ�һ��
5��ѡ���� �칬һ�Ŵ��صij������Ż��ʹ�õ���Ҫȼ����ƫ�����£���R��ʾ�����������������ڻ������ʱ�����߾��ҷ�Ӧ�����������岢�ͷų��������ȣ��÷�Ӧ�Ļ�ѧ����ʽΪ��R+2N2O4=3N2+4H2O+2CO2����������������ǣ�������
A���˷�Ӧ����˲����������������壬�ƶ��������
B���˷�Ӧ��������ԭ��Ӧ��N2O4����ԭ��
C���˷�Ӧ��������ԭ��Ӧ��ƫ����������ԭ��
D���˷�Ӧ��R�ķ���ʽΪC2H8N2
�ο��𰸣�B
���������
�����Ѷȣ���