微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)实验室常用的浓盐酸密度为1.17 g・mL-1,质量分数为36.5%。
(1) 此浓盐酸的物质的量浓度为_________。
(2) 取此浓盐酸50 mL,用蒸馏水稀释到200 mL,稀释后盐酸的物质的量浓度为_________。
(3) 将13 g锌投入足量的上述实验所得的稀盐酸中,充分反应后,
① 放出的H2在标准状况下的体积为_______。
② 将生成的H2通过足量的灼热CuO,则被还原出的铜的质量为______ (假设氢气在反应中没有损失)。
参考答案:(1)11.7 mol・L-1 ?
(2)2.93mol/L或2.925 mol/L
(3)①4.48 L ?②12.8 g
本题解析:略
本题难度:简单
2、选择题 配制一定体积、一定物质的量浓度的溶液,下列操作会使配得的溶液浓度偏小的是(?)
A.容量瓶中原有少量蒸馏水
B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯
C.滴管加水时,有少量水滴到容量瓶外
D.加水未达到刻度线
参考答案:B
本题解析:A.容量瓶中原有少量蒸馏水对溶质物质的量和溶液体积均无影响,所以不影响溶液的浓度,不符题意;
B.没有洗涤烧杯会使溶质的物质的量偏小,导致配得的溶液物质的量浓度偏小,符合题意;
C.滴管加水时,有少量水滴到容量瓶外,对溶质物质的量和溶液体积均无影响,对溶液物质的量浓度无影响,不符题意;
D.加水未达到刻度线,会使配得的溶液体积偏小,导致溶液物质的量浓度偏大,不符题意。
点评:本题考查了一定物质的量浓度溶液的配制的误差分析时,注意从c=n/V分析操作对溶质的物质的量或对溶液的体积的影响判断。
本题难度:一般
3、计算题 将25 g硫酸铜晶体溶解于水中,配成1 L溶液,此溶液的物质的量浓度是多少?取其溶液100 mL,向其中加入100 mL 0.2? mol・L-1的NaOH溶液,反应后溶液的物质的量浓度又是多少?(设混合后溶液体积不变)
参考答案:c(CuSO4)="0.1" mol・L-1;c(Na2SO4)="0.05" mol・L-1。
本题解析:CuSO4溶液的物质的量浓度是:
c(CuSO4)=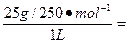 0.1 mol・L-1。
0.1 mol・L-1。
取100 mL 0.1 mol・L-1CuSO4溶液,其中含CuSO4的物质的量:
n(CuSO4)="0.1" mol・L-1×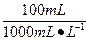 ="0.01" mol
="0.01" mol
100 mL 0.2 mol・L-1NaOH溶液中含NaOH的物质的量:
n(NaOH)="0.2" mol・L-1×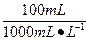 ="0.02" mol
="0.02" mol
CuSO4? +? 2NaOH====Na2SO4 +Cu(OH)2↓
1 mol? 2 mol? 1 mol
0.01 mol? 0.02 mol
由方程可知CuSO4与NaOH 恰好反应,生成0.01 mol Na2SO4。
Na2SO4溶液的物质的量浓度:
c(Na2SO4)=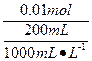 ="0.05" mol・L-1。
="0.05" mol・L-1。
本题难度:简单
4、选择题 NA为阿伏伽德罗常数,下列叙述错误的是
A.18gH2O中含的质子数为10NA
B.标准状况下,22.4L空气含有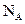
 个单质分子
个单质分子
C .46gNO2和N2O4混合气体中含有原子总数为3NA
.46gNO2和N2O4混合气体中含有原子总数为3NA
D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
参考答案:B
本题解析:略
本题难度:一般
5、选择题 下列叙述正确的是?(?)
A.1 mol  H2SO4的质量为98 g・mol-1
H2SO4的质量为98 g・mol-1
B.H2SO4的摩尔质量为98 g
C.98 g H2SO4含有NA个H2SO4分子
D.6.02×1023个H2SO4分子的质量为9.8 g
参考答案:C
本题解析:略
本题难度:简单