微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 体积为1L的干燥容器中充入氨气,测得容器中气体对氢气的相对密度为9.7。用此气体进行喷泉实验,当喷泉停止后,进入容器中液体的体积约是(? )
A.0.2L
B.0.25L
C.0.75L
D.0.8L
参考答案:D
本题解析: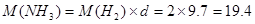 ,则根据“十字交叉”法可得它们的物质的量关系为:
,则根据“十字交叉”法可得它们的物质的量关系为:

即可知,在1L容器中,进入容器中液体的体积约是0.8L;
本题难度:一般
2、填空题 某化肥厂以氨和空气(其中氧气的体积分数为0.2)为原料生产硝酸铵过程如下:
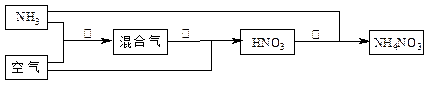
其中反应①为4NH3+5O2 4NO+6H2O
4NO+6H2O
⑴步骤②中发生了两个反应,将这两个化学方程式合并为一个化学方程式,可表示为_____________
________________________。
⑵若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为____________。
⑶假设实际生产中,反应①、②中含氮物质的利用率分别为a、b,反应③中氨的利用率为c、硝酸的利用率为100%,则合成硝酸铵的整个流程中,氨的总利用率是多少?
参考答案:(1)4NO+3O2+2H2O=4HNO3?
(2)1/6(或16.7%)
本题解析:本题考查了在工业流程背景下的化学计算,关键是能够准确的找出各生产原料和产物间的关系,然后根据所找到的比例关系进行相应计算.找关系式的一种方法就是将方程式当作代数式进行相应的消元,得出我们需要的相关物质的关系。
⑴反应②涉及这样几步反应:? 2NO+O2 = 2NO2?I
3NO2+H2O = 2HNO3+NO?II
I×3+II×2,消去中间物NO2,得 :4NO+3O2 +2H2O = 4HNO3
⑵整个过程包括这样几步反应:
4NH3+5O2 4NO+6H2O?①
4NO+6H2O?①
4NO+3O2 +2H2O = 4HNO3 ?②
NH3+HNO3 = NH4NO3 ?③
①+ ②+③×4,约简得: 2NH3++2O2 = NH4NO3 ?+ H2O
由n(NH3):n(O2)=1:1 推知V(NH3):V(空气)=1:5?
(3)
解法一:假设消耗NH3的总物质的量为1mol,其中用于制取HNO3的NH3的物质的量为x mol,被HNO3吸收的NH3的物质的量为ymol,则有:x+y=1、abx=cy。
解得:x= ?y=
?y=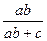
氨的总利用率=(xab+yc)/1= ?
?
解法二:假设第①步参加反应的氨气的物质的量为4mol,则:生成硝酸的物质的量4abmol;
第③步需要氨气的物质的量为 mol;?氨的总利用率=
mol;?氨的总利用率= =
=
本题难度:一般
3、选择题 将盛有24mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余4mL无色气体,则原混合气体中O2的体积是
A.2.4mL
B.2.8mL
C.8.6mL
D.8.0mL
参考答案:AD
本题解析:考查过量不足的典型题目。
4NO2+O2+2H2O===4HNO3? 3 NO2 +H2O===2HNO3 +NO
当剩余气体为氧气时,则原气体中氧气为4+(24-4)×1/5=8mL
当剩余气体为NO时,则原气体中O2为:(24-3×4)×1/5=2.4mL
本题难度:简单
4、实验题 (10分)工业合成氨气的 成功,解决了人类的重要的饥饿问题.我们在实验室中也常用NH4Cl和Ca(OH)2反应来制取一些氨气以便研究它的性质.请回答下列问题:
成功,解决了人类的重要的饥饿问题.我们在实验室中也常用NH4Cl和Ca(OH)2反应来制取一些氨气以便研究它的性质.请回答下列问题:
(1) 下图装置中能用于实验室制NH3的是____________ .
.
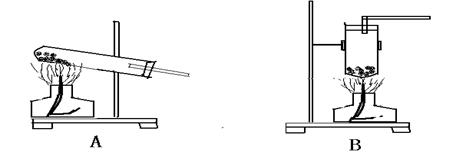
(2) 写出用 NH4Cl和Ca(OH)2制取氨气的反应方
NH4Cl和Ca(OH)2制取氨气的反应方 程式:_______________.
程式:_______________.
(3) 将湿润的红色石蕊试纸伸入充满氨 气的试剂瓶中可以看到的现象是___________________.
气的试剂瓶中可以看到的现象是___________________.
(4) NH3在工业上除作为制作化肥的原料外,也常用来制取硝酸,其主要步骤为: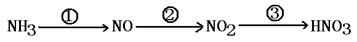
请 写出下列反应的化学方程式:
写出下列反应的化学方程式:
NH3→ NO : _________________________________________.
Cu和浓硝酸反应:_ __________________________________________.
__________________________________________.
参考答案:(10分)
(1)A?(2) 2NH4Cl + Ca(OH)2 =" CaCl2" + 2NH3 + 2H2O
(3) 变蓝?(4) 4NH3 + 5O2? =" 4NO" + 6H2O
Cu + 4HNO3(浓) =" Cu(NO3)2" + 2NO2 + 2H2O
本题解析:略
本题难度:一般
5、选择题 下列关于硒的叙述中,不正确的是(?)

A.硒在空气中燃烧生成SeO2,和钠反应生成Na2Se

B.硒化氢有恶臭味,有毒,比硫化氢易分解

C.硒化氢在空气中不能燃烧

D.亚硒酸(H2SeO3)是一种弱酸
参考答案:C
本题解析: 硒和硫同属氧族元素,但硒的核电荷数,原子半径都比硫大,这两种元素除化学性质相似外,硒的非金属性比硫弱,据此可作硫在空气中燃烧生成二氧化硫;与钠能组成化合物Na2S;硫化氢有臭鸡蛋气味,有剧毒;硫化氢在空气充足时燃烧生成二氧化硫和水,在空气不足时燃烧生成硫单质和水;亚硫酸为中强酸
硒和硫同属氧族元素,但硒的核电荷数,原子半径都比硫大,这两种元素除化学性质相似外,硒的非金属性比硫弱,据此可作硫在空气中燃烧生成二氧化硫;与钠能组成化合物Na2S;硫化氢有臭鸡蛋气味,有剧毒;硫化氢在空气充足时燃烧生成二氧化硫和水,在空气不足时燃烧生成硫单质和水;亚硫酸为中强酸 而硒的非金属性比硫弱,所以硒化氢比硫化氢易分解,亚硒酸的酸性比亚硫酸弱,应是弱酸
而硒的非金属性比硫弱,所以硒化氢比硫化氢易分解,亚硒酸的酸性比亚硫酸弱,应是弱酸
本题难度:一般