微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 镁铝合金m g和足量盐酸反应后得到的气体在标准状况下的体积为2.24L,m的数值可能是(?)
A.1.8
B.2.0
C.2.2
D.2.4
参考答案:BC
本题解析:极值法,气体在标准状况下的体积为2.24L,也就是1mol,转移2mol电子,假设都是镁,质量为2.4g,假设都是铝,质量为1.8g,所以1.8g<m<2.4g
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的值,下列有关叙述不正确的是 (? )
A.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为(7/22.4)NA
B.1 mol甲基(―CH3)所含的电子总数为9NA
C.0.5mol 1, 3-丁二烯分子中含有C=C双键数为 NA
D.1 mol碳正离子(CH3+)所含的电子总数为8 NA
参考答案:A
本题解析:略
本题难度:一般
3、选择题 下列叙述中正确的是(?)
A.1 mol氢的质量是1 g
B.1 mol CO的质量为28 g・mol-1
C.阿伏加德罗常数等于6.02×1023
D.3.01×1023个SO2分子约是0.5 mol
参考答案:D
本题解析:A中1 mol氢指代不明,无法计算; B、1 mol CO的质量为28 g;C、阿伏加德罗常数约等于6.02×1023个; D、3.01×1023个SO2分子约是0.5 mol正确。
本题难度:一般
4、填空题 明矾石的主要成分为K2SO4・Al2(SO4)3・2Al2O3・6H2O,此外还含有少量Fe2O3杂质。某校研究小组利用明矾石制备氢氧化铝的流程如下:
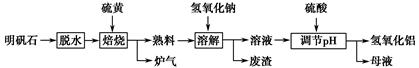
(1)“焙烧”过程中反应的化学方程式为 Al2(SO4)3+
Al2(SO4)3+ S
S
 Al2O3+
Al2O3+ ______↑。
______↑。
(2)分离溶液和废渣的操作是________,“溶解”时反应的离子方程式为_________________________________________________________________。
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是________。
(4)“母液”中可回收的物质是________。
(5)若“焙烧”过程中恰好消耗48 g硫黄,则理论上最终可得到________ g氢氧化铝。
参考答案:(1)2 3 2 9 SO2
(2)过滤 Al2O3+2OH-=2AlO3-+H2O
(3)取最后一次洗涤的滤液于试管中,滴加BaCl2溶液,若无白色沉淀生成,则证明已洗涤干净
(4)K2SO4、Na2SO4
(5)468
本题解析:(1)分析已知的反应物和生成物可知,只有硫元素化合价发生变化,故最终只可能生成SO2。(2)结合流程可知,分离溶液和废渣可用过滤操作;溶解时,Al2O3与碱反应。(3)Al(OH)3沉淀表面吸附有SO42-,故可取最后一次洗涤的滤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则证明已洗涤干净。(4)“母液”中可回收的物质是易溶的K2SO4和Na2SO4。(5)根据反应的化学方程式可知,2Al2(SO4)3~3S,n(S)=1.5 mol,n[Al2(SO4)3]=1 mol,n(Al2O3)=1 mol,明矾石中n(Al2O3)=2 mol,依据铝元素守恒可知,n(Al)=n[Al(OH)3]=6 mol,则氢氧化铝质量为468 g。
本题难度:一般
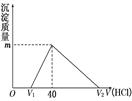
5、选择题 将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是(? )
A.原合金质量为0.92 g
B.标准状况下产生氢气896 mL
C.图中m值为1.56 g
D.图中V2为60 mL
参考答案:C
本题解析:反应后得到20 mL pH=14的溶液,所以n(OH-)=0.02mol,所以需要1mol/L的盐酸20mL来中和,因此V1为20mL,继续加盐酸发生AlO2-+H++H2O=Al(OH)3,Al(OH)3+3H+=Al3++3H2O,因此沉淀AlO2-用掉20mL盐酸,溶解Al(OH)3用掉60mL盐酸,所以V2为100mL。所以Al(OH)3为0.02mol,则m为1.56g,原混合物中含有Al为0.54g,当盐酸加100mL时,溶液中的溶质为NaCl和AlCl3,又知n(Cl-)=0.1mol,n(Al3+)=0.02mol,所以n(Na+)=0.04mol。所以原混合物中有Na为0.04mol,质量为0.92g,所以原混合物的质量为0.92g+0.54g=1.46g。反应过程中产生氢气0.05mol,1120mL。所以C项正确,答案选C。
点评:搞清楚图像中每一段发生的变化以及图像中数字的含义。
本题难度:一般