微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 砷污染事件曾多次发生,含砷化合物一般都有毒性,其中以砒霜(As2O3)毒性最强,As2O3可用于制造杀虫剂和灭鼠剂等,是两性偏酸性氧化物,其无色晶体在193℃升华,微溶于水生成H3AsO3;其对应的盐也有毒性。其中碱金属对应的盐易溶于水,其他金属对
应的盐几乎不溶于水。根据以上信息,下列说法正确的是?
A.As2O3是砷的最高价含氧酸的酸酐







B.As2O3的晶体为原子晶体
C.如不慎As2O3不慎撒落河水中,可投入纯碱以消除污染
D.如不慎As2O3不慎撒落河水中,可投入生石灰以消除污染
参考答案:
D
本题解析:
在H3AsO4中As元素为+5价,其酸酐为As2O5而不是As2O3。因As2O3为无色晶体,在193 ℃时可升华,所以As2O3为分子晶体。由题意可知碱金属的亚砷酸盐(如Na3AsO3)易溶于水且有毒,而其他金属的亚砷酸盐〔如Ca3(AsO3)2〕难溶于水,故应用生石灰消除砒霜对河水的污染。
本题难度:一般
2、填空题 硝酸是极其重要的化工原料,工业上将产生的NO2在密闭容器中用水多次反复循环吸收制备硝酸。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:
______________________________________________________________。
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。
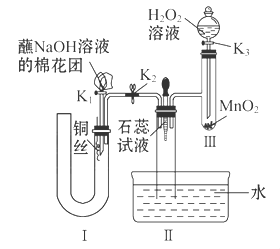
①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至 后,迅速关闭K1,观察到U形管内的现象是____________________________________________________。
②装置Ⅲ中发生反应的化学方程式为_______________________________。
③蘸NaOH溶液的棉花团的作用是___________________________________。
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,长玻璃管中并未充满液体。设计简单方法检验长玻璃管中的气体是否含NO__________________________________________________。
参考答案:(1)4NO2+O2+2H2O=4HNO3(或分成两个方程式写)
(2)①U形管右侧胶塞下沿 U形管左端液面高于右端,铜丝慢慢溶解,产生无色气体,溶液逐渐变蓝(至少答三点) ②2H2O2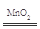 2H2O+O2↑
2H2O+O2↑
③吸收氮的氧化物防止污染环境
④再打开K3,若观察到长玻璃管中气体迅速变为红棕色,则证明余气含NO,若无颜色变化,则证明不含NO(其他合理答案也可)
本题解析:根据实验目的和所放置的试剂可以推断,Ⅰ装置的作用是制备NO,Ⅲ装置的作用是制备O2,Ⅱ装置的作用是证明NO也可以与氧气和水共同作用生成HNO3。
(1)NO2经多次氧化、用水吸收的循环操作,充分转化为硝酸的化学方程式为4NO2+O2+2H2O=4HNO3。
(2)①注入稀硝酸应至U形管右侧胶塞下沿,迅速关闭K1后,U形管左端液面高于右端,铜丝慢慢溶解,产生无色气体,溶液逐渐变蓝。
②装置Ⅲ中发生反应的化学方程式为:2H2O2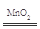 2H2O+O2↑。
2H2O+O2↑。
③蘸NaOH溶液的棉花团的作用是吸收氮的氧化物,防止污染环境。
④再打开K3,若观察到长玻璃管中气体迅速变为红棕色,则证明余气含NO,若无颜色变化,则证明不含NO。
本题难度:一般
3、选择题 将空气中氮气转化为氮的化合物过程中称为固氮。下面能实现人工固氮的是
 ?
?
A.闪电
B.电解饱和食盐水


C.大豆的根瘤
D.合成氨工厂
参考答案:D
本题解析:略
本题难度:简单
4、选择题 下列关于室温下氨水的叙述,正确的是?
?[? ]
A.同pH同体积的氨水和NaOH溶液,能分别与同浓度同体积的盐酸恰好完全中和
B.加水稀释0. 10 mol・L-1的氨水,溶液中n(OH-)减小
C.若温度不变,在氨水中加入少量NH4Cl固体,氨水的电离度和电离平衡常数均变小
D.氨水中的离子浓度关系满足:[OH-]=[H+]+[NH4+]
参考答案:D
本题解析:
本题难度:简单
5、实验题 为探究铜与稀硝酸反应产生的气体主要是NO,某课外活动小组设计了下列实验。图中D为止水夹,F是装有一半空气的注射器,其中加热装置和固定装置均已略去。
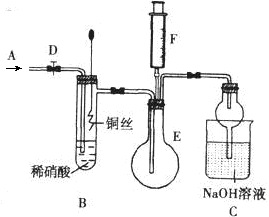
请回答有关问题:
(1)组装好装置后,关闭D,若装置的气密性良好,向外抽注射器活塞,C装置中有什么现象?
?;
(2)反应开始前要向体系中通入气体A,为什么??;A可以是??(填序号)?①N2?②O2?③空气?④CO2
(3)当完成装置A的实验目的后,关闭D,再将装置B中的铜丝插入稀硝酸。B中反应的离子方程式是:?。
(4)反应一段时间后,将F中空气推入E中,证明生成了NO实验现象是:?。
(5)装置C的作用是:?。
参考答案:(1)有一段水柱上升(2分)
(2)赶尽整个装置内的空气,避免对NO的检验造成干扰(2分)
①④(多选、少选、错选不给分)(2分)
(3)3Cu + 8H+?+? 2NO3― = 3Cu2+ + 2NO↑ + 4H2O(2分)
(4)E中无色气体变为红棕色(2分)
(5)吸收多余的氮氧化物,防止污染空气(2分)
本题解析:本题为探究铜与稀硝酸反应产生的气体主要是NO的实验,明确NO容易被空气中的氧气氧化是解答本题的关键,结合实验的基本操作及氮的氧化物的性质来解答。(1)分析题给装置知,关闭D,若装置的气密性良好,向外抽注射器活塞,装置内气压降低,外界大气压把水压入C装置,C装置中有一段水柱上升;(2)反应开始前,体系中含有空气,其中的氧气能与一氧化氮反应生成二氧化氮,要向体系中通入气体A的目的是赶尽整个装置内的空气,避免对NO的检验造成干扰;A可以是 N2和CO2,选①④;(3)将装置B中的铜丝插入稀硝酸,二者反应生成硝酸铜、一氧化氮和水,反应的离子方程式是:3Cu + 8H+?+ 2NO3― = 3Cu2+ + 2NO↑ + 4H2O;(4)反应一段时间后,将F中空气推入E中,NO和空气的氧气反应生成红棕色的NO2,实验现象是:E中无色气体变为红棕色;(5)NO、NO2都有毒,能污染环境,氮的氧化物能被NaOH溶液吸收,装置C的作用是:吸收多余的氮氧化物,防止污染空气。
本题难度:一般