微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中,正确的是
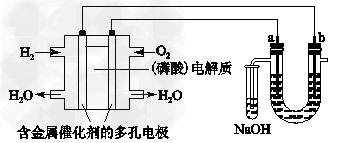
[? ]
A.电池工作时,正极反应式为:O2+2H2O+4e-===4OH-
B.电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量损耗,当电池中消耗0.02?g?H2时,b极周围会产生0.04?g?H2
参考答案:B
本题解析:
本题难度:一般
2、选择题 下图是一原电池的装置,关于它的说法正确的是?
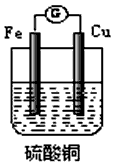
[? ]
A.装置中铜是负极
B.铜表面的反应为:2H++2e-=H2↑
C.电流的方向是从铁经导线流向铜
D.构成原电池后,铁与硫酸铜的反应速率加快
参考答案:D
本题解析:
本题难度:一般
3、实验题 某小组按图1所示的装置探究铁的吸氧腐蚀。完成下列填空:
 ?
?
(1)图2 是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式;在方括号内用箭头表示出电子流动的方向。
(2)写出正、负极反应的方程式。正极:?,负极:?。
(3)按图1装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是?。
a.用纯氧气代替具支试管内的空气
b.用食盐水浸泡过的铁钉再蘸取铁粉和炭粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(4)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施?(填“可行”或“不行”)。
(5)有同学观察到图1装置在组装时就会使导管中液面低于试管中液面,导致实验时导管中液柱上升需要更多的时间。图1装置组装时,使导管中液面低于试管中液面的原因是?。消除这一现象的简单操作是?。
参考答案:(1)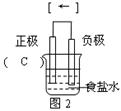 (各1分,共2分)
(各1分,共2分)
(2)2H2O+ O2+4e→4OH- (1分)Fe-2e→Fe2+(1分)
(3)a? b? c (3分)
(4)不行(1分)
(5)不论是后塞塞子还是后将导管插入水中,都会造成容器中气体体积减小,压强增大,使导管中液面低于试管中液面(2分);用针筒从橡胶塞处抽气或把橡皮塞换成带分液漏斗的单孔塞(2分,合理即给分)
本题解析:(1)氯化钠溶液显中性,所以在食盐水中,铁钉发生吸氧腐蚀,铁作负极,碳作正极,电子从铁沿导线流向正极碳,其图象为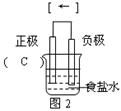
(2)该装置中,负极上铁失电子发生氧化反应,电极反应式为Fe-2e-=Fe2+;正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4 e-=4OH?-。
(3)a.用纯氧气代替具支试管内的空气,氧气的浓度增大,反应速率加快,故a正确;b.用食盐水浸泡过的铁钉再蘸取铁粉和炭粉的混合物,增大反应物的接触面积,反应速率加快,故b正确;c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水,改变相同的压强即改变相同的体积,毛细尖嘴管上升的高度大于玻璃导管,且红墨水现象更明显,故c正确,所以答案选a?b?c。
(4)温度越高,氧气的溶解度越小,反应速率越小,所以用酒精灯加热具支试管,降低反应速率,因此这一措施是不行的。
(5)一定量的气体,压强与气体体积成反比,体积越小,压强越大,导致导管中液面低于试管中液面,所以可以采用用针筒从橡胶塞处抽气或把橡皮塞换成带分液漏斗的单孔塞的方法消除这一现象。因此使导管中液面低于试管中液面的原因是不论是后塞塞子还是后将导管插入水中,都会造成容器中气体体积减小,压强增大,使导管中液面低于试管中液面;所以消除这一现象的简单操作是用针筒从橡胶塞处抽气或把橡皮塞换成带分液漏斗的单孔塞。
本题难度:一般
4、选择题 将表面发黑(黑色物质为Ag2S)的银器按下图方法处理,一段时间后银器光亮如新。下列说法正确的是
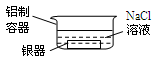
A.铝质容器为正极,银器为负极
B.反应前后银器质量不变
C.Ag2S被还原生成单质银
D.总反应为2Al+3Ag2S → 6Ag+ Al2S3
参考答案:C
本题解析:根据题意,发生的电极反应为:负极:2Al-6e-=Al3+;正极:3Ag2S+6e-=6Ag+3S2-,A错误。处理过程中,硫化银变为银单质,质量减少,B错误;硫化银发生还原反应,生成银单质,C正确;原电池总反应方程式:3Ag2S+2Al+6H2O=6Ag+2Al(OH)3↓+3H2S↑,D错误;
本题难度:一般
5、选择题 将Al片和Cu片用导线相连,一组插入浓HNO3溶液中,一组插入稀NaOH溶液中,分别形成了原电池。则在两个原电池中正极分别为:(?)
A.Al片、Al片;
B.Cu片、Al片;
C.Al片、Cu片;
D.Cu片、Cu片
参考答案:C
本题解析:在判断原电池的正负极时通常情况下是教活泼的作为负极。但在具体的原电池中还需要根据电解质综合进行分析。在浓硝酸中铝会发生钝化,所以此时应该是铜作负极。在氢氧化钠溶液中,铝可以与氢氧化钠发生氧化还原反应,而铜不能,故铝作负极。答案C。
本题难度:简单