微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知①2CuO+C 2Cu+CO2↑;②2Mg+CO2
2Cu+CO2↑;②2Mg+CO2 2MgO+C,由此得出下列结论正确的是(? )
2MgO+C,由此得出下列结论正确的是(? )
A.还原性:Mg>C>Cu
B.还原性:Mg>Cu>C
C.氧化性:CuO>CO2>MgO
D.氧化性:CuO>MgO>CO2
参考答案:AC
本题解析:由①可知氧化性CuO>CO2,还原性C>Cu。由②可知氧化性CO2>MgO,还原性Mg>C。
本题难度:简单
2、选择题 在水溶液中发生下列反应:YO3n-+3S2-+6H+=Y-+3S↓+3?H2O?,下列说法不正确的是在
A.YO3n-中Y的化合价是+5
B.n=1()
C.Y元素原子的最外层电子数为5
D.还原性:S2->Y-
参考答案:C
本题解析:根据反应YO3n-+3S2-+6H+=Y-+3S↓+3?H2O可知3mol S2-失去6mol电子,所以1molYO3n-就得到6mol电子,其中Y元素的化合价降低6个单位,所以在YO3n-中Y的化合价是=5价,则n=1,但Y的最低化合价是-1价,所以属于第ⅦA,最外层含有7个电子。依据还原剂的还原性强于还原产物的,选项D正确。答案是C。
本题难度:简单
3、选择题 研究表明:多种海产品体内含有+5价的砷(As)元素,对人体无毒,而砒霜的成分是As2O3,有剧毒;青菜中含有维生素C。专家忠告:不要同时大量食用海鲜和青菜,否则容易中毒。下面有关解释不正确的是
[? ]
A.As2O3中As元素为+3价
B.致人中毒过程中砷发生氧化反应
C.维生素C能将+5价砷还原成As2O3
D.维生素C具有还原性
参考答案:B
本题解析:
试题分析:
选项A,As2O3中As元素为+3价,因O是-2价;
选项B,致人中毒过程中砷发生还原反应,As化合价降低;
选项C,维生素C能将+5价砷还原成As2O3,As元素的化合价降低;
选项D,维生素C具有还原性。
故选:B
本题难度:简单
4、填空题 写出下列反应的化学方程式。若是氧化还原反应,请用“双线桥”分析(指出氧化剂、还原剂)。
(1)电解食盐水制取氯气?
(2)氯气通入溴化钾溶液中?
(3)漂白粉中的次氯酸钙与水蒸气、二氧化碳作用??
参考答案:见解析
本题解析:
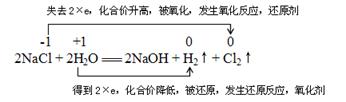

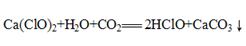
点评:化学方程式的书写是中学化学学习的重点。应注意反应的条件,沉淀和气体符号。注意细节。同时双线桥的表示中,要先标出化合价。
本题难度:一般
5、填空题 (12分)化学学习中有很多形如“A+B→C+D”的反应,请根据不同的情况回答下列问题:
(1)如果上式中A、B、C、D均为多核10电子微粒,其中A为阳离子,B为阴离子,C、D均为分子,且C的相对分子质量比D大1.
则:①A+B→C+D表示的离子方程式为?。
②标准状况下,若2.24L的D被100mL 2mol/L盐酸吸收,则所得溶液中各离子浓度从大到小的顺序为_?___.
(2)如果上式中A、C为生活中常见的金属单质,B、D为两种氧化物且它们的摩尔质量比为12:17,其中D能与NaOH溶液反应.
则:①A+B→C+D表示的化学方程式为?.
②D与NaOH溶液反应的化学方程式为___?_.
③工业上,将B、D按一定的量溶于盐酸后,继续通入气体Z,再加入NaOH溶液调节pH可得高效净水剂(化学式为CA(OH)aCl6-n ),则气体Z的作用是__?__,B、D的最佳物质的量之比是___?_.
④工业上,通常第一步先用C与过量稀硫酸作用得溶液X:第二步再往溶液X中加入亚硝酸钠来制备C(OH)SO4,同时有气体NO生成,写出第二步反应的化学方程式为__?__。
参考答案:(共12分)(1)① NH4+ + OH- = H2O + NH3? 2分
② c (Cl-) >c (H+)> c (NH4+)> c (OH-)? 2分
(2)①2Al+ 3FeO ="3Fe" +Al2O3? 2分
② Al2O3?+2NaOH ="2" NaAlO2 +H2O? 2分
③ 将Fe2+氧化为Fe3+? 1分; 2:1? 1分
④? 2FeSO4? +2 NaNO2? + H2SO4 =? 2Fe(OH)SO4? +Na2SO4? +2 NO↑? 2分
本题解析:(1)①多核10电子微粒有如H2O、NH2-、 NH3、H3O+、CH4、NH4+,由题意可推知该离子方程式为NH4+ + OH- = H2O + NH3 ②所得溶液相当于0.1molNH4Cl和0.1molHCl的混合物,所以各离子浓度从大到小的顺序为c (Cl-) >c (H+)> c (NH4+)> c (OH-);
(2)①由题意可知,该反应为2Al+ 3FeO =3Fe? +Al2O3,②Al2O3与NaOH溶液反应的化学方程式为Al2O3?+2NaOH ="2" NaAlO2 +H2O③由高效净水剂的化学式可知,气体Z为氯气,作用是将Fe2+氧化为Fe3+,B、D的最佳物质的量之比为2:1,④Fe与过量稀硫酸作用得FeSO4溶液,第二步反应为FeSO4和NaNO2反应,由产物Fe(OH)SO4可知反应有H2SO4参与,可推知该反应的化学方程式为2FeSO4? +2 NaNO2? + H2SO4 =? 2Fe(OH)SO4? +Na2SO4? +2 NO↑
点评:本题内容综合性较强,主要考查多核电子微粒、弱电解质的电离、常见金属及其重要化合物、氧化还原反应等相关的知识,有一定难度,需要考生平时多积累知识。
本题难度:一般