微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
www.^91exam.org
绝密★启用前
2015年普通高等学校招生全国统一考试
化 学
注意事项:
1.本试卷分第I卷(选择题)和第II卷(非选择题)两部分。答卷前,考生务必将自己的姓名.准考证号填写在答題卡上。
2.回答第I卷时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑, 如需改动,用橡皮擦干净后,再选涂其它答案标号。写在本试卷上无效。
3.回答第II卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回.
可能用到的相对原子质量: H 1 C 12 N 14 O16 Zn65 Ag108 Cl 35.5 Fe56 Cu64
第I卷
一.选择题:本题共6小题。每小题2分,共12分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关。下列应用中利用了物质氧化性的是
A.明矾净化水 B.纯碱去油污
C.食醋除水垢 D.漂白粉漂白织物
2.下列离子中半径最大的是
A.Na+ B.Mg2+ C.O2- D. F-
3.0.1mol下列气体分别与1L0.lmol·L-1的NaOH溶液反应,形成的溶液pH最小的是
A. NO2 B.SO2 C.SO3 D.CO2
4.己知丙烷的燃烧热△H=-2215KJ·mol-1,若一定量的丙烷完全燃烧后生成18g水,则放出的热量约为
A. 55 kJ B.220 kJ C. 550 kJ D.1108 kJ
5.分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)
A.3种 B. 4种 C. 5种 D.6种
6.己知在碱性溶液中可发生如下反应:
2R(OH)3 + 3C1O- + 4OH- = 2RO4n-+3Cl- +5H2O。则RO4n-中 r 的化合价是
A. +3 B. +4 C. +5 D.+6
7.下列叙述正确的是
A.稀盐酸可除去烧瓶内残留的MnO2 B.可用磨口玻璃瓶保存NaOH溶液
C.稀硝酸可除去试管内壁的银镜 D.煮沸自来水可除去其中的Ca(HCO3)2
8.10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是
A.K2SO4 B.CH3COONa C.CuSO4 D.Na2CO3
9.下列反应不属于取代反应的是
A.淀粉水解制葡萄糖 B.石油裂解制丙烯
C.乙醇与乙酸反应制乙酸乙酯 D.油脂与浓NaOH反应制高级脂肪酸钠
10.下列制定微粒的数目相等的是
A.等物质的量的水与重水含有的中子数
B.等质量的乙烯和丙烯中含有的共用电子对数
C.同温.同压同体积的CO和NO含有的质子数
D.等物质的量的铁和铝分别于足量氯气完全反应时转移的电子数
11.下列曲线中,可以描述乙酸(甲,Ka=1.8×10-5)和一氯乙酸(乙,Ka=1.4×10-3)在水中的电离度与浓度关系的是
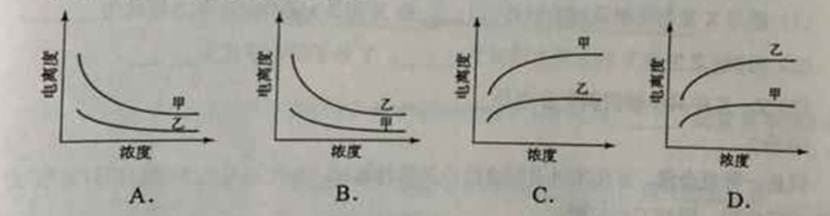
12.a.b.c.d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c。下列叙述错误的是
A.d元素的非金属性最强
B.它们均存在两种或两种以上的氧化物
C.只有a与其他元素生成的化合物都是离子化合物
D.b.c.d与氢形成的化合物中化学键均为极性共价键
13 (8分)
乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:
回答下列问题:
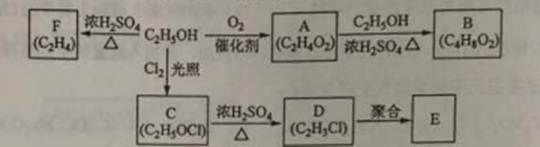
(1)A的结构简式为 。
(2)B的化学名称是 。
(3)由乙醇生产C的化学反应类型为 。
(4)E是一种常见的塑料,其化学名称是 。
(5)由乙醇生成F的化学方程式为 。
14.(8分)
单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备,其中X为Z的氧化物,Y为氢化物,分子结构与甲烷相似,回答下列问题:
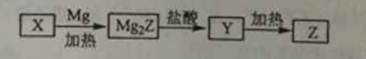
(1)能与X发生化学反应的酸是 ;由X制备Mg2Z的化学方程式为 。
(2)由Mg2Z生成Y的化学反应方程式为 ,Y分子的电子式为 。
(3)Z.X中共价键的类型分别是 。
15.(9分)
银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。回答下列问题。
(1)久存的银制器皿表面会变黑,失去银白色的光泽,原因是 。
(2)已知Ksp(AgCl)=1.8×10-10,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中的Ag+的浓度为 mol·L-1,pH为 。
(3)AgNO3溶液光照易分解,生成Ag和红棕色气体等物质,其光照分解的化学方程式为 。
(4)右图所示原电池正极的反应式为 。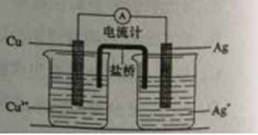
16.(8分)
氨是合成硝酸.铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的PH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,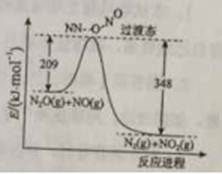 r若生成1molN2,其△H= kJ·mol-1,
r若生成1molN2,其△H= kJ·mol-1,
海南化学
17.(11分)
工业上,向500—600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行试验。

回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为 ,装置B中加入的试剂是 。
(2)制取无水氯化亚铁的实验中,装置A用来制取 。尾气的成分是 。若仍用D的装置进行尾气处理,存在的问题是 、 &n