微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 2008年北京奥运会“祥云”火炬用的是环保型燃料――丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为2221.5?kJ/mol,下列有关说法正确的是?
[? ]
A.奥运火炬燃烧主要是将化学能量转变为热能和光能
B.丙烷的沸点比正丁烷高
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)===3CO2(g)+4H2O(g) ΔH=-2221.5kJ/mol
参考答案:A
本题解析:
本题难度:一般
2、选择题 从手册上查得:H-H、Cl-Cl和?H-Cl的键能分别为436、243和431kJ?mol-1,请用此数据估计,下列热化学方程式正确的是( )
A.H2(g)+Cl2(g)=2HCl(g);△H=-183kJ?mol-1
B.H2(g)+Cl2(g)=2HCl(g);△H=+183kJ?mol-1
C.H2(g)+Cl2(g)=2HCl(g);△H=-91.5kJ?mol-1
D.H2(g)+Cl2(g)=2HCl(g);△H=+91.5kJ?mol-1
参考答案:A
本题解析:
本题难度:简单
3、选择题 下列热化学方程式书写正确的是(△H的绝对值均正确)
[? ]
A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g)△H= -1367.0 kJ/mol(燃烧热)
B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l)△H= +57.3kJ/mol(中和热)
C.S(s)+O2(g)==SO2(g) △H= -269.8kJ/mol(反应热)
D.2NO2==O2+2NO △H= +116.2kJ/mol(反应热)
参考答案:C
本题解析:
本题难度:简单
4、填空题 (6分)甲醇(CH3OH)和二甲醚(CH3OCH3)被称为21世纪的新型燃料。以CH4和H2O为原料制备甲醇和二甲醚的工业流程如下:
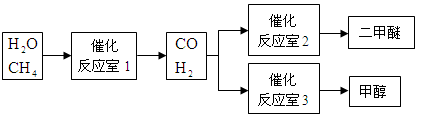
根据要求回答下列问题:
(1)“反应室1”在一定条件下反应的化学方程式为 。
(2)水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) CH3OH(g) ΔH= -90.8kJ・mol-1
CH3OH(g) ΔH= -90.8kJ・mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH= -23.5kJ・mol-1
CH3OCH3(g)+H2O(g) ΔH= -23.5kJ・mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH= -41.3kJ・mol-1
CO2(g)+H2(g) ΔH= -41.3kJ・mol-1
完成热化学反应方程式:3H2(g)+3CO(g) CH3OCH3(g)+CO2(g);ΔH= 。
CH3OCH3(g)+CO2(g);ΔH= 。
参考答案:(1)H2O+CH4一定条件CO+3H2(3分,不写条件扣1分)
(2)-246.4kJ・mol-1(3分,漏写单位扣1分)
本题解析:(1)从流程可知、水和甲烷反应生成一氧化碳和氢气,所以方程式为:H2O+CH4一定条件CO+3H2。(2)根据盖斯定律,①×2+②+③,计算反应热为-246.4kJ・mol-1。
考点:盖斯定律。
本题难度:一般
5、填空题 已知 0.4 mol 液态肼和足量H2O2反应生成氮气和水蒸气时放出256.64 kJ的热量。
(1)写出肼和H2O2反应的热化学方程式: 。
(2)已知H2O(l)=H2O(g) ΔH="+44" kJ/mol,则16 g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是 。
(3)上述反应应用于火箭推进器,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是 。
(4)向次氯酸钠溶液中通入一定物质的量的氨气可生成肼,写出反应的离子方程式: ,该反应的还原产物是 。
参考答案:(1)N2H4(l)+2H2O2(l) N2(g)+4H2O(g)
N2(g)+4H2O(g)
ΔH="-641.6" kJ/mol
(2)408.8 kJ
(3)产物为氮气和水,对环境无污染
(4)2NH3+ClO- N2H4+Cl-+H2O NaCl
N2H4+Cl-+H2O NaCl
本题解析:(1)首先根据题意确定反应物和生成物,然后写出化学方程式:N2H4+2H2O2 N2↑+4H2O。0.4 mol液态肼和足量H2O2反应生成氮气和水蒸气时放出256.64 kJ的热量,则1 mol液态肼和足量H2O2反应时放出热量为:2.5×256.64 kJ="641.6" kJ,由此可确定上述反应的热化学方程式的ΔH。
N2↑+4H2O。0.4 mol液态肼和足量H2O2反应生成氮气和水蒸气时放出256.64 kJ的热量,则1 mol液态肼和足量H2O2反应时放出热量为:2.5×256.64 kJ="641.6" kJ,由此可确定上述反应的热化学方程式的ΔH。
(2)16 g液态肼的物质的量为0.5 mol,则与足量双氧水反应生成0.5 mol N2和2 mol H2O(l)时放出热量为:0.5 mol×641.6 kJ/mol+2 mol×44 kJ/mol="408.8" kJ。
(3)反应生成的物质是N2和H2O,对环境无污染。
(4)氨气中氮元素的化合价为-3价,肼分子中氮元素的化合价为-2价,则氨气是还原剂,次氯酸钠是氧化剂,还原产物是NaCl,然后根据电子转移守恒以及电荷守恒即可写出离子方程式。
本题难度:一般