��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�������£�A��B��Ӧ������C��D���������仯���£�

�����йط�ӦA+B=C+D��˵����ȷ���ǣ�?��
A����Ӧǰ��ԭ�ӵ��������Ŀ���ܸı�
B���÷�Ӧ���������仯����һ����������ԭ��Ӧ
C�����÷�ӦΪ���ȷ�Ӧ��������ȷ�Ӧ��һ���ܽ���
D���÷�Ӧ��ѭ�����غ㣬����һ���������仯
2��ѡ���� þ�����۾��Ȼ�ϣ��μӼ���ˮ���������ҷ�Ӧ��������������ɫ���������������������
A��H2O������
B����ɫ������I2
C���÷�Ӧ�Ƿ��ȷ�Ӧ
D����Ӧ�����ʵ�����������
3��ѡ���� ����˵����ȷ���ǣ�?��
A������ѹǿ�������������
B�������¶ȣ�����Ӱٷ�������
C��ʹ�ô����ܽ��ͷ�Ӧ��
D�����뷴Ӧ�ʹ����Ӱٷ������ӣ���ѧ��Ӧ��������
4������� ����2SO2(g)+O2(g) 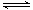 2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����ش��������⣺
2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����ش��������⣺
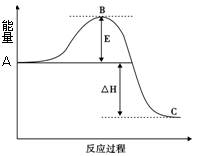
��1��ͼ��A��ʾ?��
��2��E�Ĵ�С�Ը÷�Ӧ���ʱ�����Ӱ�죿?��
�÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�������ǽ��ͣ�?��
��3��ij�¶��£���1L�ܱ������п�ʼ����2molSO2��1molO2����V2O5��������ʱ��Ӧ�ﵽƽ�⣬ѹǿ��СΪ��ʼʱ��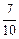 ��������ͬ�¶��£���ͬ��������ܱ������г���2mol��SO3��Ҳ��V2O5��������ʱ��Ӧ�ﵽƽ�⣬����¶��·�Ӧ2SO3 (g) ?
��������ͬ�¶��£���ͬ��������ܱ������г���2mol��SO3��Ҳ��V2O5��������ʱ��Ӧ�ﵽƽ�⣬����¶��·�Ӧ2SO3 (g) ?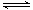 ?2SO2(g) + O2(g)��ƽ�ⳣ����д��������̣�
?2SO2(g) + O2(g)��ƽ�ⳣ����д��������̣�
����ѧ�Լ��������͵�ƹ�ҵ�ŷŵķ�ˮ�г�����20~100mg.L-1Cr(��)�����ú�Cr(��)��ˮ�����˵ij�θ�ȣ���֪Cr(��)�Ķ�����Cr(��)��0.5%�����ҹ涨��ҵ��ˮ��Cr(��)�����ŷű�Ϊ0.1mg.L-1����ҵ�ϳ��û�ѧ���͵�ⷨ������Cr(��)��ˮ���ٽ�Cr(��)ת���ɳ�����ȥ��ij�о���ѧϰС��Ϊ�о���ˮ�ľ��������������ʵ�����̣�
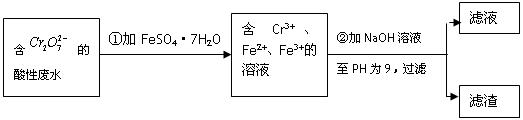
��1����ƽ�ڢٲ���Ӧ�����ӷ���ʽ��
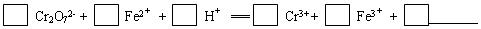
��2���ڢڲ�����PH��ֽ�ⶨ��ҺPH�IJ����ǣ�
?
��3�����һ�����װ��Ҳ����ʵ������Ŀ�ģ�װ������ͼ����������ʯī���缫����

�缫���ϣ�cΪ��??
�缫��Ӧ��d����?
5��ѡ���� ��֪�Ȼ�ѧ����ʽ��SO2(g)+ 1/2O2(g)  ?SO3(g) ��H= �D98.32kJ��mol���������г���2molSO2��1molO2��ַ�Ӧ�����շų�������Ϊ?��?��
?SO3(g) ��H= �D98.32kJ��mol���������г���2molSO2��1molO2��ַ�Ӧ�����շų�������Ϊ?��?��
A��196.64kJ
B��196.64kJ��mol
C����196.64kJ
D����196.64kJ