微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 如图所示“合成氨”的演示实验(夹持仪器均已省略)。在Y形管的一侧用Zn粒和稀H2SO4反应制取H2,另一侧用NaNO2固体和NH4Cl饱和溶液反应制取N2,N2和H2混合后通过还原铁粉来合成NH3,再将产生的气体通入酚酞试液中,若酚酞试液变红,则说明产生了氨气。
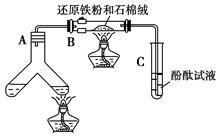
某课外活动小组通过查阅资料和多次实验,得到了如下信息:
信息一:NaNO2固体和饱和NH4Cl溶液混合加热的过程中发生如下反应:
①NaNO2+NH4Cl ?NH4NO2+NaCl
?NH4NO2+NaCl
②NH4NO2 NH3↑+HNO2
NH3↑+HNO2
③2HNO2 N2O3↑+H2O
N2O3↑+H2O
④2NH3+N2O3 2N2+3H2O
2N2+3H2O
信息二:查阅资料,不同体积比的N2、H2混合气体在相同实验条件下合成氨,使酚酞试液变红所需要的时间如下:
N2和H2的体积比
| 5∶1
| 3∶1
| 1∶1
| 1∶3
| 1∶5
|
酚酞变红色所需时间/min
| 8~9
| 7~8
| 6~7
| 3~4
| 9~10
|
?
据此回答下列问题:
(1)Y形管左侧管中发生反应的离子方程式________________________。
(2)铁粉撒在石棉绒上的目的是_________________________________
(3)课外活动小组的同学们认为,该实验中即使酚酞变红也不能说明N2和H2反应合成了NH3,得出此结论的理由是________________________。
请你另设计一个简单的实验验证你的理由____________________。欲解决这一问题,可以选用下图中的________装置连接在原装置中的________和________之间。
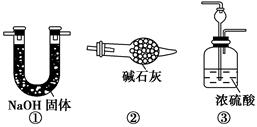
(4)在上述实验过程中,为尽快观察到酚酞试液变红的实验现象,应该控制N2和H2的体积比为________比较适宜;但该装置还难以实现此目的,原因是______________________________________。
(5)实验过程中通入试管C中的气体成分有________。
参考答案:(1)Zn+2H+=Zn2++H2↑
(2)增大混合气体与催化剂的接触面积,使反应进行得更快
(3)从分步反应可知,产生N2的过程中,有可能直接产生氨气 将混合加热产生的气体直接通入酚酞试液,若试液变红,则说明理由成立;否则,说明理由不成立 ③ A B
(4)1∶3 无法控制通入B中N2和H2的体积比
(5)NH3、N2、H2
本题解析:(1)根据Y形管右侧管需加热,说明右侧管反应制取N2,左侧管反应制取H2。(2)铁粉撒在石棉绒上的目的是增大与混合气体的接触面积,从而提高催化效率 ,增大反应速率。(3)因为NH4NO2分解可产生NH3,所以不能证明N2和H2反应生成了NH3。直接将Y形管中混合气体通入酚酞试液,若试液变红,则理由成立,否则理由不成立。在A、B之间加一个除NH3的装置,排除了NH3的干扰。(4)由表可知V(N2)∶V(H2)=1∶3时,反应最快,在Y形管中,无法控制气体的体积。(5)气体成分中有生成的NH3,同时还有未反应的N2、H2。
本题难度:一般
2、实验题 (13分)硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3・5H2O)。
I.[查阅资料]
(1)Na2S2O3・5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
Ⅱ.[制备产品]
实验装置如图所示(省略夹持装置)
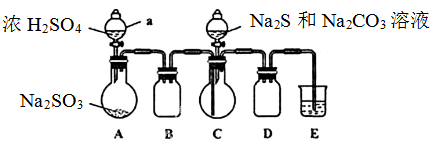
实验步骤:
(1)检查装置气密性,按图示加入试剂。仪器a的名称是____;E中的试剂是___(选填下列字母编号)。
A.稀H2SO4? B.NaOH溶液? C.饱和NaHSO3溶液
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合液,滤液经____(填写操作名称)、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.[探究与反思]
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)为减少装置C中生成的Na2SO4的量,在不改变原有装置的基础上对原有实验步骤(2)进行了改进,改进后的操作是_______。
(3)Na2S2O3・5H2O的溶解度随温度升高显著增大,所得产品通过_____方法提纯。
参考答案:Ⅱ.(1)分液漏斗;B?(3)蒸发
Ⅲ. (1)过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀HCl。
(2)先向A中烧瓶滴加浓硫酸,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3混合溶液。(3)重结晶
本题解析:Ⅱ.[制备产品]
(1)根据仪器的构造特点可知,仪器a的名称是分液漏斗。根据装置可知,A装置是制备SO2的,C装置是制备得Na2S2O3,BD装置是防倒吸的,由于SO2有毒,需要尾气处理,因此E装置是吸收SO2的。由于SO2是酸性氧化物,可以用氢氧化钠溶液吸收,即E中的试剂是氢氧化钠溶液,答案选B。
(3)由于Na2S2O3・5H2O是无色透明晶体,易溶于水,因此要从溶液中得到硫代硫酸钠晶体,责问需要经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.[探究与反思]
(1)Na2S2O3・5H2O的稀溶液与BaCl2溶液混合无沉淀生成,而实验过程中有白色沉淀生成,因此要进一步验证,则可以向白色沉淀中滴加稀盐酸,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)由于亚硫酸盐易被氧化生成硫酸盐,而装置中含有空气,空气能氧化亚硫酸盐,所以为减少装置C中生成的Na2SO4的量,改进后的措施是先向A中烧瓶滴加浓硫酸,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3混合溶液。
(3)由于Na2S2O3・5H2O的溶解度随温度升高显著增大,因此所得产品通过重结晶方法提纯。
本题难度:一般
3、实验题 为探究氯气的性质,某同学做了如下图所示的实验,将少量试剂分别放入培养皿中的相应位置,已知:
KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。请回答下列问题:

(1)用单线桥表示生成氯气的反应电子转移的方向和数目:
KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(2)实验A的现象是_______,反应的离子方程式为_________ 。
(3)实验D的现象是 ___________,反应的离子方程式为_____________ ,这一实验说明氧化性Cl2 __________I2(填“>”或“<”)。
(4)实验C的现象是紫色石蕊溶液先变红,后褪色,使石蕊试液变红的反应的离子方程式为 _____________。为了探究褪色原因,这位同学又做了下图所示实验,将干燥的氯气通入双通管中,其中a为干燥的红纸条,b为湿润的红纸条。
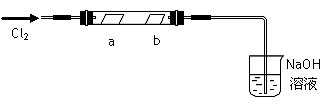
①实验现象是:a ___________,b___________ 。NaOH溶液的作用 ___________。
②该实验说明具有漂白作用的物质是_______________ 。
③将氯气通入水中形成黄绿色的氯水,见光放置数天后黄绿色会褪去,同时失去漂白作用,原因是___________________ (用化学方程式表示)。
(5)实验B的实验现象是______________ ,工业上利用与实验B类似的反应制备漂白粉,制漂白粉的化学方程式为_________________ 。
参考答案:(1)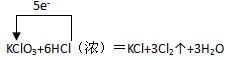
(2)浅绿色溶液变为红色溶液;2Fe2++Cl2==2Fe3+ +2Cl-。
(3)无色溶液变为蓝色;2I-+Cl2==I2+2Cl- ;>。
(4)Cl2+H2O==H++Cl-+HClO;
①a:不褪色;b:褪色;吸收Cl2,防止污染空气;
②HClO;
③ 2HClO  2HCl+O2↑
2HCl+O2↑
(5)红色溶液褪色;2Ca(OH)2+2Cl2==Ca(ClO)2+CaCl2+2H2O。
本题解析:
本题难度:一般
4、实验题 (9分)用如图所示装置(夹持仪器省略)进行实验,将液体A逐滴加入到固体B中,回答下列问题:
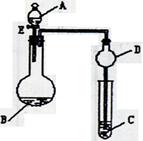
(1)图中D装置在实验中的作用是??。
(2)若 A为30%H2O2溶液,B为MnO2,C盛有氢硫酸(H2S)饱和溶液,旋开E后,C中出现浅黄色浑浊的现象,写出C中发生反应的化学方程式为?。
(3)若A为浓盐酸,B为KMnO4,C中盛有KI淀粉溶液,旋开E后,C中的现象是??;继续通气体于C中,足够长的时间后,发现C中溶液的颜色消失,这是因为在溶液中I2能被Cl2氧化为HIO3(碘酸为强酸),写出该反应的离子反应方程式?。
(4)若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,旋开E,足够长的时间后,C中的现象是?,C中发生反应的离子方程式为?。
参考答案:(9分)⑴防倒吸(1分)
⑵2H2S + O2 ="=" 2S ↓+ 2 H2O? (2分)
⑶有气泡出现,同时溶液由无色变成蓝色(1分);6H2O +I2 +5Cl2===2IO3- + 10Cl- +12H+? (2分)
⑷有白色沉淀生成(1分)? Al3++3NH3.H2O ="==" Al(OH)3↓+ 3NH4+ (2分)
本题解析:略
本题难度:一般
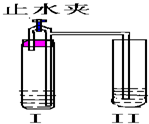
5、选择题 如图所示装置进行实验(图中铁架台等仪器均已略去).在I中加入试剂后,塞紧橡皮塞,立即打开止水夹,II中有气泡冒出;一段时间后关闭止水夹,II?中液面上升,溶液由无色变为浑浊.符合以上实验现象的I和II中应加入的试剂是( )
| A | B | C | D
I
CaCO3
稀盐酸
Na2CO3
稀硫酸
Zn
稀盐酸
Cu
稀硫酸
II
Ca(OH)2
NaOH
AgNO3
Ba(OH)2
|
A.A
B.B
C.C
D.D