微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
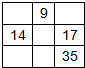
1、选择题 下列各表分别是元素周期表的一部分,表中的数字表示元素的原子序数,各表中数字所表示的元素在周期表中的位置与周期表的结构相符的是( )
A.
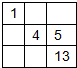
B.
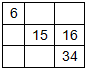
C.
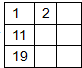
D.
参考答案:A、4和5,12和13间有10个空列为7个副族和1个Ⅷ族,故A错误;
B、中列为7、15、33,中行为14、15、16,符合位置关系,故B正确;
C、1号和11号元素之间相隔一个周期,第一列应为1、3、11、19,2号元素与1号元素之间相隔16列,故C错误;
D、14号元素与17号元素之间相隔2列,9号元素与17号、35号元素,处于同列,故D错误.
故选:B.
本题解析:
本题难度:一般
2、选择题 已知:短周期元素A和B可组成化合物AB3,当A的原子序数为a时,B的原子序数可能是( )
①a+4?②a-4?③a-8?④a+2?⑤a-6?⑥a+12.
A.①②③
B.①④⑤⑥
C.①②③④⑤
D.①②③④⑤⑥
参考答案:根据短周期元素A和B组成的化合物的化学式为AB3,可知A的化合价可能为+3价、+6价或-3价,B的化合价可能为-1价、+1价或-2价,A可能属于ⅢA族、ⅥA族、ⅤA族元素,
B可能属于ⅠA族、ⅥA族、VIIA族元素.则A可能为B、Al、S、N或P元素,原子序数分别为5、13、16、7、15,B可能为F、Cl、O、S或H元素,原子序数分别为9、17、8、16、1,
可能的化合物有BF3、BCl3、AlF3、AlCl3、SO3、NH3、NF3、PCl3等;根据这几种元素的原子序数可知当A的原子序数为a时,B的原子序数可能是:a+4、a+12、a-4、a-8、a-6、a+2,
即①a+4?②a-4?③a-8?④a+2?⑤a-6?⑥a+12这六种情况都存在,
故选:D.
本题解析:
本题难度:一般
3、推断题 有A、B、C、D、E五种元素,原子序数依次增大,位于不同的三个短周期,其中B与D为同一主族元素,它们可形成化合物DB2、DB3,在同周期元素中,C的金属性最强,E的非金属性最强;请回答:
(1)写出A、E三种元素的名称:A____________,E_____________。
(2)A、B形成的原子个数比为1∶1的化合物的电子式为__________________,该化合物与DB2化合生成一种强酸的化学方程式为:__________________________。
(3)已知在一定条件下1mol DB2完全转化为气态DB3,放出98.3 kJ的热量。该反应的热化学方程式是
_____________________________,工业上进行这一反应的设备是_____________,反应的适宜条件为
________________________。
(4)用铂作电极电解由C、E形成化合物的饱和溶液时,检验阳极产物的实验方法为________________________________________;电解一段时间后,将阳极产物和阴极溶液混合,反应的离子方程式是
_____________________________。工业实际中常采用阳离子交换膜电解槽进行电解,若某一电极由碳钢网制成,则该电极为电解槽的___________(填“阴”或“阳”,下同)极,精制的由C、E形成的化合物的饱和溶液进入_________极室。
参考答案:(1)氢;氯
(2) ;H2O2+SO2=H2SO4
;H2O2+SO2=H2SO4
(3)2SO2(g)+O2(g)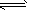 2SO3(g),ΔH=-196.6 kJ/mol;接触室;常压、400~500℃、催化剂;用湿润的
2SO3(g),ΔH=-196.6 kJ/mol;接触室;常压、400~500℃、催化剂;用湿润的
KI淀粉试纸接近阳极产物,试纸变蓝;Cl2+2OH-==Cl-+ClO-+H2O;阴;阳
本题解析:
本题难度:一般
4、填空题 下表为元素周期表的片段组合,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族
周期 | IA | | 0
1
①
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
②
③
④
3
⑤
⑥
⑦
⑧
|
(1)⑤、⑥、⑧相应离子半径由大到小的顺序:(离子符号表示)______.
(2)②、③、⑥的最高价氧化物的水化物酸性由强到弱的顺序是[填化学式]______.
(3)⑤、④、⑦元素可形成既含离子键又含极性键的一种可溶于水的化合物,其化学式为______.
(4)由②和④组成质量比为3:8的化合物结构式是______,微粒的空间构型______,形成______晶体,该物质与⑤的同周期相邻主族元素的单质反应的化学方程式为______.
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为______.
参考答案:根据元素在周期表中的分布,可以知道①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl.
(1)微粒电子层越多半径越大,所以Cl->Na+、Al3+,电子排布一样,核电荷数越多半径越小,则Na+>Al3+,故答案为:Cl->Na+>Al3+;
(2)同一周期元素的原子,从左到右最高价氧化物对应水化物的酸性逐渐增强,所以酸性:HNO3>H2CO3,氢氧化铝是两性氧化物,
故答案为:HNO3>H2CO3>Al(OH)3;
(3)O、Na、Si元素形成的硅酸钠时既含离子键又含极性键的一种可溶于水的化合物,化学式为:Na2SiO3 ,故答案为:Na2SiO3 ;
(4)由C与O组成质量比为3:8的化合物是二氧化碳,其结构式是C=O=C,属于直线型的分子晶体,金属镁在二氧化碳中燃烧的反应为:2Mg+CO2?点燃?.?2MgO+C,
故答案为:C=O=C;直线型;分子;2Mg+CO2?点燃?.?2MgO+C;
(5)Al单质与Na的最高价氧化物的水化物氢氧化钠反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑.
本题解析:
本题难度:简单
5、选择题 短周期元素W、X、Y、Z在元素周期表中的位置关系如图所示.下列说法正确的是( )
A.元素Y的最高价氧化物对应水化物的酸性比Z的强
B.元素Z位于元素周期表中的第3周期ⅦA族
C.原子半径的大小顺序:rY>rW>rX
D.元素X可能为氮或氧元素