| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ���ʵ�����������ѵ��2017�����°棩(��)
�ο��𰸣�D ���������a agij���庬������ΪP����bg�����庬�еķ�����Ϊ �����Ѷȣ�һ�� 3��ѡ���� ��0.5L?1mol/L?FeCl3��Һ��ˮϡ����1L��������Һ�������ӵ����ʵ���Ũ���� �ο��𰸣�C ���������������0.5L?1mol/L?FeCl3��Һ�������ӵ�Ũ��Ϊ3mol/L������ϡ�Ͷ��ɣ�ϡ��ǰ�������ӵ����ʵ������䣬�ݴ˼���ϡ�ͺ�������Һ�������ӵ�Ũ�ȣ� �����Ѷȣ�һ�� 4������� ��.���б�״���µ��������ʣ� |
�ο��𰸣�I C��D��A��B? C��B��D��A? C��A=D��B? D��A��B��C
II 11�U7? 11�U14 ?11�U7? 11�U7
�������������n=m/M=N/NA=V/Vm����֪
A.11.2LO2��n��O2��=11.2/22.4=0.5mol��m��O2��=0.5mol��32g/mol=16g��ԭ����Ϊ2��0.5NA=1NA��
��="M/V=32/22.4" g/L
B.6.8gNH3��n��NH3��=6.8/17=0.4mol��ԭ����Ϊ4��0.4NA=1.6NA����="17/22.4" g/L
C.1.204��1024CH4��n��CH4��=1.204��1024/6.02��1023=2mol��m��CH4��=2mol��16g/mol=32g����="16/22.4" g/L
D.0.5molCO2��m��CO2��=0.5mol��44g/mol=22g��ԭ����Ϊ3��0.5NA=1.5NA����="44/22.4" g /L
���ԣ������ɴ�С��˳��ΪC��D��A��B������������ԭ�����ɴ�С��˳����C��B��D��A��������ɴ�С��˳����C��A=D��B��������ܶ��ɴ�С��˳����D��A��B��C��
����CO��CO2��������Ϊmg����n��CO��="m/28" mol��n��CO2��="m/44" mol���������ʵ���֮��Ϊm/28��m/44=11��7����������ԭ�Ӹ�����Ϊ��11��7��2=11��14������̼Ԫ�ص������ȵ���̼Ԫ�ص����ʵ���֮�ȣ�Ϊ��11��7����ͬ�����µ������Ϊ�������ʵ���֮�ȣ�Ϊ11��7
���������⿼�����ʵ�������ؼ��㣬��Ŀ�ѶȲ���ע����㹫ʽ�����ã���ǿ�Ը�������⡣����n=m/M=N/NA=V/Vm��Ϸ��ӵĹ��ɺ����ʵ����������
�����Ѷȣ�һ��
5��ѡ���� ��a L����狀�����淋Ļ��Һ��Ϊ���ȷݣ�һ������b mol�ռ�պðѰ�ȫ���ϳ�����һ����BaCl2��Һ��Ӧǡ������c mol BaCl2����ԭ��Һ��NO3�������ʵ���Ũ����(����)��
A��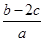 mol��L��1
mol��L��1
B��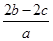 mol��L��1
mol��L��1
C��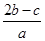 mol��L��1
mol��L��1
D��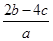 mol��L��1
mol��L��1
�ο��𰸣���D
�������������NH4+��OH��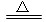 NH3����H2O��֪һ����Һ��n(NH4+)��b mol����(NH4)SO4��BaCl2===BaSO4����2NH4Cl��֪��һ����Һ��n(SO42��)��c mol����ԭ���Һ�У�n(NH4+)��2b mol��n(SO42��)��2c mol���ݵ���غ���ɿɵã�n(NO3��)��2n(SO42��)��n(NH4+)��n(NO3��)��(2b��4c)mol��c(NO3��)��
NH3����H2O��֪һ����Һ��n(NH4+)��b mol����(NH4)SO4��BaCl2===BaSO4����2NH4Cl��֪��һ����Һ��n(SO42��)��c mol����ԭ���Һ�У�n(NH4+)��2b mol��n(SO42��)��2c mol���ݵ���غ���ɿɵã�n(NO3��)��2n(SO42��)��n(NH4+)��n(NO3��)��(2b��4c)mol��c(NO3��)��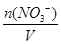 ��
��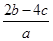 mol��L��1��
mol��L��1��
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ�㽲�⡶��ѧƽ�⡷.. | |
| �����Ŀ |