微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 将36 mL KBr和KI的混合溶液分为两等份。向其中一份通入足量的Cl2,完全反应后蒸发溶液至干,灼烧所得物质,得6.1 g固体残留物。测得另一份混合液中I-的浓度为0.086 mol・L-1。试判断并计算:
(1)固体残留物中含有什么物质?
(2)原溶液中含有KBr的质量为多少?
(3)反应完全时消耗Cl2的体积(标准状况)是多少?
参考答案:(1)KCl?(2)15.9 g?(3)0.92 L
本题解析:(1)固体残留物是KCl。因为通入足量的Cl2时,发生的反应有:2KI+Cl2 2KCl+I2,2KBr+Cl2
2KCl+I2,2KBr+Cl2 2KCl+Br2。在蒸干并灼烧的过程中,I2会升华,Br2会挥发,H2O会汽化。
2KCl+Br2。在蒸干并灼烧的过程中,I2会升华,Br2会挥发,H2O会汽化。
(2)欲计算原溶液中KBr的含量,可通过已知混合溶液中I-的浓度,据反应首先计算由KI生成KCl的质量,再由残留物的总质量与KI生成KCl质量的差,进一步计算出在一份溶液中含KBr的质量。与此同时,也可求得通入Cl2的体积。
因c(KI)=c(I-)=0.086 mol・L-1,则在一份溶液中含KI物质的量即为0.086 mol・L-1×0.018 L=0.015 mol。
由2KI? ~? Cl2?~? 2KCl
2 mol? 22.4 L? 149 g
0.015 mol?x?y
解得:x=0.168? L,y=1.12 g
因在6.1 g固体残留物中KBr生成KCl的质量为6.1 g-1.12 g=4.98 g
由2KBr? ~? Cl2? ~? 2KCl
238 g? 22.4 L? 149 g
x′? y′? 4.98 g
解得:x′=7.95 g,y′=0.75 L
故原混合溶液中含KBr的质量为7.95 g×2=15.9 g。
(3)在一份混合溶液中消耗Cl2的体积(标准状况)为0.168 L+0.75 L=0.92 L。
本题难度:简单
2、计算题 使250 mL密度为1.1 g・cm-3、质量分数为 24.5%的硫酸跟铁屑充分反应。
(1)求此硫酸中H2SO4的物质的量浓度:
(2)求生成H2的体积(标准状况):
(3)将生成的硫酸亚铁配制成400 mL溶液,此溶液中硫酸亚铁的物质的量浓度是多少?
参考答案:(1)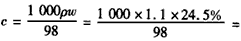 2.75 mol・L-1
2.75 mol・L-1
(2)n(H2SO4)=2.75 mol・L-1×0. 250 L≈ 0. 688 mol,
根据Fe+ H2SO4=FeSO4+H2↑
即知生成的氢气也为0. 688 mol,
在标准状况下的体积为0.688 mol×22.4L・mol-1=15.4L
(3)从(2)中可以求出硫酸亚铁也是0.688 mol,则

本题解析:
本题难度:一般
3、选择题 在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
A.2 mol・L-1
B.2.5 mol・L-1
C.5 mol・L-1
D.7.5 mol・L-1
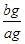 ×P=
×P=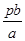 。所以bg该气体的物质的量为
。所以bg该气体的物质的量为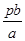 ÷NA=
÷NA=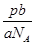 mol,故标准状况下,bg该气体的体积为
mol,故标准状况下,bg该气体的体积为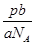 mol×22.4L/mol=
mol×22.4L/mol= L,答案选D。
L,答案选D。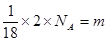 ,解得NA=9m,答案选B。
,解得NA=9m,答案选B。