微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液:
(1)求所得盐酸的物质的量浓度?
(2)若将此溶液再稀释成1L溶液,求稀释后盐酸的物质的量浓度?
(3)将(2)的溶液取出250mL与足量的Zn反应可以产生多少体积的H2(在标准状况下)?
参考答案:(1)4 mol・L-1?(3分)?(2)1?mol・L-1?(2分)?(3)2.8 L(3分)
本题解析:略
本题难度:简单
2、填空题 (8分)
① 44.8L某气体在标准状况下的质量为142g,该气体的摩尔质量为_________;
② N2在标准状况下的密度为__________g/L;
③在 mol AL2(SO4)3中含0.3molSO42―,其中含Al3+ 个。
参考答案:(每空2分,共8分)
①71g/mol ②1.25 ③0.1 0.2NA_或1.204X1023
本题解析:考查物质的量的简单计算
①M=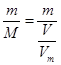 =
=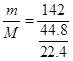 =71g/mol
=71g/mol
②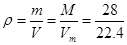 =1.25g/L
=1.25g/L
③由化学式可知道,在0.1mol AL2(SO4)3中含0.3molSO42―,其中含有Al3+0.2mol,即0.2NA个
本题难度:一般
3、选择题 某溶液大量含有的离子仅有: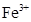 、
、 、
、 和M离子,且
和M离子,且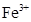 、
、 、
、 ?和M离子的物质的量之比为2:4:1:1,则M离子是( )
?和M离子的物质的量之比为2:4:1:1,则M离子是( )
A.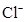
B.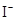
C.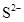
D.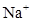
参考答案:A
本题解析:溶液为中性,阳离子所带正电荷总数与阴离子所带负电荷总数相等,设M离子的电荷为n,则:2×3―4×2+3×1+n=0,求出n=―1,因为I?能与Fe3+发生氧化还原反应,不能共存,所以只有A型Cl?符合题意。
本题难度:一般
4、简答题 实验室配制500ml2mol?L-1的H2SO4溶液
(1)所需仪器应该有容量瓶、玻璃棒、量筒、______、______.
(2)容量瓶在使用前,首先应检查______.
(3)此实验中,玻璃棒的两个作用分别是______、______.
(4)配制时,要用量筒量取密度为1.84g/cm3,质量分数为98%的浓硫酸______ml.
(5)若配好摇匀后,发现容量瓶中的液面略低于刻度线,问是否应该补充蒸馏水______(填“应该”或“不应该”);若所用的容量瓶中事先有少量的蒸馏水,则对实验结果有无影响______.(填“有影响”或“无影响”)
参考答案:(1)实验室配制500ml 2mol?L-1的H2SO4溶液,配制顺序是:计算→量取→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,需要的仪器有量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,
故答案为:胶头滴管; 烧杯.
(2)容量瓶有瓶塞,容量瓶在使用前,首先应检查容量瓶是否漏水,
故答案为:检验容量瓶是否漏水;
(3)在稀释浓硫酸时,使用玻璃棒进行搅拌,加速溶解过程;在转移溶液时,使用玻璃棒进行引流,避免液体流到容量瓶以外,
故答案为:搅拌; 引流;
(4)密度为1.84g/cm3,质量分数为98%的浓硫酸浓度为:1000×1.84×98%98mol/L=18.4mol/L,
500ml 2mol?L-1的H2SO4溶液中需要硫酸的物质的量为:2mol?L-1×0.5L=1mol,需要浓硫酸的体积为:1mol18.4mol/L=0.0543L=54.3mL,
故答案为:54.3ml;
(5)配好摇匀后,发现容量瓶中的液面略低于刻度线,由于刻度线上面含有部分溶液没有流下来,不需要加入蒸馏水;若配制前容量瓶中有蒸馏水,由于定容时需要加入蒸馏水,所以不影响配制结果,
故答案为:不应该; 无影响.
本题解析:
本题难度:一般
5、填空题 在9.5克某二 价金属的氯化物中含有0.2摩Cl-,此氯化物的摩尔质量为_______________,该金属元素的相对原子质量为_________________。
价金属的氯化物中含有0.2摩Cl-,此氯化物的摩尔质量为_______________,该金属元素的相对原子质量为_________________。
参考答案:___95g・mol-1___________, ___24_____
本题解析:略
本题难度:简单