| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ����ʵ�������Ƶ����ǿ����ϰ��2017�����°棩(ʮ)
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1~2cm�� ��4�������������������������ҺŨ�Ƚ��к�Ӱ�죨�ƫ�ߡ�����ƫ�͡�����Ӱ�족������û�н���A����______________��������ʱ���ӿ̶���_______________�� �ο��𰸣���1�� 14.3?��2���٢ڢۢܢޣ�? 250mL����ƿ�������� �����������1������250mL 0.2 mol��L��1��̼������Һ��Ҫn(Na2CO3)=0.05mol��������Ҫ��ȡNa2CO3?10H2O 14.3g�� �����Ѷȣ�һ�� 2��ѡ���� ��NA��ʾ�����ӵ�����������˵������ȷ���� |
�ο��𰸣�C
�����������״̬��H2OΪҺ̬�������ø������µ�����Ħ���������A�����1L1mol/L��CaCl2��Һ�к�Cl��Ϊ2mol����ĿΪ2NA����B�����25�桢1��01��105Pa�������µ�����Ħ���������22��4L/mol����2��24L H2�к��еķ�����С��0��1NA����C����ȷ����״���£�2��24 LCl2���ɵ���ˮ��Cl2����һ������ˮ��Ӧ����Cl2������ĿӦС��0��1NA����D�����
���㣺�����ӵ�����Ӧ�á�
�����Ѷȣ�һ��
3��ѡ���� �ԡ����ʵ�����Ϊ���ĵļ����ǻ�ѧ����Ļ����������롰���ʵ�������صļ�����ȷ�ģ�?��
A������CO��CO2��O3�������壬���Ƿֱ���1molO����������������ʵ���֮��Ϊ 3��2��1
B��5.6g CO ��22.4L CO2�к��е�̼ԭ����һ�����
C����״���£�11.2 L X������ӵ�����Ϊ16 g����X�����Ħ��������32
D��n g Cl2����m��Clԭ�ӣ����ӵ�����NA����ֵ�ɱ�ʾΪ 35.5m/n
�ο��𰸣�D
���������A ������1molO����������������ʵ����ֱ���1mol��1�M2mol��1�M3mol�����ǵı�ֵ��6��3��2 ����B������Ե����ʵ����������ʵ�����ȣ���̼ԭ����һ����ȡ�����CĦ������ȱ��λ������D ��ȷ��
�����Ѷȣ�һ��
4��ѡ���� ����״���µ�aLHCl��g������1000gˮ�У��õ��������ܶ�Ϊbg?/mL�������������ʵ���Ũ����
A.mo1?L-1����������������������������
B.mol?L-1
C.mol?L-1������������
D.mol?L-1
�ο��𰸣�D
�������������������n= �������ʵ����������ܼ������ʵ�������������Һ������������Һ���������ܶȿɼ�����Һ��������������c=
�������ʵ����������ܼ������ʵ�������������Һ������������Һ���������ܶȿɼ�����Һ��������������c= ������������ʵ���Ũ�ȣ�
������������ʵ���Ũ�ȣ�
��𣺱�״���µ�aLHCl��g����
n��HCl��=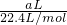 =
=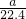 mol��
mol��
��Һ������Ϊ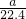 mol��36.5g/mol+1000g��
mol��36.5g/mol+1000g��
��Һ�����Ϊ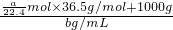 ��10-3L��
��10-3L��
��c= ��֪��
��֪��
c=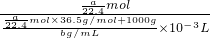 =
=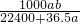 mol/L��
mol/L��
��ѡD��
���������⿼�����ʵ���Ũ�ȵļ��㣬��ȷ��Һ��������������ܶȵĹ�ϵ�����ʵ���Ũ�ȵļ��㹫ʽ���ɽ���ѶȲ���
�����Ѷȣ���
5��ѡ���� ����״���µ�V?L?HCl����������1000gˮ�У��õ��������ܶ�Ϊ��g/cm3�������������ʵ���Ũ��Ϊ��������
A��
| 1000V�� 22400+36.5V |
| V�� 22400 |
| V�� 22400+36.5V |
| V 22.4 |
�ο��𰸣�����״���µ�V?L?HCl�����������ʵ���ΪVL22.4L/mol=V22.4mol��
�Ȼ��������ΪV22.4mol��36.5g/mol=36.5V22.4g��
������Һ����Ϊ1000g+36.5V22.4g=��1000+36.5V22.4��g��
������Һ�����Ϊ(1000+36.5V22.4)g��g/ml=22400+36.5V22.4��ml=22400+36.5V22.4�ѡ�10-3L��
������ҺŨ��ΪV22.4mol22400+36.5V22.4�ѡ�10-3L=1000V��22400+36.5Vmol/L��
��ѡ��A��
���������
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ�㽲�⡶���仯��.. | |
| �����Ŀ |