微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应属于吸热反应的是
A.中和反应
B.锌与稀硫酸反应
C.炭燃烧生成CO
D.炭与高温水蒸汽反应
参考答案:D
本题解析:试题分析:理清常见放热反应:①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属与酸的置换反应;⑤铝热反应等;常见吸热反应:①大多数分解反应;②盐的水解;③Ba(OH)2・8H2O与NH4Cl反应;④碳与水蒸气、C与CO2的反应。选D
考点:考查常见的放热反应和吸热反应。
本题难度:困难
2、填空题 (12分:除注明分数的小题之外,其余为1分)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是________(用字母代号填)。
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是______nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:___________________________________。
某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是______________(2分),在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05 g.溶液中c(Cl-)= mol/L.
(4)若要验证该溶液中含有Fe2+,正确的实验方法是 。
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+。
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+。
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(5)欲从废水中回收铜,并重新获得FeCl3溶液设计实验方案如下:

A请写出上述实验中加入或生成的有关物质的化学式:
①_____________②____________③___________④____________
B请写出通入⑥的化学方程式__________________________________
参考答案:(1)C (1分);(2)1~100 (1分) ;(3)2Fe3++Cu===2Fe2++Cu2+ (1分);
Fe3+、Fe2+、Cu2+;(2分,每少一个扣一分,扣完为止。) 6.0 (1分)
(4)B (1分) (5)A ①Fe ②FeCl2 ③Fe Cu(少一个不得分) ④HCl (各1分)
B 2FeCl2+Cl2=2FeCl3 (1分)
本题解析:(1)因元素的化合价处于中间价态时,既能升高,又能降低,既有氧化性又有还原性,只有C中铁为+2价,符合条件;(2)透明的红褐色液体是胶体,胶体的粒子直径1nm<d<100nm;(3)Fe3+能与铜反应得到Fe2+和Cu2+,离子方程式为: 2Fe3++Cu===2Fe2++Cu2+;由于滴入KSCN溶液呈红色,证明溶液中Fe3+有剩余,溶液中含有的金属阳离子是:Fe3+、Fe2+、Cu2+;43.05g沉淀是AgCl,其物质的量为0.3mol,溶液中c(Cl-)=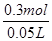 =6.0mol/L;(4)A、向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe3+,A错误;B、向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+;B正确;C、要证明原溶液中含有Fe2+,应该是先加入硫氰化钾,不变色,再加入氯水,若显示红色,证明有Fe2+;C错误;故选B;(5)A、制取的是FeCl3溶液,金属①是Fe;滤液②是FeCl2氯化亚铁溶液;加入的铁过量,滤渣③是Fe和Cu;制取FeCl3,溶解滤渣中的铁,应加入④是盐酸; B、⑥是将Fe2+氧化成Fe3+,反应方程式是:2FeCl2+Cl2=2FeCl3。
=6.0mol/L;(4)A、向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe3+,A错误;B、向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+;B正确;C、要证明原溶液中含有Fe2+,应该是先加入硫氰化钾,不变色,再加入氯水,若显示红色,证明有Fe2+;C错误;故选B;(5)A、制取的是FeCl3溶液,金属①是Fe;滤液②是FeCl2氯化亚铁溶液;加入的铁过量,滤渣③是Fe和Cu;制取FeCl3,溶解滤渣中的铁,应加入④是盐酸; B、⑥是将Fe2+氧化成Fe3+,反应方程式是:2FeCl2+Cl2=2FeCl3。
考点:考查铁及铁的化合物的性质、胶体的性质。
本题难度:一般
3、选择题 在含有酚酞的0.1mol/L氨水中加少量的NH4Cl晶体,则溶液颜色
A.变蓝色
B.变深
C.变浅
D.不变
参考答案:C
本题解析:试题分析:氨水中存在平衡:NH3+H2O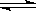 NH3・H2O
NH3・H2O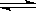 NH4++OH-,加少量氯化铵晶体,铵根离子浓度增大,平衡向左移动,氢氧根离子浓度减少,溶液颜色变浅。
NH4++OH-,加少量氯化铵晶体,铵根离子浓度增大,平衡向左移动,氢氧根离子浓度减少,溶液颜色变浅。
考点:弱电解质的电离平衡
点评:勒沙特列原理同样适用于弱电解质电离平衡。
本题难度:简单
4、选择题 ClO2是一种高效安全的杀菌消毒剂,还可用于除去水中的CN
参考答案:
本题解析:
本题难度:一般
5、选择题 蛋白质在胃蛋白酶和胰蛋白酶的作用下变成氨基酸的反应属于
A.消去反应
B.水解反应
C.取代反应
D.聚合反应
参考答案:B
本题解析:试题分析:蛋白质在胃蛋白酶和胰蛋白酶的作用下变成氨基酸的反应属于水解反应,故选B。
考点:蛋白质的水解
点评:蛋白质在酸、碱或酶的作用下发生水解反应,经过多肽,最终后会得到多种α-氨基酸。
本题难度:简单