��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ѧ����ѡ��2����ѧ�뼼������15�֣�̼�����;�㷺���������մɡ�ҩ�������Ҳ�dz��õ�����ӵ�ص�ԭ�ϡ���ҵ����﮻�ʯ��Li2O��Al2O3��4SiO2��������Ca��MgԪ�أ�Ϊԭ������̼��ﮡ��䲿�ֹ����������£�?
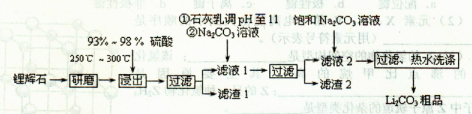
��֪����Li2O��Al2O3��4SiO2+H2SO4��Ũ��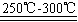 Li2SO4+Al2O3��H2O��
Li2SO4+Al2O3��H2O��
��ijЩ���ʵ��ܽ�ȣ�S�����±���ʾ��
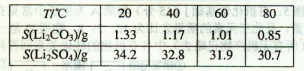
��1��������1�з����Al2O3�IJ�����������ͼ��ʾ�����ű�ʾ������Լ��������ʾ���õ������ʡ�
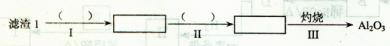
����I�з�Ӧ�����ӷ���ʽ��?�������Ӧͨ��һ�������Լ�Ϊ?������II��Ӧ��֮����Ҫ�IJ�����?��
��2����֪����2����Ҫ�ɷ���Mg��OH��2��CaCO3������Һl�м���ʯ����������ǣ������ӷ���ʽ��ʾ��?��
��3������Һ2�м��뱥��Na2CO3��Һ�����˺��á���ˮϴ�ӡ���ԭ����?��
��4����ҵ�ϣ���Li2CO3�ֲ�Ʒ�Ʊ��ɸߴ�Li2CO3�IJ��ֹ������£�
a����Li2CO3�������������۵�����Һ��LiOH��Һ������Һ������������ѡ����Ĥ�������ö��Ե缫��⡣
b��������LiOH��Һ�м���� ��NH4HCO3��Һ�����ˡ���ɵøߴ�Li2CO3��
��a�У������ĵ缫��Ӧʽ��?��
��b�У�����Li2CO3��Ӧ�Ļ�ѧ����ʽ��?��
�ο��𰸣���1��Al2O3 +6H+ = 2Al3++3H2O��2�֣� NH3 ��2�֣� ���ˣ�2�֣�
��2��Ca(OH)2 + 2H+ = Ca2+ + 2H2O��1.5�֣�Ca(OH)2(s) + Mg2+ Mg(OH)2(s) +Ca2+��1.5�֣�
Mg(OH)2(s) +Ca2+��1.5�֣�
��3�� Li2CO3���ܽ�����¶����߶���С����ˮϴ�ӿɼ���Li2CO3����ʧ��2�֣�
��4���� 2Cl���D2e����Cl2����2�֣��� 2LiOH+2NH4HCO3��Li2CO3��+(NH4)2CO3+2H2O��2�֣�
������������⿼��Ԫ�ػ���������ʼ���ѧ�뼼���й�֪ʶ����1�����ὫAl2O3��Һ�⣬��ͨ�백��ת��ΪAl(OH)3���������˺����յõ�Al2O3������I�з�Ӧ�����ӷ���ʽ��Al2O3 +6H+ = 2Al3++3H2O��ͨ�������������NH3������II��Ӧ��֮����Ҫ�IJ����ǹ��ˡ���2������Һl�м���ʯ����������ǵ�����Һ��pHֵ����Mg2+ת��Ϊ���ܵ�Mg(OH)2��������Ӧ�����ӷ���ʽΪCa(OH)2 + 2H+ = Ca2+ + 2H2O��Ca(OH)2(s) + Mg2+ Mg(OH)2(s) +Ca2+����3���ӱ������ݿ�֪��Li2CO3���ܽ�����¶����߶���С��������ˮϴ���ܼ���Li2CO3����ʧ����֤���ߵIJ��ʡ���4����Li2CO3�������ᣬ�õ�LiCl��Һ�����ʱ������Cl-ʧ���ӱ����������缫��ӦʽΪ2Cl���D2e����Cl2����Li+ͨ����Ĥ�������������õ�LiOH��Һ���ڵ���õ�LiOH��Һ������NH4HCO3����LiOHת��ΪLi2CO3����Ӧ�Ļ�ѧ����ʽ��2LiOH+2NH4HCO3��Li2CO3��+(NH4)2CO3+2H2O��
Mg(OH)2(s) +Ca2+����3���ӱ������ݿ�֪��Li2CO3���ܽ�����¶����߶���С��������ˮϴ���ܼ���Li2CO3����ʧ����֤���ߵIJ��ʡ���4����Li2CO3�������ᣬ�õ�LiCl��Һ�����ʱ������Cl-ʧ���ӱ����������缫��ӦʽΪ2Cl���D2e����Cl2����Li+ͨ����Ĥ�������������õ�LiOH��Һ���ڵ���õ�LiOH��Һ������NH4HCO3����LiOHת��ΪLi2CO3����Ӧ�Ļ�ѧ����ʽ��2LiOH+2NH4HCO3��Li2CO3��+(NH4)2CO3+2H2O��
�����Ѷȣ���
2������� ����������һ����;ʮ�ֹ㷺�Ļ���ԭ�ϡ���ҵ����Ҫͨ������Ȼ��Ʊ�����Һ�ķ�������������ƣ��ҹ����ȼҵ������������ӽ���Ĥ���ۡ�
(1)���ӽ���Ĥ����һ����ý���������������ԭ����__________________________________��
����һ����̼�����Ƴɡ������ӽ���Ĥ�ѵ��۸��������Һ������ң���������____________________________________��
(2)Ϊʹ����Ȼ��Ƶ����ʼӿ죬���д�ʩ���е���__________��
a����������̼���������
b����߱����Ȼ�����Һ���¶�
c���Ӵ�������������ľ���
d����ߵ��ʱ��Դ��ѹ
(3)�����ij���ӽ���Ĥ���۵Ģٵ��ʱ��ѹ����ԭ����2�����ڵ��ʱ�ĵ���ǿ������ԭ����2�����۵��ʱ�¶ȴ�30 ����ߵ�60 �棬��������һ����ﵽԭ����2������________________��
�ο��𰸣�(1)����������Cl2����ʴ�ѡ����ܷ�ֹH2��Cl2��ϱ�ը�����ܱ���Cl2��NaOH��Ӧ
(2)abd��(3)��
������������ʱH����Cl���ֱ������������ϵ�ʧ���ӣ�����H2��Cl2���������ϱ���ѡ���ױ�Cl2��ʴ�IJ��ϣ��������������¶ȡ������ѹ�������ڼӿ���ʳ��ˮ�����ʡ������ʱ��ѹ����ԭ����2�������صĵ�����ܷ����仯�����ʱ�ĵ���ǿ�Ȳ�һ������ԭ����2�������ʱ�¶ȴ�30 ����ߵ�60 �棬���ص�������������ͣ�������һ��ǡ�ý���Ϊԭ����һ�룻�����ʱ�ĵ���ǿ������ԭ����2������λʱ����������·�ĵ���ǡ��Ϊԭ����2����������Ӧ�����ʵ���Ҳǡ��Ϊԭ����2��������Ӧ����Ϊԭ����2����
�����Ѷȣ�һ��
3��ѡ���� ���ά��һ���ִ�����ͨѶ���ߣ�������ά����Ҫԭ����
[? ]
A��CaCO3
B��SiO2
C��CaO
D��Na2CO3
�ο��𰸣�B
���������
�����Ѷȣ���
4������� ��12�֣�I����Դ�������������ᷢչ�Ļ��������������������Դ��? ��?������Ȼ������һ��Դ��ɹ�����? ��?�����������ǿ����������ɫ��Դ����֪��������ֵ��143kJ��g-1����ֵָ������һ�������µ�λ������������ȫȼ�����ų�������������ת��ΪҺ̬ˮ������д������ȼ�յ��Ȼ�ѧ����ʽ? ��?��
������������һ���Է���������ԭ��Ӧ������Ƴ�ԭ��أ��������·�Ӧ��
2FeCl3 + Cu = 2FeCl2 + CuCl2
���������Ƴ�ԭ��أ���д���������ϼ������缫��Ӧʽ��
�������ϣ�? ��?�������缫��Ӧʽ��? ��?��
III����ҵ���õ�������������ķ�����ȡ��������
��1����д����ҵ�õ��������������ȡ���Ļ�ѧ����ʽ��? ��?��
��2����ұ��2.7 t ������Ҫת�Ƶ��ӵ����ʵ���Ϊ? ��?mol��
�ο��𰸣�(4��) �ڡ��١��ܡ���(ÿ��1��)
�����������
�����Ѷȣ�һ��
5��ѡ���� ����ұ�������У��ɽ��������еĽ���Ԫ�ػ�ԭΪ�������ʵ���
A������Al2O3
B������CaCO3
C���������NaCl
D���Ȼ��������۸��¹���
�ο��𰸣�C
���������A�����ǻ��õĽ�����ֻ��ͨ����ⷨұ������˵�����ڵ����������Ի�ý�������A����ȷ��B�����ǻ��õĽ�����ֻ��ͨ����ⷨұ��������̼��Ʒֽ����������ƺ�CO2��B����ȷ��C�����ǻ��õĽ�����ֻ��ͨ����ⷨұ������˵�����ڵ��Ȼ��ƿ��Եõ��ƣ�C��ȷ��D�����ǻ��õĽ������һ�����ǿ���������������Ȼ��Ʋ����ܷ������ȷ�Ӧ��D����ȷ����ѡC��
�����Ѷȣ�һ��