微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关无机非金属材料的说法中,不正确的是
[? ]
A、高纯硅可用于制造半导体材料
B、SiO2?制成玻璃纤维,由于导电能力强而被用于制造光缆
C、玻璃、水泥、陶瓷其成分均含有硅酸盐
D、Si3N4是一种新型无机非金属材料,可用于制造发动机
参考答案:B
本题解析:
本题难度:简单
2、填空题 硫酸铅(PbSO4)广泛应用于制造蓄电池、白色颜料等。利用锌冶炼过程中的铅浮渣生产PbSO4的流程如下:
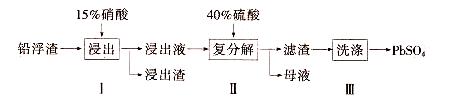
已知铅浮渣的主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。25℃时,Ksp(CaSO4)=4.9x10-5,Ksp(PbSO4)=1.6xl0-8。
(1)已知步骤I有NO气体产生,浸出液中含量最多的阳离子是Pb2+。分别写出PbO、Pb参加反应的化学方程式?。
(2)步骤I需控制硝酸的用量并使Pb稍有剩佘,目的是?。
(3)母液可循环利用于步骤I,其溶质主要是?(填一种物质化学式),若母液中残留的SO42-过多,循环利用时可能出现的问题是?。
(4)产品PbSO4还需用Pb(NO3)2溶液多次洗涤,目的是除去?。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为?。
参考答案:
(1)PbO+2HNO3=Pb(NO3)2+H2O? (2分)?
3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O? (3分)
(2)防止Ag被溶解进入溶液? (或使Ag留在浸出渣中)(2分)
(3)HNO3?(2分)?浸出时部分铅离子生成PbSO4随浸出渣排出,降低PbSO4的产率?(2分)
(4)CaSO4杂质? (2分)
(5))PbSO4+2e-=Pb+SO42-? (2分)
本题解析:(1)写方程式时注意,Pb的二价稳定,Pb与HNO3发生氧化还原反应生成NO。
(2)Pb过量可将溶解的Ag置换出来,防止Ag+进入溶液。
(3)母液循环利用,第一步需要加入HNO3,因此母液中溶质主要是HNO3。根据题意PbSO4难溶于水,若硫酸根过多,则会使部分Pb生成PbSO4随浸出渣排出,产率降低。
(4)产品中含有的主要杂质是CaSO4,根据沉淀转化原理,加入Pb(NO3)2溶液可使CaSO4转化为Ca(NO3)2,除去杂质。
(5)根据铅蓄电池原理,负极的Pb充电时接电源负极,成为电解池的阴极,因此阴极的反应式为PbSO4+2e-=Pb+SO42-。
本题难度:困难
3、填空题 (10分)某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如下图所示。

已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
离子
| 开始沉淀时的pH
| 完全沉淀时的pH
|
Fe2+
| 6.34
| 9.7
|
Fe3+
| 1.48
| 3.2
|
Zn2+
| 6.2
| 8.0
|
请回答下列问题:
⑴氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)??Ksp(ZnS)(选填“>”“<”或“=”)(Ksp 沉淀离子浓度积)。
⑵物质A可使用下列物质中的?。
A.KMnO4? B.O2? C.H2O2? D.Cl2
⑶除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在?范围之间。
⑷物质B可直接用作氮肥,则B的化学式是?。
参考答案:⑴<? ⑵BC? ⑶3.2~6.2? ⑷(NH4)2SO4
本题解析:(1)在H2SO4的作用下ZnS可以溶解而CuS不溶,说明硫化铜更难溶,因此溶度积常数小于硫化锌的。
(2)A是氧化溶液中的亚铁离子的,由于不能引入杂质,所以应该选择臭氧和双氧水,答案选BC。
(3)关键表中数据可知,铁离子完全沉淀的pH是3.2,而锌离子开始沉淀的pH是6.2,所以pH的范围是3.2~6.2。
(4)物质B可直接用作氮肥,则B是铵盐,因此是(NH4)2SO4。
本题难度:一般
4、选择题 下列所列各物质的用途中,不正确的是( )
A.分子筛:吸附剂、催化剂
B.硅胶:干燥剂、吸附剂、催化剂载体
C.碳化硅:砂纸、砂轮
D.硅酸:粘合剂、耐火材料
参考答案:D
本题解析:
本题难度:一般
5、选择题 下列关于硅酸盐材料的说法错误的是( )
A.生活中常见的硅酸盐材料有玻璃、水泥、陶瓷
B.普通玻璃的主要成分是SiO2
C.陶瓷的主要原料是黏土
D.硅酸盐水泥以石灰石和黏土为主要原料
参考答案:B
本题解析:
本题难度:简单