��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ�С�H1=��393.5 kJ?mol-1����H2=��395.4 kJ?mol-1���й�˵����ȷ����

A�����ʯ��ʯī�ȶ���ǿ
B��ʯī��Ϊ���ʯ�������仯
C��ʯī��Ϊ���ʯ�Ƿ��ȷ�Ӧ
D��1 molʯī���ܼ��ܱ�1 mol���ʯ���ܼ��ܴ�1.9 kJ
�ο��𰸣�D
�������������ͼ���֪�����ʯ����������ʯī������������ʯī��Ϊ���ʯ�����ȷ�Ӧ��ʯī�Ƚ��ʯ�ȶ���A��C����ȷ��ͬ��������֮���ת���ǻ�ѧ�仯��B����ȷ��1 molʯī���ܼ��ܱ�1 mol���ʯ���ܼ��ܴ�395.4kJ��393.5kJ��1.9 kJ��D��ȷ����ѡD��
�������������е��Ѷȵ����⣬���������ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������Ĺؼ�����ȷ��Ӧ���뷴Ӧ����������������Ĺ�ϵ���Լ������ȶ����������Ĺ�ϵ������������ѧ����������������Ӧ��������
�����Ѷȣ���
2������� ͬ���������ת���ķ�Ӧ���൱С����ת�����ʽ�������ʱ���ܲ���ȫ���ⶨ��Ӧ�Ⱥ����ѡ����ڿɸ��ݸ�˹����ġ����ܻ�ѧ������һ����ɻ��Ƿּ�����ɣ�����ܹ��̵���ЧӦ����ͬ�ġ��۵������㷴Ӧ�ȡ���֪��
P4(s������)+5O2��g��====P4O10��s��
��H="-2" 983.2 kJ��mol-1��
P(s������)+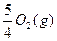 ====
====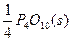 ?
?
��H="-738.5" kJ��mol-1��
�����ת��Ϊ�����Ȼ�ѧ����ʽΪ_________����ͬ״���£�����״̬�ϵ͵���_________�������ȶ��ԱȺ���_________����ߡ��͡�����
�ο��𰸣�P4��s�����ף�====4P��s�����ף�
��H="-29.2" kJ��mol-1?����?��
�����������-4���ڵ�P4(s,����)=4P��s�����ף�? ��H=��H1-4��H2="-2" 983.2 kJ��mol-1-4��(-738.5 kJ��mol-1)="-29.2" kJ��mol-1����P4��s�����ף�====4P��s�����ף�? ��H="-29.2" kJ��mol-1������ת��Ϊ�����Ƿ��ȷ�Ӧ���ȶ��ԱȺ��ͣ�����Խ��Խ�ȶ�����
�����Ѷȣ���
3��ѡ���� �����Ȼ�ѧ���̣���101kpaʱ����S��s��+O2��g��=SO2��g����H=-297.23kJ/mol����������˵���в���ȷ���ǣ�������
A��S��ȼ����Ϊ297.23KJ/mol
B��S��s��+O2��g��=SO2��g���ų�����������297.23kJ
C��S��s��+O2��g��=SO2��g���ų�������С��297.23kJ
D���γ�1mol��������Ļ�ѧ�����ͷŵ����������ڶ���1molS��1molO2�Ļ�ѧ�������յ�������
�ο��𰸣�A����������Ϊ�ȶ������S��ȼ����Ϊ297.23?kJ/mol����A��ȷ��
B���ɸ�˹���ɿ�֪��S��g��+O2��g���TSO2��g����H��-297.23kJ/mol����ų�����������297.23?kJ����B����
C���ɸ�˹���ɿ�֪��S��g��+O2��g���TSO2��g����H��-297.23kJ/mol����ų�����������297.23?kJ����C��ȷ��
D���÷�ӦΪ���ȷ�Ӧ�����γ�1?mol?SO2�Ļ�ѧ�����ͷŵ����������ڶ���1?mol?S��s����1?mol?O2��g���Ļ�ѧ�������յ�����������D��ȷ��
��ѡB��
���������
�����Ѷȣ���
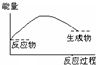
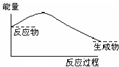
4��ѡ���� ��Ba��OH��2?8H2O������NH4Cl�����ϣ��ܱ�ʾ��Ӧ�����������仯��ʾ��ͼ�ǣ�������
A��
B��
C��

D��

�ο��𰸣�Ba��OH��2?8H2O������NH4Cl�����Ϸ����������ȷ�Ӧ�����Է�Ӧ��������С����������������Aѡ���з�Ӧ��������С����������������Bѡ���Dѡ��Ƿ�Ӧ��������������������������Cѡ�Ӧ������������������������ȣ���ѡA��
���������
�����Ѷȣ���
5��ѡ���� ��֪������������ȼ��ʱ������ɫ���棬�ڷ�Ӧ�����У��ƻ�1 mol�����Ļ�ѧ�����ĵ�����ΪQ1 kJ���ƻ�1 mol�����Ļ�ѧ�����ĵ�����ΪQ2kJ ���γ�1 mol�Ȼ����еĻ�ѧ�����ĵ�����ΪQ3kJ�����й�ϵʽ��ȷ���� ��?��
A��Q1 + Q2 > Q3
B��Q1 + Q2 > 2Q3
C��Q1 + Q2 < Q3
D��Q1+ Q2 < 2Q3
�ο��𰸣�D
���������1mol������1mol������ȫ��Ӧ����2molHClΪ���ȷ�Ӧ�����ƻ�1 mol�����Ļ�ѧ�����ĵ�����ΪQ1 kJ���ƻ�1 mol�����Ļ�ѧ�����ĵ�����ΪQ2kJ֮��С���γ�2 mol�Ȼ����еĻ�ѧ�����ĵ�����2Q3kJ����ѡD��
�����Ѷȣ�һ��