微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:?
物理性质
| 色态
| 挥发性
| 熔点
| 沸点
|
金黄色液体
| 易挥发
| -76℃
| 138℃
|
化学性质
| 300 ℃以上完全分解
|
S2Cl2+Cl2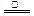 2SCl2 2SCl2
|
遇水反应生成SO2、S等产物
|
向熔融的硫中通以干燥、纯净的C12即可生成S2C12。下图是实验室制备S2Cl2的装置。
 ?
?
(1)仪器A的名称是?,导管F除导气外还起的作用是?;
(2)B中反应的离子方程式为?;
(3)开始实验,打开分液漏斗的活塞,发现浓盐酸流出少量后即难以下滴,经检查分
液漏斗活塞没有堵塞,你认为应采取的措施是?;
(4)装置C中的试剂是?;如果缺少D装置,则对实验的影响是(用化学方程式表示)?;
(5)如果在加热E时温度过高,对实验结果的影响是?;为了提高S2C12的纯度,关键的操作是控制好温度和?。
(6)设计装置H的目的是?;烧杯中发生反应的离子方程式
是?。
参考答案:(1)分液漏斗?冷凝?
(2)MnO2 + 4 H+ +2 C1- ="=" Mn2+ + C12↑+ 2H2O ?
(3)将玻璃塞上的凹槽与漏斗口颈上的小孔对准(或拔去玻璃塞)
(4)饱和食盐水? 2S2Cl2 +2H2O=SO2+3S+4HCl?
(5)产率降低?控制浓盐酸的滴速不要过快?
(6)吸收尾气,防止污染? C12+2OH-=Cl-+ClO-+ H2O
本题解析:略
本题难度:简单
2、填空题 硅在地壳中的含量较高,硅及其化合物的开发由来已久,在现代生活中有广泛应用。回答下列问题:
(1)陶瓷、水泥和玻璃是常用的传统的无机非金属材料,其中生产普通玻璃的主要原料有?。
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:

①工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃除生成粗硅外,也可以生产碳化硅,则在电弧炉内可能发生的反应的化学方程式为?。
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应方程式?。
(3)有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和?;SiHCl3极易水解,其完全水解的产物为?。
物质
| Si
| SiCl4
| SiHCl3
| SiH2Cl2
| SiH3Cl
| HCl
| SiH4
|
沸点/℃
| 2355
| 57.6
| 31.8
| 8.2
| -30.4
| -84.9
| -111.9
|
?
(4)还原炉中发生的化学反应为:?。
(5)氯碱工业可为上述工艺生产提供部分原料,这些原料是?。
参考答案:(1)石英砂、纯碱和石灰石(2分)
(2)①SiO2 + 2C Si + 2CO↑(2分)、SiO2 + 3C
Si + 2CO↑(2分)、SiO2 + 3C SiC + 2CO↑(2分)
SiC + 2CO↑(2分)
②Si + 3HCl SiHCl3 + H2(2分)
SiHCl3 + H2(2分)
(3)蒸馏(1分)? H4SiO4(或H2SiO3)、H2、HCl(2分,答不全,少一种扣一分,但有错不给分)
(4)SiHCl3 + H2 ?Si + 3HCl (2分)
?Si + 3HCl (2分)
(5)H2、HCl(2分)
本题解析:(1)生产普通玻璃的主要原料有石英砂、纯碱和石灰石
(2)①石英砂的主要成分是SiO2,与C可能的反应有:SiO2 + 2C Si + 2CO↑、SiO2 + 3C
Si + 2CO↑、SiO2 + 3C SiC + 2CO↑
SiC + 2CO↑
②粗硅生成SiHCl3的化学反应方程式为Si + 3HCl SiHCl3 + H2
SiHCl3 + H2
(3)硅的氯化物的熔点相差较大且互溶,所以采用蒸馏的方法可提纯SiHCl3,从元素的种类上分析SiHCl3完全水解的产物有H4SiO4(或H2SiO3)、H2、HCl
(4)还原炉中发生的反应是氢气还原SiHCl3,化学方程式为SiHCl3 + H2 ?Si + 3HCl
?Si + 3HCl
(5)氯碱工业的产品有H2、Cl2、NaOH,所以为上述工艺生产提供部分原料是H2、HCl
本题难度:困难
3、选择题 下列有关二氧化硅和硅酸盐的叙述中,正确的是
A.水晶和玛瑙的主要成分都是硅酸盐
B.水玻璃不与盐酸反应
C.陶瓷、玻璃、水泥是常用的三大类硅酸盐产品
D.纯净的二氧化硅是现代光学及光纤制品的基本原料
参考答案:CD
本题解析:水晶和玛瑙的主要成分都是二氧化硅,A不正确。水玻璃是硅酸钠的水溶液,和盐酸反应生成硅酸沉淀,B不正确。所以正确的答案是CD。
本题难度:一般
4、填空题 (6分)实验室中的Na2SiO3溶液长期放置,瓶底会出现白色沉淀,形成沉淀的离子方程式是?。取瓶中的上层清液滴入稀盐酸,既有气泡又有沉淀生成,其离子方程式为??,?。
参考答案:(6分)SiO32- + H2O +CO2= H2SiO3↓+ CO32-;(2分)
CO32- +2H+== H2O +CO2↑;(2分))? SiO32- +2H+==H2SiO3↓。(2分)
本题解析:碳酸的酸性强于硅酸的,所以硅酸钠能吸收空气中的CO2和水生成硅酸白色沉淀,反应的离子方程式是SiO32- + H2O +CO2= H2SiO3↓+ CO32-。在该反应中还有碳酸钠生成,所以。取瓶中的上层清液滴入稀盐酸,既有气泡又有沉淀生成,气体是CO2,白色沉淀是硅酸,反应的离子方程式分别是CO32- +2H+= H2O +CO2↑、SiO32- +2H+=H2SiO3↓。
点评:该题是基础性试题的考查,主要是检验学生对硅酸制备的了解掌握程度,以及离子方程式书写的掌握程度,有利于培养学生的规范答题能力和逻辑推理能力。
本题难度:一般
5、选择题 能证明硅酸的酸性比碳酸的酸性弱的实验事实是
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸沉淀
C.高温下SiO2与碳酸盐反应生成CO2
D.氯化氢通入碳酸钠溶液中放出气体,通入硅酸钠溶液中生成沉淀
参考答案:B
本题解析:依据较强的酸制取较弱的酸可知,B中CO2可以制取硅酸,这就说明硅酸的酸性弱于碳酸的酸性;A是溶解性和酸性强弱无关系;C中反应不是复分解反应,不能说明;D中只能说明硅酸和碳酸的酸性都弱于盐酸的,不正确,答案选B。
点评:本题是中等难度的试题,对学生的要求较高。该题的关键是理解“强制弱的原理”,然后结合具体问题、具体分析即可。
本题难度:简单