微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (5分).利用右图所示装置收集以下6种气体
(图中烧瓶的位置不得变化):
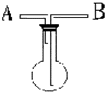
①NO?②Cl2③SO2 ④HCl ⑤NH3
⑴若烧瓶充满水,可收集的气体有?,这时气体由?口进入(填序号)
⑵若烧瓶是干燥的,则由A口进气,可收集的气体有?。
⑶若在烧瓶中装入浓硫酸进行气体干燥,这时气体由?口进入,则不可用此装置来干燥的气体有?。
参考答案:(1)①? A;?(2)⑤;(3)B?⑤
本题解析:(1)②③④⑤均可溶于水或极易溶于水,所以不能用排水法收集。NO不溶于水,可以通过排水法收集,因为必须从B口排出水,所以从A口进气。
(2)烧瓶是干燥的,由A口进气,说明空气从B口排出,因此气体的密度应小于空气的密度,所以是氨气。
(3)干燥气体时,进气口的导管必须插入到浓硫酸中,所以气体从B口进气。氨气是碱性气体,能和浓硫酸反应生成硫酸铵,所以不能干燥氨气。
本题难度:一般
2、实验题 (10分)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
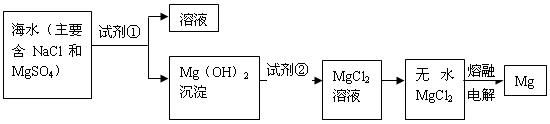
(1)为了使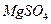 转化为
转化为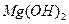 ,试剂①可以选用?,要使
,试剂①可以选用?,要使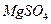 ?完全转化为沉淀,加入试剂①的量应?;
?完全转化为沉淀,加入试剂①的量应?;
(2)加入试剂①后,能够分离得到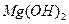 沉淀的方法是?;
沉淀的方法是?;
(3)试剂②可以选用?;
(4)无水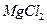 在熔融状态下,通电后会产生
在熔融状态下,通电后会产生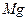 和
和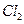 ,该反应的化学方程式为:
,该反应的化学方程式为:
?。
参考答案:(1)? Ca(OH)2,?过滤量;?(1)Ca(OH)2(或NaOH、KOH等)
(2)?过滤?;(3)盐酸?;
(4)? MgCl2(熔融) Mg + Cl2 ↑
Mg + Cl2 ↑
本题解析:略
本题难度:简单
3、实验题 (12分)硫酸亚铁铵[(NH4)2SO4・FeSO4・6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1?将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2?向处理过的铁屑中加入过量的3mol・L-1 H2SO4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3?向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有__________(填仪器编号)
①铁架台? ②燃烧匙? ③锥形瓶? ④广口瓶? ⑤研钵? ⑥玻璃棒? ⑦酒精灯
(2)在步骤2中趁热过滤,其原因是________________________________;
(3)在步骤3制的的硫酸亚铁铵晶体常含有Fe3+杂质。检验Fe3+的试剂可以用K4〔Fe(CN)6〕生成普鲁士蓝沉淀,有关的离子方程式是_________________________ _____。
(4)制得的晶体经过过滤后用无水乙醇洗涤而不用蒸馏水,理由是__________________;(任说两点)
(5)在25℃时,相同物质的量浓度的(NH4)2CO3、(NH4)2SO4、硫酸亚铁铵三种盐溶液a、b、c,其铵根离子浓度由小到大的排列顺序为_______________(用a、b、c回答)
参考答案:(1)②④⑤;(2)防止溶液冷却时,硫酸亚铁因析出而损失。
(3)K++Fe3++[Fe(CN)6]4-=KFe[Fe(CN)6]↓
(4)①硫酸亚铁铵晶体在乙醇中的溶解度小,可减小晶体在洗涤时应溶解而损失;②酒精易挥发,不会附着在晶体表面。(或:减少蒸馏水中的溶解氧对晶体的氧化)
(5)a<b<c
本题解析:(1)步骤I是除去油污,由于需要加热,所以②④⑤是不需要的。
(2)由于硫酸亚铁的溶解度随温度的降低而降低,所以趁热过滤的目的是防止溶液冷却时,硫酸亚铁因析出而损失。
(3)根据反应物和生成物可以得出方程式为K++Fe3++[Fe(CN)6]4-=KFe[Fe(CN)6]↓。
(4)由于硫酸亚铁铵晶体在乙醇中的溶解度小,可减小晶体在洗涤时应溶解而损失;其次酒精易挥发,不会附着在晶体表面。
(5)NH4+水解显酸性,CO32-水解显碱性,二者相互促进。Fe2+水解显酸性,和NH4+水解相互抑制,所以铵根离子浓度由小到大的排列顺序为a<b<c。
本题难度:一般
4、实验题 (8分)
用实 验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸。其具体实验步骤如下:
验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸。其具体实验步骤如下:
①取一支碱式滴定管(如图有两只滴定管,你选择哪一只?)?(填写对应字母),用少量标准NaOH溶液润洗2~3次水洗后的碱式滴定管,再加入标准的0.100mol/L的NaOH溶液并记录液面刻度读数;

②用酸式滴定管精确地放出25.00mL待测盐酸,置于用蒸馏水洗净的锥形瓶中。再加入酚酞试液2滴;
③滴定时,边滴边振荡,同时眼睛注视锥 形瓶内溶液颜色的变化,当锥形瓶内溶液由
形瓶内溶液颜色的变化,当锥形瓶内溶液由
?(填写颜色变化)且半分钟内不褪色时,即达到滴定终点;
④记录液面刻度读数。根据滴定管的两次读数得出消耗标准盐酸的体积,再重复测定两次,实验结果记录见下表:
实验次数
| 起始滴定管读数
| 终点滴定管读数
|
1
| 0.00mL
| 24.02mL
|
2
| 0.50mL
| 24.46mL
|
3
| 1.00mL
| 25.02mL
|
测得未知稀盐酸的物质的量浓度为?(保留小数点后3位)。
⑤如果滴定结束时俯视碱式滴定管刻度读数(其它操作均正确),则对滴定结果稀盐酸浓度的影响是?(填“偏高”、“偏低”或“无影响”)。
参考答案:① b?③无色→浅红色?④ 0.096mol/L?⑤偏低
本题解析:略
本题难度:一般
5、选择题 实验室在制备气体时,对某些气体来说,收集方法即可采用排水法,又可采用排空气法收集。下列气体中,能同时采用上述两种收集方法的是(?)
A.NH3
B.NO
C.NO2
D.H2
参考答案:D
本题解析:排水法收集气体,要求气体难溶于水,且不与水发生反应;能用向上排空气法收集,要求该气体密度比空气的大且不与空气反应;能用向下排空气法收集,要求该气体密度比空气的小且不与空气反应。
A项中的NH3 易溶于水,不能用排水法收集;密度比空气小,可采用向下排空气法收集,所以A不符合。
B项中的NO会与空气中的氧气反应,不能用排空气法收集;NO难溶于水,且不与水发生反应,可采用排水法收集。所以B不符合。
C项中的NO2?会与水发生反应,不能用排水法收集;不与空气反应且密度比空气大,可采用向上排空气法收集。所以C不符合。
D项中的H2难溶于水且不与水发生反应,不与空气反应且密度比空气小,可采用排水法和向下排空气法收集,所以D符合。故本题选D。
点评:本题考查收集气体的方法。可根据所学知识作答。题目难度不大。
本题难度:简单