微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列操作中,能使电离平衡H2O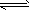 H++OH-,向右移动且溶液呈酸性的是
H++OH-,向右移动且溶液呈酸性的是
[? ]
A.向水中加入NaHSO4溶液
B.向水中加入Al2(SO4)3溶液
C.向水中加入NaOH溶液
D.将纯水加热到100℃
参考答案:B
本题解析:
本题难度:一般
2、选择题 常温下,某溶液中由水电离的c(H+)=1×10-13mol?L-1,该溶液可能是( )
①氯化铵水溶液②硝酸钠水溶液③硫酸水溶液④氢氧化钠水溶液.
A.①④
B.①②
C.②③
D.③④
参考答案:D
本题解析:
本题难度:一般
3、填空题 NH3和CO是重要的化工原料气。
(1)一定条件下,CO与H2反应可制得甲醇CO+2H2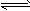 CH3OH
CH3OH
图1表示该反应进行过程中的能量变化(曲线a未使用催化剂,曲线b使用催化剂)。图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
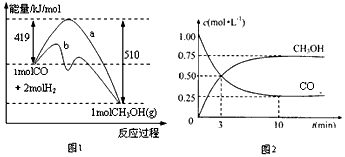
①根据上图1,写出在该条件下CO制备甲醇的热化学反应方程式__________________________
②根据上图2计算该该温度下,反应CO(g)+2H2(g)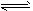 CH3OH(g)的平衡常数为_________________
CH3OH(g)的平衡常数为_________________
③图2所示的具体反应,若在温度保持不变、恒压情况下(体积可变)达到平衡,则H2的平衡转化率将
__________ (填“增大”、“减小”或“不变”)。
(2)已知:
a.常温下,CH3COOH和NH3・H2O的电离平衡常数均为1.74×10-5
b.CH3COOH + NaHCO3=CH3COONa+ CO2↑+ H2O
则NH4HCO3溶液呈______性(填“酸”、“碱”或“中”),溶液中浓度最大的离子是______,其次是
_______(以上填化学式)。
(3)室温下,向一定量的稀氨水中逐滴加入浓度相同的稀盐酸,直至盐酸过量。
①当溶液中离子浓度关系满足c(NH4+)<c(Cl-)时,则反应的情况可能为_____________
A. 盐酸不足,氨水剩余 B. 氨水与盐酸恰好完全反应 C. 盐酸过量
②实验过程中,H2O的电离程度先_______后________(填“增大”、“减小”或“不变”)。
参考答案:(1)①CO(g)+2H2(g)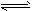 CH3OH(g) △H=-91kJ・mol-1;②12L2/mol2;③增大
CH3OH(g) △H=-91kJ・mol-1;②12L2/mol2;③增大
(2)碱性;NH4+;HCO3-
(3)①ABC;②增大;减小
本题解析:
本题难度:困难
4、选择题 在其他条件不变时,纯净水中加入下列物质,不会影响水的电离平衡的是( )
A.FeCl3
B.NaOH
C.H2SO4
D.NaNO3
参考答案:D
本题解析:
本题难度:一般
5、选择题 下列电离方程式书写正确的是
[? ]
A.NaHSO4=Na++H++SO42-
B.NaHCO3=Na++H++CO32-
C.CH3COOH CH3COO-+H+
CH3COO-+H+
D.H2CO3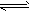 2H++CO32-
2H++CO32-
参考答案:AC
本题解析:
本题难度:简单