微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 21世纪是钛的世纪。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
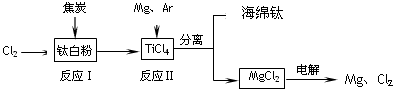
已知: ① Mg(s)+Cl2 (g)=MgCl2 (s) △H=-641 kJ・mol-1
② Cl2(g)+1/2Ti (s)=1/2TiCl4 (l) △H=-385 kJ・mol-1
(1)钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。TiO2+发生水解的离子方程式为______________________________________ 。
(2)反应Ⅰ在800~900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式为_______________________ ;反应Ⅱ的热化学方程式为________________________ 。
(3)该工艺流程中,可以循环使用的物质有_______________________ 。
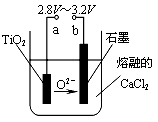
(4)在800℃~1000℃时电解TiO2也可制得海绵钛,装置如下图所示。图中b是电源的__________ 极,阴极的电极反应式为_____________________ 。
参考答案:(1)TiO2++2H2O=H2TiO3↓+2H+
(2)TiO2+2Cl2+2C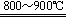 TiCl4+2CO;2Mg(s)+TiCl4(l)=2MgCl2(s)+Ti(s) △H=-512 kJ・mol-1(3)Mg、Cl2
TiCl4+2CO;2Mg(s)+TiCl4(l)=2MgCl2(s)+Ti(s) △H=-512 kJ・mol-1(3)Mg、Cl2
(4)正;TiO2+4e-=Ti+2O2-
本题解析:
本题难度:一般
2、选择题 铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶的甲基磺酸铅为电解质,电池总反应:Pb+PbO2+4H+ 2Pb2++2H2O。下列有关新型液流式铅酸蓄电池的说法正确的是
2Pb2++2H2O。下列有关新型液流式铅酸蓄电池的说法正确的是
[? ]
A. 充放电时,溶液中Pb2+浓度保持不变
B. 充放电时,溶液的导电能力变化不大
C. 放电时的负极反应式为:Pb-2e-=Pb2+
D. 充电时的阳极反应式为:Pb2++4OH-+2e-=PbO2+2H2O
参考答案:BC
本题解析:
本题难度:一般
3、实验题 (14分)如图所示,以石墨为电极电解A的水溶液,并做下面一系列实验。试根据实验现象完成下列问题(电解质A的水溶液焰色反应呈紫色)。
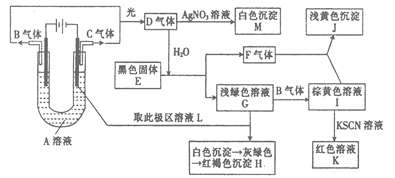
(1)A的化学式为? ?,E的名称为? ?。
(2)I和F反应的离子方程式是? ? ?。
(3)若将电解装置中的阳极换成铁棒,则在U型管底部可观察到的现象是??
? ?,阳极的电极反应式为? ?,阴极的电极反应式为? ?,电解的化学方程式为? ? ?。
参考答案:
(1)KCl;?硫化亚铁
(2)2Fe3+ + H2S==2Fe2+ + S↓+ 2H+
(3)产生了白色絮状沉淀? Fe-2e-=Fe2+? 2H++2e-=H2↑? Fe+2H2O Fe(OH)2↓+H2↑
Fe(OH)2↓+H2↑
本题解析:略
本题难度:简单
4、填空题 (10分)某学生试图用电解法根据电极上析出物质的质量来验证阿伏伽德罗常数的值,其实验方案的要点为:
①用直流电电解氯化铜溶液,所用仪器如图:

②在电流为I A,通电时间为t s后,精确测得某电极上析出的铜的质量为m g.
试回答:
(1)连接这些仪器的正确顺序为:(用图中标注仪器接线柱的英文字母表示,下同)E接________,C接________,________接F.
(2)写出B电极上发生反应的离子方程式________________.G试管中淀粉KI溶液变化的现象为__________________,相应的离子方程式是__________________.
(3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序是________.(选填下列操作步骤的编号)
①称量电解前电极质量
②刮下电解后电极上的铜并清洗
③用蒸馏水清洗电解后电极
④低温烘干电极后称量
⑤低温烘干刮下的铜后称量
⑥再次低温烘干后称量至恒重
(4)已知电子的电荷量为1.6×10-19C.试列出阿伏伽德罗常数的计算表达式:NA=________.
参考答案:(1)D A B?(2)2Cl--2e-===Cl2↑ 溶液变蓝? Cl2+2I-===2Cl-+I2
(3)①③④⑥?(4)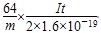 mol-1
mol-1
本题解析:(1)B电极上应产生Cl2:2Cl--2e-===Cl2↑,B极上流出电子,电子进入直流电源的正极,即F极,由此可得仪器连接顺序及电流方向。
(2)B中产生Cl2,Cl2进入G中与KI反应,有I2生成,I2使淀粉变蓝色。
(3)镀在A电极上的Cu是没必要刮下的,也无法刮干净,故②⑤两步须排除在外。
(4)因为析出Cu的物质的量=m/64mol,电子转移物质的量为m/64×2 mol,即m/64×2×NA个电子,由于电子的电荷量为1.6×10-19C,所以m/64×2×NA×1.6×10-19=It,
则NA=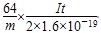 mol-1。
mol-1。
本题难度:一般
5、简答题 (20分) Ⅰ.(1)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,该反应的化学方程式为 ;
生成0.1molK2FeO4转移的电子的物质的量 mol。
(2)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:
3Zn+2K2FeO4+8H2O  3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
放电时电池的负极反应式为 。充电时电解液的pH (填“增大”“不变”或“减小”)。
Ⅱ.NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:

(1)相同条件下,0.1 mol・L-1NH4Al(SO4)2中c(NH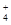 ) (填“等于”、“大于”或“小于”)0.1 mol・L-1NH4HSO4中c(NH
) (填“等于”、“大于”或“小于”)0.1 mol・L-1NH4HSO4中c(NH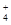 )。
)。
(2)如图1是0.1 mol・L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol・L-1NH4Al(SO4)2的pH随温度变化的曲线是 (填写字母);
②20℃时,0.1 mol・L-1NH4Al(SO4)2中2c(SO )-c(NH
)-c(NH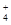 )-3c(Al3+)= mol・L-1。
)-3c(Al3+)= mol・L-1。
(3)室温时,向100 mL 0.1 mol・L-1NH4HSO4溶液中滴加0.1 mol・L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是 ;在b点,溶液中各离子浓度由大到小的排列顺序是 。
(4)已知Al(OH)3为难溶物(常温下,Ksp[Al(OH)3]=2.0×10-33)。当溶液pH=5时,某溶液中的
Al3+ (填“能”或“不能”)完全沉淀(溶液中的离子浓度小于1×10-5 mol・L-1时,沉淀完全)。
参考答案:(20分)
Ⅰ、(1)2Fe(OH)3 + 3KClO + 4KOH = 2K2FeO4 + 3KCl + 5H2O (2分) 0.3 (2分)
(2)Zn + 2OH- - 2e- = Zn(OH)2 (2分) 减小(2分)
Ⅱ、(1) 小于 (2分) (2)①A (2分) ②10-3-10-11 (2分)
(3)a (2分) c(Na+)>c(SO )>c(NH
)>c(NH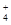 )>c(OH-)=c(H+) (2分)
)>c(OH-)=c(H+) (2分)
(4)能 (2分)
本题解析:Ⅰ、(1)KClO在KOH存在条件下,把Fe(OH)3氧化为K2FeO4,同时生成KCl、H2O,根据化合价升降法配平可得化学方程式:2Fe(OH)3 + 3KClO + 4KOH = 2K2FeO4 + 3KCl + 5H2O;根据Fe元素化合价变化可得:K2FeO4 ~ 3e?,所以生成0.1molK2FeO4转移的电子的物质的量为0.3mol。
(2)放电时电池的负极发生氧化反应,元素化合价升高,根据总方程式可得放电时电池的负极反应式为:Zn + 2OH- - 2e- = Zn(OH)2,根据化学方程式,充电时消耗KOH,所以充电时电解液的pH减小。
Ⅱ、(1) NH4HSO4为强酸的酸式盐,电离出的H+抑制NH4+的水解,所以相同条件下,0.1 mol・L-1NH4Al(SO4)2中c(NH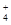 )小于 0.1 mol・L-1NH4HSO4中c(NH
)小于 0.1 mol・L-1NH4HSO4中c(NH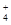 )。
)。
(2)①NH4Al(SO4)2中NH4+和Al3+水解使溶液显酸性,温度升高,水解程度增大,pH减小,故符合0随温度变化的曲线为A。
②根据示意图可知:20℃时,0.1 mol・L-1NH4Al(SO4)2pH为3,则c(H+)=10-3mol?L?1,c(OH?)= 10-11mol?L?1,根据电荷守恒可得:c(H+)+c(NH4+)+3c(Al3+)=c(OH?)+2c(SO42?),所以2c(SO )-c(NH
)-c(NH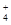 )-3c(Al3+)=c(H+)―c(OH?)= 10-3-10-11
)-3c(Al3+)=c(H+)―c(OH?)= 10-3-10-11
(3)a点显酸性,NH4+、Al3+水解,促进了H2O的电离,b点为中性,没有其它离子干扰,c、d显碱性,NaOH过量,抑制了H2O的电离,所以水的电离程度最大的是a;b点为中性,c(H+)=c(OH?),根据电荷守恒,c(Na+)+c(NH4+)=2c(SO42?),溶液显中性,NaOH应稍过量,抵消NH4+水解产生的H+,所以离子浓度由大到小顺序为:c(Na+)>c(SO )>c(NH
)>c(NH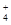 )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
(4)溶液的pH=5,则c(OH?)=10-9mol?L?1,带入c(Al3+)?c3(OH?)= 2.0×10-33,解得c(Al3+)= 2.0×10-6mol?L?1,所以Al3+ 完全沉淀。
考点:本题考查氧化还原反应、电化学原理、盐类的水解、离子浓度比较、Ksp的应用。
本题难度:困难