微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示。下列说法不正确的是
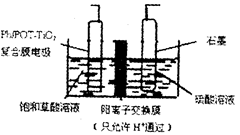
A.电解时石墨电极应与直流电源的正极相连
B.阴极反应式为:HOOCCOOH+2H++2e-=OHCCOOH+H2O
C.电解时石墨电极上有O2放出
D.电解一段时间后,硫酸溶液的pH不变化
参考答案:D
本题解析:由题目提供的信息可知草酸(HOOCCOOH)在电解时被还原得到乙醛酸(OHCCOOH)。还原反应应该是在阴极发生的。所以石墨电极应该与电源的正极相连,作阳极。阳极的电极反应式为:2H2O-4e-=4H++ O2↑,产生氧气。Pb电极为阴极,阴极发生还原反应,反应的方程式为HOOCCOOH+2H++2e- =OHCCOOH+H2O。由上述电极反应式可以看出,H2SO4的物质的量没有变化,水的物质的量也没有变化,但是草酸要不断的消耗,所以溶液的酸性减弱,溶液的pH会增大。因此错误的选项为D.
本题难度:简单
2、选择题 下列说法正确的是
A.金属腐蚀就是金属原子失去电子被还原的过程
B.钢铁吸氧腐蚀时,负极反应式为2H2O+O2+4e-===4OH-
C.氯碱工业中,阳极发生的反应为2Cl--2e-===Cl2↑
D.工业上电解精炼铜时,阳极减小的质量和阴极增加的质量相等
参考答案:C
本题解析:金属腐蚀就是金属原子失去电子被氧化的过程。原电池中负极是失去电子的,所以钢铁吸氧腐蚀时,负极反应式为Fe-2e-=Fe2+。电解池中阳极失去电子,发生氧化反应,C正确。应用粗铜中含有各种杂质,所以阳极减小的质量和阴极增加的质量不相等。答案是C。
本题难度:一般
3、选择题 下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是
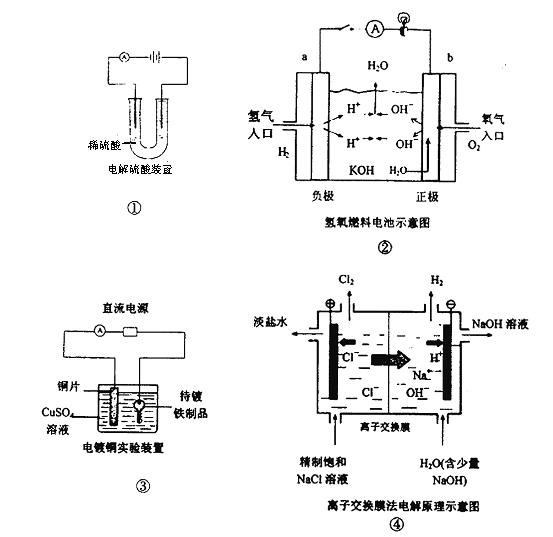
A.装置①中电解一段时间后,溶液的PH不变。
B.装置②中b极为正极,该极的电极反应方程式为O2+4H++ 4e-=2H2O
C.装置③中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol
电子转移,此时铜片和铁制品的质量差为128g
D.装置④中阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2
参考答案:C
本题解析:A项,电解稀硫酸实质是电解水,电解过程中,硫酸的物质的量不变,溶液的体积减少,H+的浓度增大,溶液的PH减少;B项,该电池的电解质溶液为KOH溶液,故该极的电极反应式应为O2+2H2O+4e-=4OH-;C项,阴极反应式:Cu2++2e-="Cu" ,即2mol电子转移时铜片质量增加64克,阳极反应式:Cu-2e-= Cu2+,当2mol电子转移时,铜片质量减少64克,故铜片和铁制品的质量差为128g。D项,阳离子交换膜上每透过1mol Na+时,电子转移1mol,据阴极反应式:2H+ + 2e-+ =H2 ↑,若在标准状况下,产生11.2L H2,但题意中无此条件,故D项错。
本题难度:一般
4、填空题 (14分)高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是 价,Na2FeO4具有较强的 (填“氧化性”或“还原性”)。
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是 (用离子方程式表示)。
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 + 10NaOH + 3NaClO = 2 + 5 + 9 。
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4 。
① 若电解所需的浓NaOH溶液为16 mol/L,则在实验室配制500 mL该浓度的溶液需NaOH g,配制过程所需玻璃仪器是 。
② 电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:

阳极的电极反应式是 ;可循环使用的物质是 ,理由是 。
参考答案:(1)+6, 氧化性(各1分,共2分)(2)Fe3++3H2O  Fe(OH)3+3H+ (2分)
Fe(OH)3+3H+ (2分)
(3)Na2FeO4 H2O NaCl (2分) (4)① 320,烧杯、玻璃棒、500 mL容量瓶、胶头滴管
(计算2分,仪器答对2个给1分,答对4个给2分,没有500mL容量瓶扣1分) ②Fe-6e-+8OH-=FeO42-+4H2O(2分);NaOH溶液(1分);水电离的H+在阴极放电:2H++2e-=H2↑,c(OH-)增大,Na+通过阳离子交换膜进入阴极区,使阴极区c(NaOH)增大,故可以循环使用(1分)
本题解析:(1)Na2FeO4中钠和氧元素的化合价分别是+1价和―2价,则根据正负价代数和为0可知铁元素的化合价是+6价价。+6价的铁易得到电子,则Na2FeO4具有较强的氧化性。
(2)Fe3+在溶液中水解生成氢氧化铁胶体,胶体具有吸附性可以净水,反应的离子方程式表示为Fe3++3H2O  Fe(OH)3+3H+。
Fe(OH)3+3H+。
(3)根据方程式可知铁元素的化合价从+3价升高到+6价失去3个电子,氯元素的化合价从+1价降低到―1价,得到2个电子,则根据电子得失守恒可知氧化剂与还原剂的物质的量之比是3:2,所以根据质量守恒定律可知反应的化学方程式可表示为2FeCl3 + 10NaOH + 3NaClO=2 Na2FeO4+ 5H2O + 9 NaCl。
(4)①实验室配制500 mL该浓度的溶液需NaOH的质量是16mol/L×0.5L×40g/mol=320g。配制过程所需玻璃仪器是烧杯、玻璃棒、500 mL容量瓶、胶头滴管。
②电解池中阳极失去电子,则根据装置图可知阳极是铁电极,铁失去电子转化为高碳酸盐,阳极反应式为Fe-6e-+8OH-=FeO42-+4H2O;由于水电离的H+在阴极放电:2H++2e-=H2↑,c(OH-)增大,Na+通过阳离子交换膜进入阴极区,使阴极区c(NaOH)增大,故氢氧化钠可以循环使用。
考点:考查高碳酸盐的性质以及制备
本题难度:困难
5、选择题 有两只串联的电解池(Pt为电极),甲池盛有足量的CuSO4溶液,乙池盛有足量的某硝酸盐的稀溶液.电解时当甲池电极析出6.4gCu时,乙池电极析出21.6g金属,则乙池的溶质可能是( )
A.NaNO3
B.Cu(NO3)2
C.Al(NO3)3
D.AgNO3
参考答案:甲池盛有足量的CuSO4溶液,电解过程中,阴极上的电极反应为:Cu2++2e-=Cu,
当该电极析出6.4gCu即0.1molCu时,转移电子为0.2mol,在转移这些电子的情况下,乙池电极会析出21.6g金属,,设乙池析出金属M,其相对原子量为M,乙池中阴极反应为
? ?Mx++xe-=M,
?1?x? 1
? 0.2mol?2.16M?
则M和x的关系满足:1.08xM=0.1,
将四个选项的金属元素化合价x和相对原子量M代入上式,只有D符合,即x=1,M=108.
故选D.
本题解析:
本题难度:简单