微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
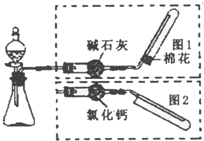
1、实验题 某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置。

实验步骤及现象如下:
①检查装置气密性后,装入药品并连接仪器。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体。
③一段时间后,将导管末端伸入集气瓶中收集气体。装置D中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色。
回答下列问题:
(1)装置B中的湿润的红色纸条褪色,证明A中反应有________(填化学式)生成。若B中改放湿润的淀粉KI试纸,仅凭试纸变蓝的现象不能证明上述结论,请用离子方程式说明原因___________________________________________。
(2)装置C的作用是____________________________________________。
(3)甲同学认为O2是Na2O2被盐酸中的HCl还原所得。乙同学认为此结论不正确,他可能的理由为①________;②________。
(4)实验证明,Na2O2能与干燥的HCl反应,完成并配平该化学方程式。
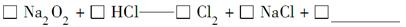
该反应________(填“能”或“不能”)用于实验室快速制取纯净的Cl2,理由是____________________________________________(要求答出要点)。
参考答案:(1)Cl2 4H++4I-+O2=2I2+2H2O(或4I-+O2+2H2O=2I2+4OH-)
(2)吸收HCl和过量的Cl2,防止污染空气,使D中能收集到较为纯净的氧气
(3)①Na2O2被还原时氧元素的化合价应该降低,不可能得到O2
②O2有可能是Na2O2与盐酸中的H2O反应生成的
(4) 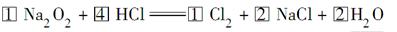
不能 实验室没有可直接使用的干燥HCl气体的物质;固体与气体反应较慢;产生的氯气中含有大量的氯化氢气体(答出任何一点即可,其他合理答案均可)
本题解析:(4)选择Na2O2、Cl2配平,Na2O2中氧的化合价降低2价、生成氯气化合价升高2价,所以Na2O2、Cl2的化学计量数均为1,再配NaCl的化学计量数为2。
本题难度:一般
2、选择题 下列气体不能用H2SO4干燥的是
[? ]
A.CO2
B.NH3
C.SO2
D.HC1
参考答案:B
本题解析:
本题难度:简单
3、选择题 利用下列实验装置进行的相应实验,能达到实验目的的是
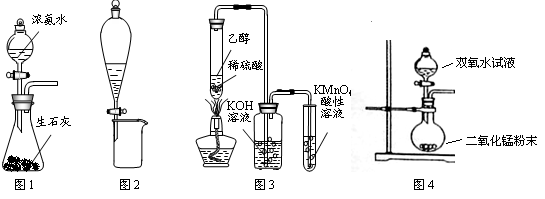
A.图1所示装置可制备氨气
B.图2所示装置可分离CH3CH2OH和CH3COOC2H5的混合液
C.图3所示装置可制备、收集乙烯并验证其易被氧化
D.图4所示装置可制备氧气
参考答案:AD
本题解析:A、生石灰与水反应生成氢氧化钙增大氨水中的氢氧根离子浓度,抑制一水合氨的电离,有利于氨气的逸出,同时生石灰溶于水放热,减小氨气的溶解度,所以可以用该装置制备氨气,正确;B、CH3CH2OH和CH3COOC2H5互溶,不分层,不能分液,错误;C、乙醇在浓硫酸作催化剂、加热条件下发生消去反应生成乙烯,而图中是稀硫酸,错误;D、过氧化氢在二氧化锰作催化剂条件下分解产生氧气,二氧化锰固体放在圆底烧瓶里,过氧化氢放在分液漏斗里,正确,答案选AD。
本题难度:一般
4、选择题 下图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是
| 发生装置的药品 | 干燥和集气装置
A
氧化钙和浓氨水
图1
B
大理石和稀盐酸
图1
C
铜和稀硝酸
图2
D
电石和水
图2
|
( )
A.A
B.B
C.C
D.D