微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (14分)下图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。
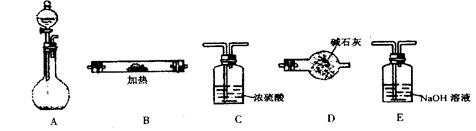
(1)若烧瓶中盛装锌片,分液漏斗中盛装稀硫酸,则:
①当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末。此实验的目的是?。D装置的作用是?。
②为了使B中CuO反应充分,在不改变现有药品的条件下,可采取的方法有(写一种)?。
③加热前必须进行的 操作是?。
操作是?。
(2)若烧瓶中盛装Na2O2固体,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,则:
① 烧瓶内产生的气体主要有(写化学式)?。
烧瓶内产生的气体主要有(写化学式)?。
②用产生的气体做氨的催化氧化实验,各仪器装置按气流方向从左到右 连接顺序是(填字母)( )→(
连接顺序是(填字母)( )→(  )→( )→E
)→( )→E
③试管B中的反应方程式为??
参考答案:(1)①验证H2的还原性并检验其氧化产物;
防止空气中的水进入装置,干扰H2氧化产物的检验
②控制分液漏斗的活塞,使稀H2SO4缓慢滴下(或在烧瓶中加水或将烧瓶放入冰水中或用冰毛巾捂着烧瓶或加入 醋酸钠固体等,其他合理答案亦可给分);
醋酸钠固体等,其他合理答案亦可给分);
③检验装置中空气是否排尽或检验氢气是否纯净。
(2)① O2、NH3?② A→D→B;③4NH3 +5O2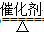 4NO +6H2O
4NO +6H2O
本题解析:略
本题难度:一般
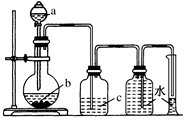
2、选择题 实验室中制取、洗气并收集气体的装置如图所示。仅用此该装置和表中提供的物质完成相关实验,最合理的选项是
选项
| a中的液体
| b中的固体
| c中液体
|
A
| 浓盐酸
| MnO2
| 饱和食盐水
|
B
| 浓氨水
| 生石灰
| 浓H2SO4
|
C
| 浓硫酸
| Cu片
| NaOH溶液
|
D
| 稀HNO3
| Cu片
| H2O
|
?
参考答案:D
本题解析:A、浓盐酸与MnO2反应需要加热,装置图中无酒精灯,错误;B、浓氨水与生石灰可制取氨气,氨气不能用浓硫酸干燥,错误;C、浓硫酸与Cu反应需要加热,生成的SO2不能用NaOH溶液除去杂质,也不能用排水法收集,错误;D、Cu与稀硝酸反应可制取NO,NO可用水洗气,可用排水法收集,正确。
本题难度:一般
3、实验题 (1)写出实验室制乙烯的化学方程式
(2)该实验需加入碎瓷片目的是
(3)下列实验操作正确的是
A、配制乙醇与浓硫酸的混合液时,将1体积乙醇沿烧杯器壁缓缓注入3体积的浓硫酸中,并用玻璃棒不断搅拌
B、加热混合液时,应小心加热使温度缓缓上升至所需温度
C、温度计水银球的位置应伸入液面之下,而不是液面之上
D、收集乙烯气体时应用排水法收集,不能用排空气法收集
(4)在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:
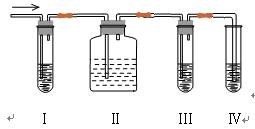
① I、II、III、IV装置可盛放的试剂是
I?;II?;III?;IV?(将下列有关试剂的序号填入空格内)。
A、NaOH溶液? B、酸性KMnO4溶液? C、溴水? D、品红溶液
②能说明SO2气体存在的现象是?。
③确定含有乙烯的现象是?。
参考答案:
(1)C2H5OH CH2=CH2? +H2O?(2分,条件1分,方程式1分)
CH2=CH2? +H2O?(2分,条件1分,方程式1分)
(2)防暴沸?(1分)
(3)C D?(2分,多选一个倒扣一分)
(4)① D A D B 或 D A D C?(每空1分)
② I中品红褪色?(1分)
③ III中品红不褪色,IV中KMnO4?溶液褪色或溴水褪色?(2分)
本题解析:略
本题难度:简单
4、实验题 为了证明CO具有还原性,有人设计了如图所示的实验.
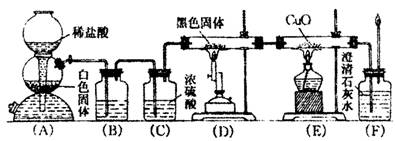
(1)装置B的最适宜的试剂是?.
(2)装置D中发生反应的化学方程式是?.
(3)必须用装置C吸收除去气体中水蒸气的理由是?.
(4)若根据F中石灰水变浑浊的现象也能确认CO具有还原性,应在下图中装置?与?之间连下图所示的?装置(填序号).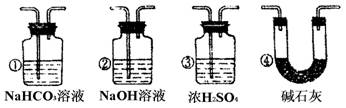
参考答案:

本题解析:略
本题难度:简单
5、实验题 (10)按要求完成硝酸钾晶体的制备实验:
步骤
| 操作
| 具体操作步骤
| 现象解释结论等
|
?
①
| 溶解
| 取20克NaNO3和17克KCl溶解在35ml水中,加热至沸,并不断搅拌。
| 固体溶解
|
②
| 蒸发
| 继续加热搅拌,使溶液蒸发浓缩。
| 有?a?晶体析出。
|
③
| 热过滤
| 当溶液体积减少到约原来的一半时,迅速趁热过滤
| 滤液中的最主要成分为?b?。
|
④
| 冷却
| 将滤液冷却至室温。
| 有晶体析出。
|
 ⑤ ⑤
| ?
| 按有关要求进行操作
| 得到初产品硝酸钾晶体
|
⑥
| ?
| 将得到的初产品硝酸钾晶体溶于适量的水中,加热、搅拌,待全部溶解后停止加热,使溶液冷却至室温后抽滤。
| ?
得到纯度较高的硝酸钾晶体
|
⑦
| ?
检验
| 分别取⑤、⑥得到的产品,配置成溶液后分别加入1滴1mol/l的HNO3和2滴0.1mol/l的AgNO3
| 可观察到⑤、⑥产品中出现的现象分别是⑤产品中产生白色沉淀,⑥产品中无明显现象。
|
(1)把上述各步骤中的内容补充完整:a: b: ?
(2)写出步骤③趁热过滤的目的?,步骤⑥的操作名称?,步骤⑦中产生白色沉淀的离子方程式?
(3)步骤⑥的抽滤装置如图所示,仪器A的名称?,该装置中的错误之处是?;抽滤完毕或中途需停抽滤时,应先?,然后?。
参考答案:(1)NaCl;? KNO3
(2)防止因温度降低而析出硝酸钾晶体;重结晶;Ag++ Cl-= AgCl↓
(3)?布氏漏斗;布氏漏斗的颈口斜面未朝向抽滤瓶的支管口;断开连接安全瓶与抽气装置间的橡皮管;关闭抽气装置的水龙头
本题解析:(1)氯化钠的溶解度小,蒸发浓缩首先写出氯化钠,即a是氯化钠。硝酸钾的溶解度受温度影响大,所以降低温度时氯化钠析出,则b是硝酸钾。
(2)步骤③趁热过滤的目的防止因温度降低而析出硝酸钾晶体。为了得到纯净的硝酸钾晶体,需要重结晶。氯离子能和银离子反应生成氯化银沉淀,方程式为Ag++ Cl-= AgCl↓。
(3)根据仪器结构特点可知,A是布氏漏斗,抽滤时布氏漏斗的颈口斜面未朝向抽滤瓶的支管口,所以该处是错误的。抽滤完毕或中途需停抽滤时,应先断开连接安全瓶与抽气装置间的橡皮管,然后再关闭抽气装置的水龙头。
本题难度:一般