微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将0.01 mol下列物质分别加入100 mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度的大小顺序是(溶液体积变化忽略不计)
①Na2O2 ②Na2O ③Na2CO3 ④NaCl
A.①>②>③>④
B.①>②>④>③
C.①=②>③>④
D.①=②>③=④
参考答案:C
本题解析:0.01 mol Na2O2、Na2O与水反应的方程式分别为Na2O2+H2O=2NaOH+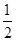 O2↑、Na2O+H2O=2NaOH,二者均产生0.02 mol OH-,因溶液体积变化忽略不计,故所得溶液中阴离子浓度:①=②;Na2CO3和NaCl电离产生的阴离子均为0.01 mol,而CO32―发生微弱的水解:CO+H2O
O2↑、Na2O+H2O=2NaOH,二者均产生0.02 mol OH-,因溶液体积变化忽略不计,故所得溶液中阴离子浓度:①=②;Na2CO3和NaCl电离产生的阴离子均为0.01 mol,而CO32―发生微弱的水解:CO+H2O HCO+OH-,使阴离子数目增多,所得溶液中阴离子浓度:③>④。
HCO+OH-,使阴离子数目增多,所得溶液中阴离子浓度:③>④。
本题难度:一般
2、选择题 欲观察H2燃烧的颜色,燃气导管的材料最好是(?)
A.钠玻璃
B.钾玻璃
C.石英玻璃
D.铜管
参考答案:C
本题解析:Na、K、Cu元素的焰色:黄、紫、绿,产生干扰,不利于观察H2燃烧时的颜色。在石英玻璃(主要成分是SiO2)管口燃烧,无干扰。
本题难度:简单
3、选择题 将11.5 g金属钠投入到足量水中,得溶液a;将12 g Mg投入到与水等质量的足量盐酸中,得溶液b。则a和b的质量关系为(?)
A.a="b"
B.a>b
C.a<b
D.无法比较
参考答案:A
本题解析:由于两反应中均有气体产生,因此需先求生成气体的质量。
2Na+2H2O 2NaOH+H2↑
2NaOH+H2↑
46? 2
11.5 g?m1(H2)
Mg+2HCl MgCl2+H2↑
MgCl2+H2↑
24? 2
12 g?m2(H2)
m1(H2)=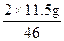 ="0.5" g
="0.5" g
m2(H2)= 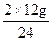 ?="1" g
?="1" g
则m(a)="11.5" g-0.5 g+m(H2O)="11" g+m(H2O)
m(b)="12" g-1 g+m〔HCl(aq)〕="11" g+m〔HCl(aq)〕。
又因为m(H2O)=m〔HCl(aq)〕,所以m(a)=m(b)。
本题难度:简单
4、选择题 下列关于Na和Na+性质的叙述中,正确的是
A.它们都是强还原剂
B.它们的化学性质相同
C.它们都显碱性
D.它们灼烧时都能使火焰呈现黄色
参考答案:D
本题解析:略
本题难度:简单
5、选择题 下列物质混合后溶液中溶质的质量分数最大的是(?)
A.4.6g钠投入45.4g水中
B.6.2g氧化钠投入42.2g水中
C.7.8g过氧化钠投入42.2g水中
D.8g烧碱投入42g水中
参考答案:BD
本题解析:钠、氧化钠、过氧化钠的物质的量分别是0.2mol、0.1mol、0.1mol,氢氧化钠是0.2mol。钠、氧化钠、过氧化钠和水反应的方程式分别如下:
2Na+2H2O=2NaOH+H2↑,溶液的质量=4.6g+45.4g-0.2g=49.8g
Na2O+H2O=2NaOH,溶液的质量=48.4g
2Na2O2+2H2O=4NaOH+O2↑,溶液的质量=48.4g
将氢氧化钠加入水中,溶液的质量=50g
根据钠原子守恒知,钠、氧化钠、过氧化钠、氢氧化钠溶于水所得氢氧化钠的物质的量都是0.2mol,因此通过以上分析可知选项BC中质量分数最大且是相等的,因此答案选BC。
点评:该题是高考中的常见题型和考点,属于中等难度的试题。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力和灵活应变能力。该题的关键是明确反应原理,然后依据方程式和题意灵活运用即可。
本题难度:一般