��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �±���Ԫ�����ڱ���һ���֣�����Ҫ��ش��������⡣
?��
����
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| O
|
2
| ?
| ?
| ?
| E
| H
| F
| I
| ?
|
3
| A
| C
| D
| ?
| ?
| ?
| G
| R
|
4
| B
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
��1��ʮ��Ԫ���л�ѧ��������õ�Ԫ����________����Ԫ�ط��ţ���
��2��A��C��D����Ԫ�ص��������Ӧ��ˮ������м�����ǿ����________���ѧʽ����
��3��IԪ�ظ�AԪ���γɻ�����ĵ���ʽ��________���������ոû�����ʱ�������________ɫ��
��4��G�ĵ��ʺ�B������������Ӧˮ���ﷴӦ�����ӷ���ʽ��__________________��
Ԫ��A��F���γ����ֻ����д�����н��ȶ��Ļ�������CO2��Ӧ���������Ļ�ѧ����ʽ? ________________________��
�ο��𰸣���1��Ar ��2��NaOH?��3�� ��
��
��4��Cl2+2OH- = Cl- + ClO- + H2O
(5)2Na2O2+2CO2=2Na2CO3+O2��
�����������Ԫ�����ڱ���֪��A:Na? B:K? C:Mg? D: Al? E:C? F:O? G:Cl? H:N? I:F? R:Ar
��1��ArΪ�������壬�����
��2��A ��C ��D����Ԫ�طֱ��Ӧ��ˮ����Ϊ NaOH�� Mg(OH)2��Al(OH)3����NaOH������ǿ��
��3�� ������Ϊ���ӻ������Ԫ����ɫ��ӦΪ��ɫ��
������Ϊ���ӻ������Ԫ����ɫ��ӦΪ��ɫ��
��4��B������������Ӧ��ˮ����Ϊǿ���ȫ���롣�ʷ�Ӧ����ʽ ΪCl2+2OH- = Cl- + ClO- + H2O
��5��A��F�γ�Na2O��Na2O2�������ʣ����к��߸��ȶ���
�����Ѷȣ�һ��
2������� ������Ԫ��A��B��C��D�У�0.5 mol AԪ�ص����ӵõ�6.02��1023�����Ӻ�ԭΪ����ԭ�ӣ�0.4 ��A��������ǡ����100 mL 0.2 mol��L-1��������ȫ��Ӧ��AԪ��ԭ�Ӻ�������������������ȣ�BԪ��ԭ�Ӻ����������AԪ��ԭ�Ӻ����������1��C-���Ӻ�����Ӳ�����AԪ�ص����Ӻ�����Ӳ�����1��DԪ��ԭ�������������Ǵ�����2����������������⣺
��1���ƶ�A��B��C��D����Ԫ�صķ��ţ�
A_______________��B_______________��C_______________��D_______________��
��2��C��ԭ�ӽṹʾ��ͼ____________________________��
��3��DԪ�ص����������Ľṹʽ��________________��
��4��C��DԪ����ɵ����ʣ������ں���____________������ԡ��Ǽ��ԡ������������Ϊ______________������ԡ��Ǽ��ԡ������ӡ�
��5���õ���ʽ��ʾA��C��Ԫ���γɻ�����Ĺ��̣�____________________________��
�ο��𰸣���1��Mg? Al? Cl? C
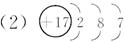
(3)O==C==O
(4)����?�Ǽ���
��5��
�����������0.5 mol AԪ�ص����ӵõ�6.02��1023�����ӣ�1 mol e-)��ԭΪ����ԭ�ӣ�֪AԪ�صĻ��ϼ�Ϊ+2����AO+2HCl====ACl2+H2O��֪0.4 g AO�����ʵ���n="0.2" mol��L-1��0.1 L��2="0.01" mol������AO��Ħ������Ϊ0.4 g/0.01 mol="40" g��mol-1����Aԭ�Ӻ�������������������ȣ���AΪMgԪ�ء�BԪ��ԭ�Ӻ����������Mgԭ�Ӻ����������1������B��AlԪ�ء�C-������Ӳ�����Mg2+������Ӳ�����1����C��ClԪ�ء�DԪ��ԭ�������������Ǵ�����2����D��CԪ�ء�
�����Ѷȣ���
3��ѡ���� 117��Ԫ����Uus��ʾ�����й���UusԪ�ص�˵���������(����)
A��ԭ�ӵļ۵����Ų�ʽ��7s27p5
B������ϼ��ǣ�7��
C���䵥����˫ԭ�ӷ��ӣ����³�ѹ�³���̬
D�������Ӿ��к�ǿ�Ļ�ԭ��
�ο��𰸣�C
���������Ԫ�����ڱ����ȫ�������������һ��Ԫ�ص�ԭ��������118����117Ԫ��λ�ڵ������ڵڢ�A�壬����Ԫ�����ʵĵݱ���ɿ�֪��ѡ��C����ȷ��������Ӧ���dzʹ�̬������ѡ�����ȷ�ģ���ѡC��
�������������е��Ѷȵ����⣬���������ǿ�����ؿ���ѧ����Ԫ�������ɵ���Ϥ�˽����ճ̶ȡ������ԡ����ڱ���Ԫ�ص��ƶϡ�Ϊ���壬����ѧ����Ԫ�����ڱ�����Ϥ�̶ȼ���Ա��и�Ԫ�����ʺ���Ӧԭ�ӽṹ�������Եݱ���ɵ���ʶ�����ճ̶ȡ�������ѧ�������ʽṹ�����ʹ�ϵ�Լ�����Ԫ�������ɽ�����廯ѧ�����������
�����Ѷȣ�һ��
4��ѡ���� ����������������������й������ʵ��ƶ���ȷ����(? )
A����������ˮ��Ӧ
B��������������ǿ�ᡢǿ����Һ��Ӧ
C��������Ļ�ѧʽΪBe2O3
D��������ֻ����ǿ����Һ��������ǿ����Һ
�ο��𰸣�B
�������������ˮ����Ӧ������Ҳ��ˮ����Ӧ������������������������ܺ�ǿ�ᡢǿ�Ӧ��������������Ҳ��ǿ�ᡢǿ���Ӧ�������ڵڢ�A������ǣ�2�ۣ�������Ļ�ѧʽΪBeO��������������������ܺ�ǿ�ᡢǿ�Ӧ������������Ҳ��ǿ�ᡢǿ���Ӧ����ѡB��
�����Ѷȣ�һ��
5������� ��14�֣���֪A��B��C��D��E����Ԫ�ص�ԭ���������ε�����A��B��C��Dλ��ǰ�����ڡ�AԪ�ز���B��C��D����Ԫ��ͬ���ڣ���ԭ���е��Ӳ�����δ�ɶԵ�������ͬ��B�Ļ�̬ԭ���е���ռ������������ͬ��ԭ�ӹ������ÿ�ֹ���еĵ���������ͬ��Dԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������3����A��B��D����Ԫ����ɵ�һ�ֻ�����M����װ�����г����е�һ���к����壻A��B����Ԫ����ɵ�ԭ�Ӹ�����Ϊ1�U1�Ļ�����N�dz������л��ܼ���E�С����������֮�ƣ�E4+���Ӻ��ԭ�ӵĺ�������Ų���ͬ��
��ش��������⣺������������漰��A��B��C��D��EԪ��ʱ��������Ӧ��Ԫ�ط��ű�ʾ��
��1��B��C��D����Ԫ�صĵ�һ��������С�����˳��Ϊ___________________��BD2�ĽṹʽΪ___________________��A3D+���ӵ�VSEPRģ��Ϊ___________________��B��C����̬�⻯������У����ǵĴ�С��ϵΪB_____C���>��= �� <������
��2��EԪ����Ԫ�����ڱ�����������_______��Ԫ�أ���Ԫ�ػ�̬ԭ�ӵ���Χ�����Ų�ʽΪ?��
��3������������ȷ����?��������ĸ��
A��AԪ��λ��Ԫ�����ڱ���s��������Ԫ�����ڱ�������Ԫ���е縺����С
B��M��N�����е�Bԭ�Ӿ�����sp2�ӻ�
C��N�����к���6���Ҽ���1���м�
D��BA4Ϊ����л���
��4��ij���ӻ�����R�Ļ�ѧʽΪCA5����������ԭ�ӵ�����㶼������Ӧ��ϡ������ԭ�ӵ��������ӽṹ����R�ĵ���ʽΪ____________��
��5����Ũ��ECl3��������Һ�м������ѣ���ͨ��HCl�����ͣ��ɵõ���λ��Ϊ6 �����ΪECl3��6H2O����ɫ���壬�þ�����������������ʵ���֮��Ϊ1�U5����������ӵĻ�ѧʽΪ?��
�ο��𰸣���1��N > O > C��2�֣���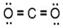 ��2�֣�?�����壨1�֣���>��1�֣�
��2�֣�?�����壨1�֣���>��1�֣�
��2��d ��1�֣�? 3d24s2��1�֣�
��3��B��D��2�֣�
��4��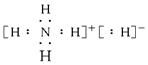 ��2�֣�
��2�֣�
��5��[TiCl(H2O)5]2+��2�֣�?�������Ӻ�ˮ���ӵ�λ�ò���Ҫ��
�����������
�����Ѷȣ���