��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��12�֣�������������Դ�������ȷ������Ź㷺����;��ʪ�����ɷ��Ʊ��������ε�ԭ�����±���ʾ��
ʪ����ǿ���Խ����У�Fe(NO3)3��NaClO��Ӧ�����Ϻ�ɫ����������Һ
�ɷ���Fe2O3��KNO3��KOH��ϼ��ȹ��������Ϻ�ɫ�������κ�KNO2�Ȳ���
��1����ҵ����ʪ���Ʊ�������أ�K2FeO4������������ͼ��ʾ��
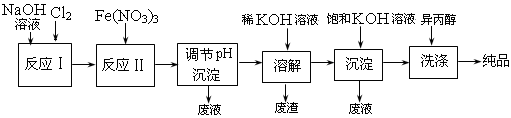
�ٷ�ӦI�Ļ�ѧ����ʽΪ����������?��������
�ڷ�ӦII�����ӷ���ʽΪ������?������������
�ۼ��뱥��KOH��Һ��Ŀ������������?����������
��2�����������һ�������ˮ���������䴦��ˮ��ԭ��Ϊ����������?������������? ______?____��
��3���ɷ��Ʊ�K2FeO4�ķ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ������������������
2������� ��20�֣���ҵ���ø�������Ҫ�ɷ�FeO��Cr2O3������ΪSiO2��Al2O3�ȣ�
�����ظ���أ���ѧʽK2Cr2O7�������������£�
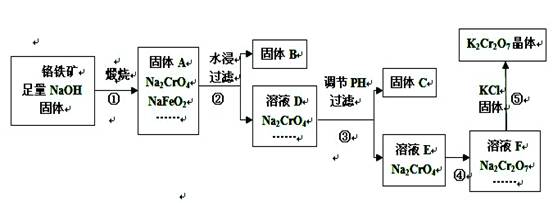
��1������A�У���Na2CrO4��NaFeO2��NaOH���?�ȣ�
��2������Aˮ��ʱ��NaFeO2�ᷢ��ǿ��ˮ���������B���仯ѧ��Ӧ����
ʽΪ?��
��3������C�к���2�����ʣ�Ҫ�ȼ������������е�?��Ȼ���
�ܽ��й��˷��롣
A������������Һ?B��ϡ��ˮ?C��ϡ����
��4������ܼ�������õ�����ҺF�У���Na2 Cr2O7�⣬�����е�����
��?��
��5�������������У���������ԭ��Ӧ�������ǵ�____����
��6����֪20��ʱK2Cr2O7������ҺŨ��Ϊ0.4 mol��L-1��������м����
���Ȼ��أ���ʹK+����Ũ�ȴﵽ4 mol��L-1�������¶�20�棩������ҺF��Cr2O72-���ӵ�Ũ�����Ϊ?��
3������� ( 14 ��)��Ԫ�����ڱ��У�п��30Zn�����ӣ�48Cd��������80Hg��ͬ����п�壬п������Ȼ���г��������ӵĽ�����Խ���п��֮�䡣ʪ����п�����в�����ͭ�����к���Cu��Cd��Zn�ȶ��ֽ��������������������ӡ��ӵ���Ҫ��;�����������D�ӵ�أ��Լ����������������ӻ����ﻹ��PVC�ȶ�����������ϡ��뵼����ϡ�ɱ�����ȷ����й㷺��Ӧ�á��ӵ�����������ͼʾ�����£�
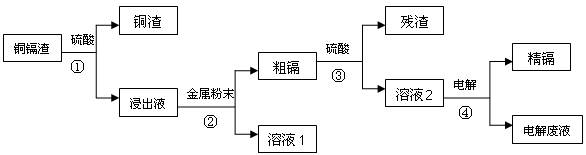 ��ش��������⣺
��ش��������⣺
��1����Ԫ��λ�����ڱ��е�?���ڣ���?�壬��ԭ�ӽṹʾ��ͼΪ?��
��2��д������ٷ�Ӧ�����ӷ���ʽ??��
��3�������������Ľ�����?��
��4��������á���Һ2�������Һ������?���������õ缫������
��5��������Һ���к����ӣ�����ֱ����Ϊ��ˮ�ŷš�Ŀǰ���ӵķ�ˮ�����ķ�ʽ�����֣�һ�����ں�����ˮ�м������ƣ����������ӣ���һ���Ǽ���ۺ��������;ۺ��Ȼ��������������ӡ�д�����Ƴ��������ӵ����ӷ���ʽ?��
4��ѡ���� �Ͻ���һ����;�㷺�Ľ������ϡ����������У������ںϽ����?
[? ]
A��̼�ظ�
B����ͭ
C��Ӳ��
D��ˮ��
5������� ��ʯΪ�����Σ���ѧʽ��Ca2Mg5Si8O22��OH��2����д����������ʽΪ______��