微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 氨在高温下进行催化氧化以制取NO不考虑NO与O2反应)时,其
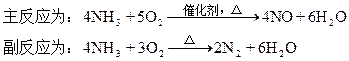
今在相同条件下将每1L氨混合10升空气后通入反应器。空气中O2和N2的体积百分含量分别以20%和80%计。上述反应完成后,测得混合气体中不含NH3,而O2与N2的物质的量之比为1∶10。试求参加主反应的氨占原料氨的体积百分含量(保留小数点后一位)。
参考答案:88.9%
本题解析:设1L氢中有x升与O2发生反应生成NO(即主反应),则参加副反应的氢为(1-x)L。
4NH3+5O2 4NO+6H2O
4NO+6H2O
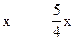
4NH3?+? 3O2? ?2N2+6H2O
?2N2+6H2O
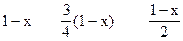

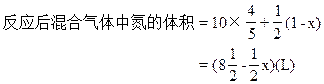
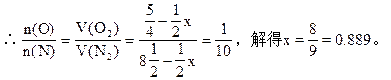
本题难度:一般
2、填空题 (4分)将铜片投入盛有稀硫酸的试管中无反应。当加入少量硝酸钾晶体后,试管内产生一种无色气体,这种气体在试管口变成红棕色。这种无色气体是__________。写出有关的离子反应方程式.________________________________________________________
参考答案:NO,3Cu + 8H+ + 2NO3― = 3Cu2+ + 2NO↑ + 4H2O
本题解析:略
本题难度:简单
3、选择题 砷为第4周期ⅤA元素,根据砷元素在元素周期表中的位置推测,砷不可能具有的性质是( )?
A.砷在通常状况下为固体?
B.As2O3对应水化物的酸性比H3PO4弱?
C.可以有-3、+3、+5等多种化合价?
D.砷的还原性比磷弱?
参考答案:D?
本题解析:同一主族元素,从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,最高价氧化物对应的水化物的酸性减弱。
本题难度:简单
4、实验题 某化学课外活动小组通过实验研究NO2的性质。
已知:2NO2+2NaOH NaNO3+NaNO2+H2O
NaNO3+NaNO2+H2O
任务1:利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
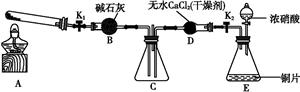
(1)E装置中制取NO2反应的化学方程式是? 。
(2)若NO2能够被NH3还原,预期观察到C装置中的现象是 ?。
(3)实验过程中,未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:
①NH3还原性较弱,不能将NO2还原;
②在此条件下,NO2的转化率极低;
③ ?。
(4)此实验装置存在一个明显的缺陷是?。
任务2:探究NO2能否与Na2O2发生氧化还原反应。
(5)实验前,该小组同学提出三种假设。
假设1:二者不反应;
假设2:NO2能被Na2O2氧化;
假设3: 。
(6)为了验证假设2,该小组同学选用任务1中的B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如图所示),重新组装,进行实验。

①装置的合理连接顺序是 ?。
②实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中反应的化学方程式为 。
参考答案:(1)Cu+4HNO3 (浓) Cu(NO3)2+2NO2↑+2H2O
Cu(NO3)2+2NO2↑+2H2O
(2)C装置中混合气体颜色变浅
(3)在此条件下,该反应的化学反应速率极慢
(4)缺少尾气吸收装置
(5)NO2能被Na2O2还原
(6)①EDBF ②2NO2+Na2O2 2NaNO3
2NaNO3
本题解析:(1)浓硝酸在加热条件下与铜片反应制取NO2:Cu+4HNO3 (浓) Cu(NO3)2+2NO2↑+2H2O。
Cu(NO3)2+2NO2↑+2H2O。
(2)由于NO2气体是红棕色的,若NO2能够被NH3还原,随NO2的消耗,气体颜色会变浅。
(3)①从反应能否发生角度作出假设;②从化学平衡角度作了假设;③可以从反应速率作出假设,也可能是二者反应速率极慢,短时间内无法观察到气体颜色的变化。
(4)NO2与NH3都是有毒气体,即使二者能够发生反应,也会反应不完全,剩余气体逸散到空气中造成污染。应该增加尾气处理装置。
(5)由于Na2O2中的氧元素处于-1价,既有氧化性,也有还原性,所以NO2也可能被Na2O2还原。
(6)①整个实验的设计原理为:利用E制取NO2气体,通过D装置进行干燥,然后进入B装置进行验证实验,最后通过F装置吸收未反应的NO2气体,所以装置的连接顺序是EDBF。
②白色物质为纯净物,且无其他物质生成,只可能是NO2被氧化为了N2O5,与生成的Na2O化合为了NaNO3。
本题难度:困难
5、选择题 不需要放入棕色瓶存放的溶液是(? )
A.浓硫酸
B.浓硝酸
C.浓氨水
D.硝酸银
参考答案:A
本题解析:见光易分解的物质一般需要保存在棕色瓶中,在4个选项中浓硫酸稳定,不易分解,所以答案是A。
本题难度:简单