微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 在标准状况下,560体积氨气溶解在1体积的水中,求制得氨水中溶质的质量分数。若制得氨水的密度为0.91 g・cm-3,求氨水的物质的量浓度。
参考答案:氨水中溶质的质量分数为29.8%;溶液的物质的量浓度为15.95 mol・L-1。
同步测验
本题解析:有关氨水浓度的计算,首先应明确溶质是氨分子。
标准状况下560体积的氨可以假定体积为560 L,便于计算。560 L除以22.4 L・mol-1即得到氨的物质的量,再乘以氨的摩尔质量便求出溶质的质量。溶质质量加上1 L水的质量即为溶液质量。
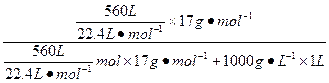 ×100%=29.8%
×100%=29.8%
知道氨水密度,再根据氨水的溶质质量分数便可以求出氨水的物质的量浓度。
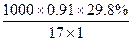 ?mol・L-1="15.95" mol・L-1
?mol・L-1="15.95" mol・L-1
本题难度:简单
2、选择题 体积为1L的干燥容器中充入氨气,测得容器中气体对氢气的相对密度为9.7。用此气体进行喷泉实验,当喷泉停止后,进入容器中液体的体积约是(? )
A.0.2L
B.0.25L
C.0.75L
D.0.8L
参考答案:D
本题解析: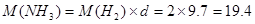 ,则根据“十字交叉”法可得它们的物质的量关系为:
,则根据“十字交叉”法可得它们的物质的量关系为:

即可知,在1L容器中,进入容器中液体的体积约是0.8L;
本题难度:一般
3、计算题 从某些方面看,氨和水相当,NH4+和H3O+(常写成H+)相当,NH2-和OH-相当,NH2-(有时还包括N3-)和O2-相当。已知在液氨中能发生下列两个反应:
NH4Cl+KNH2=KCl+2NH3
2NH4I+PbNH=PbI2+3NH3
请写出能在水溶液中发生与上述两反应相当的反应方程式。
参考答案:HCl+KOH=KCl+H2O
2HI+PbO=PbI2+H2O
本题解析:理清题给信息:NH4+和H3O+相当,NH2-和OH-相当,NH2-和O2-相当,然后将这些信息转换成解题所需信息(例如,NH4Cl相当于H3OCl,即HCl),并运用这些信息解题。有题给信息知,NH4Cl相当于H3OCl,即HCl,KNH2相当于KOH,NH3相当于H2O.所以液氨中发生的NH4Cl+KNH2=KCl+2NH3的反应相当于水溶液中发生的“酸+碱=盐+水”的中和反应,因而在水溶液中发生的与之相当的反应方程式为:
H3OCl+KOH=KCl+2H2O
可简写为:HCl+KOH=KCl+H2O
同理,NH4I相当于HI,PbNH相当于PbO,NH3相当于H2O,在液氨中发生的2NH4I+PbNH=PbI2+3NH3反应相当于水溶液中发生的“酸+碱性氧化物=盐+水”的反应,故在水溶液中发生的与之相当的反应方程式为:
2HI+PbO=PbI2+H2O
本题难度:简单
4、实验题 微型化学实验具有装置小巧,节约药品,操作简便,现象明显,安全可靠,减少污染等特点,下图是某同学设计的NH3的催化氧化并检验反应生成的酸性物质的微型装置(图中必要的铁架台、铁夹、微型酒精灯等均略去)。
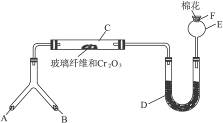
实验中所用试剂不超出下列范围:
①NH4Cl和Ca(OH)2的混合物?②4∶1氨水?③NaOH固体?④KClO3和MnO2的混合物?⑤蒸馏水⑥NH4HCO3固体?⑦6 mol・L-1 NaOH溶液?⑧0.5 mol・L-1 NaOH溶液?⑨酚酞试液?⑩碱石灰?11浓H2SO4?12CuO
试完成下列问题:
(1)微型叉形管中液态物质A是__________,固体物质B是__________。
(2)C处发生反应的化学方程式是_______________________________________。
(3)混合物D是为了检验酸性物质的生成而放入的,其组成是__________,实验过程中的现象是_______________________。
(4)E处球形玻璃管的作用是________________________________________。
(5)F处的棉花应蘸取的物质是_________________________________,其反应的化学方程式是_____________________________________________________。
参考答案:(1)4∶1的氨水(或②)? KClO3和MnO2的混合物(或④)
(2)4NH3+5O2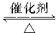 4NO+6H2O
4NO+6H2O
(3)0.5 mol・L-1 NaOH溶液和酚酞试液(或⑧和⑨)?红色褪去
(4)防止液态物质D冲出
(5)6 mol・L-1 NaOH溶液(或⑦)? NO2+NO+2NaOH====2NaNO2+H2O
本题解析:(1)因为此装置是氨的催化氧化并检验反应生成的酸性物质的微型装置,所以A和B中一个是制O2的,一个是制氨气的,根据题目提示B为固态装置,所给试剂中只有④为制氧气的药品且为固态,所以B中是KClO3和MnO2,则A为制氨气的装置。因为A为液态物质,只能选试剂中的②,即4∶1的氨水(为使NH3更易逸出,加少量NaOH固体)。
(2)玻璃纤维起增大催化剂与NH3和O2混合气体的接触面积,使反应充分的作用。
(3)为检验生成的酸性气体,需在D中加入碱液和酚酞试液,为使现象更明显,应加入0.5 mol・L-1的NaOH溶液。需在D中加入0.5 mol・L-1的NaOH溶液和酚酞试液(混合液呈红色)。
本题难度:简单
5、计算题 (9分) 在500mL? 0.2 mol・L-1的稀硝酸中加入1.92克铜片,让其充分反应。试求:
(1)产生的气体在标准状况下所占的体积为多少?
(2)反应后溶液中H+的物质的量浓度是多少?(溶液体积变化忽略不计)
(3)若要使溶液中的Cu2+全部转化为Cu(OH)2沉淀,应加入0.2 mol・L-1的氢氧化钠溶液?多少毫升?
参考答案:(1)设生成的气体是X(标准状况),则
3Cu?+? 8HNO3=3Cu(NO3)2+4H2O+2NO↑
3×64g? 8mol? 2×22.4L
1.92g? n(HNO3)? X
所以有x=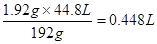
消耗硝酸n(HNO3)=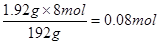
(2)原硝酸的物质的量是0.5L×0.2mol/L=0.1mol
所以剩余硝酸是0.1mol-0.08mol=0.02mol
则氢离子的浓度是0.02mol÷0.5L=0.04mol/L
(3)根据铜原子守恒可知,生成硝酸铜是1.92g÷64g/mol=0.03mol
因此反应后的溶液中含有0.02mol硝酸和0.03mol硝酸铜
所以要使溶液中的Cu2+全部转化为Cu(OH)2沉淀
需要氢氧化钠的物质的量是0.02mol+0.03mol×2=0.08mol
体积是0.08mol÷0.2mol/L=0.4L=400ml
本题解析:考查根据方程式进行的有关计算。
本题难度:一般