��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
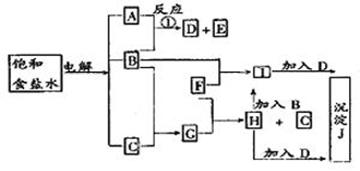
1������� ��ͼ�е�ÿһ�����ʾ�йص�һ�ַ�Ӧ�����������дֿ��ʾ��ʼ��Ӧ���Ӧʱ��������ɵ�ˮ���Լ����ɳ���Jʱ���������������ȥ����
��д���пհף�
��1������B��??��F��??��J��??��
��2����Ӧ�ٵ����ӷ���ʽ��??
�ο��𰸣�B��Cl2��F��Fe��J��Fe��OH��3
��2��Cl2��2OH�� ="===" ClO����Cl����H2O
��������������Ӧ��������˼ά���ӵ�ⱥ��ʳ��ˮ�ķ�Ӧ���֣�
2NaCl��2H2O 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
����ʾ��ͼB���ʼ�����A��Ӧ����D��E��������C��Ӧ����G���ӵ��ʳ��ˮ�IJ��������ֻ��Cl2�������ص㣬�������������ƣ�A����Ӧ����NaClO�����ɵ�H2O��ȥ��
Cl2��2NaOH=NaClO��NaCl��H2O
������������C���ڵ�ȼ����������HCl
Cl2+H2 2HCl
2HCl
�ɴ��ƶϳ�A��NaOH����B��Cl2����C��H2����G��HCl��
Ȼ����ȷ��F��F������Cl2ֱ�ӷ�Ӧ����I��������HCl��Ӧ����H��������H��Cl2�����»���ת��ΪI����FӦ���DZ�۽�������Fe������ط�Ӧ��֤��
2Fe��3Cl2 2FeCl3
2FeCl3
Fe��2HCl ="===" FeCl2��H2
2FeCl2��Cl2?="===" 2FeCl3
���˿�ͼ�еĴֶ��õ��������͡�
�����ȷ������J���ѵ㣩������ͼ��ʾ����J�ȿ���FeCl3��I����D��Ӧ�����ɣ��ֿ�����FeCl2��H����D��Ӧ�����ɣ�Jһ���Ǻ����������ʱ���ж�D��D��NaClO��NaCl�е�һ�֣���NaCl������FeCl3��FeCl2��Ӧ����J�� Dֻ���Ǵ�������NaClO��
NaClO��һ��ǿ�������Σ��� ��������ǿ�NaOH�����ᣨHClO���Σ���ˮ��ˮ����Լ��ԡ���˵�����FeCl3��Ӧʱ��ʾ�˼��ԴӶ����� Fe��OH��3����J�������������� FeCl2��Ӧʱ��ʾ�������Ժͼ��Ե�˫�����ã�Ҳ������Fe��OH��3��J������������ȷ��J�� Fe��OH��3��
��������ǿ�NaOH�����ᣨHClO���Σ���ˮ��ˮ����Լ��ԡ���˵�����FeCl3��Ӧʱ��ʾ�˼��ԴӶ����� Fe��OH��3����J�������������� FeCl2��Ӧʱ��ʾ�������Ժͼ��Ե�˫�����ã�Ҳ������Fe��OH��3��J������������ȷ��J�� Fe��OH��3��
����ӵ��ʳ��ˮ�������һ���ȵ��ʺ�����֮�����Ӧ�����磬��ν���͡����ߡ������漰��֪ʶ��㣬�������ȵ��ʡ��Ȼ���ȵĺ����������Ԫ�صı�ۡ�����������������ת�����������Ƶ������Ժ�ˮ���ԣ�������������ѧ��ѧ��Χ���ȡ���������ҪԪ�ؼ��仯����Ļ������ݡ�
���������֪ʶΪ������ؿ�����˼ά������˼ά�������������ۺϡ��Ƚ�����֤����һ�����͵����������⡣
�����Ѷȣ�һ��
2��ѡ���� ��Fe2(SO4)3��Һ�У�����a gͭ����ȫ�ܽ���ټ�b g������ַ�Ӧ��õ�c g������壬��a>c��������˵����ȷ����(? )
A�����������ͭ����
B�����õ�����Һ��һ������Cu2��
C�������������뵽ϡ�����У������ݲ���
D�����õ�����Һ�п��ܺ���Fe3��
�ο��𰸣�B
��������������a��ͭ�����ڷ��������µķ�Ӧ2Fe3����Cu��2Fe2����Cu2����ȫ���ܽ⣬����ⲿ��ͭ�ڼ���b�����ۺ�ȫ����ԭ��������cӦ��a��ȣ��������������֪a��c�����������a��ͭû��ȫ������ԭ����Һ�л���Cu2����ͬʱҲ˵����������۲��㣨����a��ͭ���ᱻȫ����ԭ�����������������������Fe2������Fe3�����ڲ����뵥��ͭ���棬˵������Һ���Ѿ����ٴ��ڣ�����������˵��c��������ͭ����Һ�л�����Cu2����Fe2����H�������������ӡ�����B��ȷ����ѡB��
������������Ҫ����ѧ���ķ����������Ѷ����С�
�����Ѷȣ�һ��
3������� ����ս̰滯ѧ1��75ҳ�ϡ����������Խ������������������ᡢ����ͭ��Һ�ȣ���Ӧת��Ϊ+2�����Ļ��������������Խ�ǿ������������������˫��ˮ�ȣ���Ӧ��ת��Ϊ+3�۵Ļ��������������ѧ�о���ѧϰС����ͨ������ʵ��̽�������ƵĻ�ԭ�����ۺ�����ķ�Ӧ���������������������̽�����ش��й����⣺
��1������KSCN��H2O2��ҩƷ���鷴Ӧ��Ļ��Һ�к��ж�������ʵ�鷽����������______������ʵ���������ֿ�����ɫѸ����ȥ��ͬʱ��Һ�ʻ�ɫ������ܵ�ԭ����______��ѧ������ʵ��ʱ�����μ�˫��ˮ��Ũ�ȹ����߹�����������Ѹ�ٲ����������ݣ�д������������Ļ�ѧ����ʽ��______��
��2�������Ͻ��ܡ�ȡ������ӦҺ�������������ȵμ��������Ʊ�����ˮ��Ȼ��μ�KSCN��Һ������Ѫ��ɫ�����ٵμӹ���������ˮ��ȴ���ֺ�ɫ��ȥ��ͬѧ�Ժ�ɫ��ȥ��ԭ��������Եļ��裮ijͬѧ�ļ����ǣ���Һ�е�+3����������Ϊ���ߵļ�̬�������+3����������ΪFeO42-����д���÷�Ӧ�����ӷ���ʽ______��
��3��̽��������ص�ij�����ʣ�
��ʵ��һ��������K2FeO4����ֱ��ܽ���pH?Ϊ?4.74��7.00��11.50?��ˮ��Һ�У����FeO42-Ũ��Ϊ?1.0mmol?L-1��1mmol?L-1=10-3mol?L-1�������������ã����첻ͬ��ʼ?pH?��ˮ��Һ��K2FeO4ij�����ʵ�Ӱ�죬�����ͼ1��ע��800min��������Һ�и�����ص�Ũ�Ȳ��ٸı䣩��


���������������?K2FeO4�ܽ���pH=4.74?��ˮ��Һ�У����Ƴ�FeO42-Ũ��Ϊ?1.0mmol?L-1?���������������ֱ�����?20�桢30�桢40���?60��ĺ���ˮԡ�У����첻ͬ�¶ȶ�K2FeO4ij�����ʵ�Ӱ�죬�����ͼ2����
��ʵ��1��Ŀ����______��
��ʵ��2�ɵó��Ľ�����______��
�۸��������ˮ�еķ�ӦΪ4FeO42-+10H2O?4Fe��OH��3+8OH-+3O2������ͼ1��֪��800minʱ��pH=11.50����Һ�и����������Ũ�ȱ�pH=4.74����Һ�иߣ���Ҫԭ����______��
�ο��𰸣���1�����������Ӿ��л�ԭ�ԣ���������KSCN��Һ��Ѫ��ɫ����KSCN��H2O2��ҩƷ���鷴Ӧ��Ļ��Һ�к��ж�������ʵ�鷽�����������ȼ����軯����Һ���������ٵμ�˫��ˮ������������Һ��Ѫ��ɫ����ʵ���������ֿ�����ɫѸ����ȥ��ͬʱ��Һ�ʻ�ɫ������ܵ�ԭ�������������������ʵ��ʱ�����μ�˫��ˮ��Ũ�ȹ����߹�����������Ѹ�ٲ����������ݣ�����2H2O2?FeCl3?.?2H2O+O2����
�ʴ�Ϊ���ȼ����軯����Һ���������ٵμ�˫��ˮ������������Һ��Ѫ��ɫ���������������2H2O2?FeCl3?.?2H2O+O2����
��2������Ϣ��֪�������ӱ���������ΪFeO42-�����ᣬ�����ӷ�ӦΪ2Fe3++3Cl2+8H2O�T2FeO42-+6Cl-+16H+��
�ʴ�Ϊ��2Fe3++3Cl2+8H2O�T2FeO42-+6Cl-+16H+��
��3������ʵ��һ��֪��pH��ͬ��FeO42-�ȶ��Բ�ͬ����ʵ��1��Ŀ��Ϊ�о�FeO42-�ڲ�ͬpH��Һ�е��ȶ��ԣ���Ӧ�����ʣ���
�ʴ�Ϊ���о�FeO42-�ڲ�ͬpH��Һ�е��ȶ��ԣ���Ӧ�����ʣ���
����ͼ2��֪���¶Ȳ�ͬ��FeO42-�ȶ��Բ�ͬ������ʵ��2�ɵó��Ľ������¶�Խ�ߣ�FeO42-Խ���ȶ�������ˮ��Ӧ������Խ�죩��
�ʴ�Ϊ���¶�Խ�ߣ�FeO42-Խ���ȶ�������ˮ��Ӧ������Խ�죩��
����ͼ1��֪��800minʱ��pH=11.50����Һ�и����������Ũ�ȱ�pH=4.74����Һ�иߣ���pH=11.50����Һ��OH-����Ũ�ȴ�ʹ4FeO42-+10H2O?4Fe��OH��3+8OH-+3O2��ƽ�������ƶ���
�ʴ�Ϊ��pH=11.50����Һ��OH-����Ũ�ȴ�ʹƽ�������ƶ���
���������
�����Ѷȣ�һ��
4��ѡ���� ij������FeCl3��Һ��ʴ����ͭ�ľ�Ե������ӡˢ��·������С��Ϊȷ��������ķ�Һ����ɣ���������ʵ�飺��1��ȡ10mL��Һ����������AgNO3��Һ�����ɳ��� 8.61g����2����ȡ10mL��Һ����ͭƬ��ַ�Ӧ��ͭƬ����������0.256g�����й���ԭ��Һ��ɵ��жϴ������
A��һ������Fe 2+��Fe 3+��Cu2+��Cl��
B��c(Fe2+)�Uc(Cu2+) = 2�U1
C��c(Fe2+)�Uc(Fe 3+) = 3�U1
D��c(Cl��) =" 6mol" / L��c(Fe 2+) =" 1.2mol" / L
�ο��𰸣�C
�������������Fe3+��Cu��Ӧ��Ļ����Һ����2Fe3+ +Cu ===2Fe2+ +Cu2+�ķ�Ӧʽ����Һ��Fe2+��Cu2+��Ũ�ȱȱ�Ϊ2:1������8.61g AgCl������10mL��Һ����0.06molCl-������֪10mL��Һ�ɷ�Ӧ��0.256g=0.004mol��Cu����֪10mL��Һ��Fe3+=0.008mol������,10mL��Һ�к���0.008molFeCl3��0.012molFe2+��0.06molCu2+��֪��C�Ǵ����. 3+�ͽ������ʵķ�Ӧ
�����Ѷȣ�һ��
5������� ij����֣���Ҫ�ɷ�ΪFe����Ʒ�к�������ͭ����ȣ������ɷֺ��ԣ���Ϊ�˲ⶨ�úϽ������ĺ���������������¹������̣�
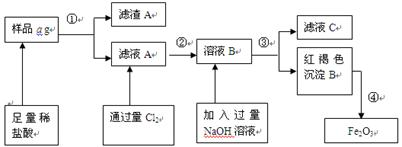
(1)ȡ��Ʒa g����ȡʱʹ�õ���Ҫ��������Ϊ_____?_______��
(2)��ҺA��������Ҫ����_______??��__? __ _��д��ѧʽ����
�����ٵ�����?����ʹ�õIJ���������______________________________��
(3)д������ҺB���ɺ��ɫ����B�����ӷ���ʽ________________________________��
(4) ������Fe2O3�������������Ϊb g���������Ʒ����Ԫ�ص������ٷ����ı���ʽΪ���ú�a��b��ʽ�ӱ�ʾ��_____________��
(5)�����֤��ҺA�к�Fe2+��������Fe3+______________________?_____________��
�ο��𰸣�(1)������ƽ
(2) FeCl2��AlCl3���� ���� ��?©�����ձ��������� ������д���÷֣�©дһ����1�֣�
(3) Fe3+ + 3OH - ="=" Fe(OH)3��
(4) (7b/10a)��100%? {��(70b/a)%}
(5)ȡ������ҺA���Թ��У��μ���KSCN��Һ����Һ����ɫ��(2��)
�ټ���ˮ����ͨ����������Һ��ΪѪ��ɫ����1�֣�?������������Ҳ���ԣ�
�����������
�����Ѷȣ�һ��