微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知NH4++AlO2-+2H2O=Al(OH)3↓+NH3?H2O,向含有等物质的量的NH4+、Al3+、H+混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应:发生反应的先后顺序正确的是( )
①H++OH-=H2O? ②Al(OH)3+OH-=AlO2-+2H2O? ③Al3++3OH-=Al(OH)3↓?④NH4++OH-=NH3?H2O.
A.①→④→③→②
B.①→③→②→④
C.①→③→④→②
D.①→②→③→④
参考答案:氢氧根离子先与氢离子反应①H++OH-=H2O,再与铝离子反应③Al3++3OH-=Al(OH)3↓,再与铵根离子反应④NH4++OH-=NH3?H2O,最后与Al(OH)3反应②Al(OH)3+OH-=AlO2-+2H2O.
故选C.
本题解析:
本题难度:简单
2、选择题 某澄清透明溶液中只可能含有:①A13+;②Mg2+;③Fe3+;④Cu2+;⑤H+;⑥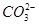 ;⑦
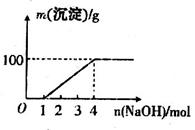
;⑦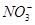 ?中的几种离子,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量如图所示。则该溶液中一定含有的离子是
?中的几种离子,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量如图所示。则该溶液中一定含有的离子是
A.②⑤⑦
B.②⑤⑥
C.③⑤⑦
D.①④⑤
参考答案:A
本题解析:0-1mol无沉淀生成,说明有H+,则无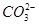 ,有
,有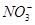 。1mol至过量,生成沉淀,且沉淀量不下降,则无A13+。故选A项。
。1mol至过量,生成沉淀,且沉淀量不下降,则无A13+。故选A项。
本题难度:一般
3、选择题 分类是化学学习中经常用到的方法,下列对一些物质或化学反应的分类以及依据正确的是
[? ]
A.H2SO4是酸,因为H2SO4中含有氢元素
B.豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间
C.Na和H2O的反应不是离子反应,因为反应中没有离子参加
D.Na在Cl2中燃烧不是氧化还原反应,因为没有得氧或失氧
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列各组离子一定能大量共存的是
A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN-
B.在强碱溶液中:Na+、K+、AlO2-、CO32-
C.在c(H+)=10-13mol/L的溶液中:NH4+、Al3+、SO42-、NO3-
D.在pH=0的溶液中:K+、Fe2+、Cl-、NO3-
参考答案:B
本题解析:分析:A.Fe3+与SCN-发生络合反应;
B.强碱溶液中存在大量的OH-;
C.c(H+)=10-13mol/L的溶液呈碱性,存在大量的OH-;
D.pH=0的溶液呈酸性,存在大量的H+.
解答:A.Fe3+与SCN-发生络合反应生成Fe(SNC)3而不能共存,故A错误;
B.强碱溶液中存在大量的OH-,离子之间不发生任何反应,可以大量共存,故B正确;
C.c(H+)=10-13mol/L的溶液呈碱性,存在大量的OH-,NH4+与OH-反应生成NH3?H2O,A13+与OH-反应生成沉淀而不能大量共存,故C错误;
D.pH=0的溶液呈酸性,存在大量的H+,Fe2+与NO3-发生氧化还原反应而不能大量共存,故D错误.
故选B.
点评:本题考查离子共存问题,题目难度中等,注意常见离子的性质,判断离子之间能否发生反应,注意题目的要求.
本题难度:简单
5、选择题 下列说法正确的是:
A.强电解质的稀溶液中不存在溶质分子
B.强电解质溶液一定比弱电解质溶液的导电性强;
C.强电解质都是离子化合物,而弱电解质都是共价化合物;
D.不同的弱电解质只要物质的量浓度相同,电离程度也相同
参考答案:A
本题解析:强电解质完全电离,所以在溶液中步存在电解质分子,选项A正确;溶液的导电性与溶液中离子浓度大小和离子所带电荷数有关系,所以选项B不正确;选项C不正确,例如氯化氢是强电解质,属于共价化合物;不同的弱电解质的电离程度是不同的,所以选项D不正确,答案选A。
本题难度:困难