��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij������Ϊ���ۺ����÷���?CaSO4�������ڵĺϳɰ�������������Ʊ���NH4��2SO4?�Ĺ�������

��ش��������⣺
��1���������з�������Ҫ��Ӧ�ǣ��û�ѧ����ʽ��ʾ��______��
��2������Һ�л�ȡ����NH4��2SO4���壬����IJ���������______����д��ţ�
A����������?B������Ũ��?C����ȴ�ᾧ?D������?E����ȡ?F��Һ
��3�������������п���ѭ��ʹ�õ�X��______��
��4���������У�Ҫ������Ͱ����Ĺܵ��Ƿ�©������ѡ��______����д��ţ�
A��Ũ����?B��ʪ�����ɫʯ����ֽ?C��ʪ��ĵ��۵⻯����ֽ?D��ϡ����?E��ʪ��ĺ�ɫʯ����ֽ��
�ο��𰸣���1����NH3��CO2ͨ��������в�����CaSO4�����ɣ�NH4��2SO4��CaCO3������CaSO4+CO2+2NH3+H2O=CaCO3��+��NH4��2SO4��
�ʴ�Ϊ��CaSO4+CO2+2NH3+H2O=CaCO3��+��NH4��2SO4��
��2������Һ�л�ȡ����Ӧ��ȡ����Ũ������ȴ�ᾧ�����˵Ȳ��������Ա������������BCD��
�ʴ�Ϊ��BCD��
��3���ɹ������̿�֪��CaCO3������¯�зֽ�����CO2��CaO��CO2ѭ��ʹ�ã�
�ʴ�Ϊ��CO2��
��4��A��Ũ����ӷ������Ȼ����백�������Ȼ�泥��а��̲��������Լ��鰱������A��ȷ��
B��������ʪ�����ɫʯ����ֽ�������������ܼ��鰱������B����
C��������ʪ��ĵ��۵⻯����ֽ�������������ܼ��鰱������C����
D��������ϡ���ᣬ�����������ܼ��鰱������D����
E�������Ǽ������壬��ʹʪ��ĺ�ɫʯ����ֽ���������Լ��鰱������E��ȷ��
��ѡ��AE��
���������
�����Ѷȣ�һ��
2��ѡ���� ��ͼ�����建��ͨ��ʢ�������Լ����Լ�ƿA�����Թ�B�п��Թ۲쵽�����������
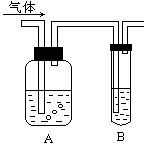
[? ]
����?
A���Լ�
B���Լ�
A.
SO2��CO2
����KMnO4��Һ
Ʒ����Һ
B.
Cl2��HCl?
Ũ����
KI������Һ
C.
NH3��CO2?
Ũ����
��̪��Һ
D.
C2H4��CH4?
����KMnO4��Һ
���CCl4��Һ
�ο��𰸣�B
���������
�����Ѷȣ���
3������� ij�о���ѧϰС���ò�����������������ΪFe2O3��Ϊԭ�ϣ������ұ���������¹������̣����ַ�Ӧ����û�б������
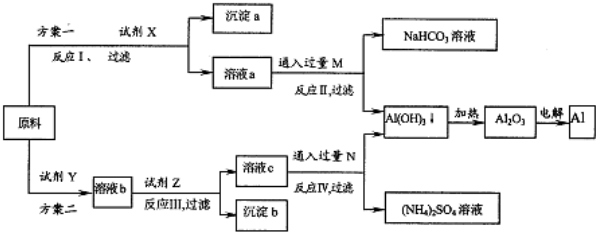
��1���Լ�X�Ļ�ѧʽΪ______����Ӧ������ӷ���ʽ��______��ʵ��������480mL?1mol?L-1?X����Һ�����õ������������ձ������������Լ�ƿ����ͷ�ι��⣬����______�����������Ա궨����X����ҺŨ���Ƿ�ȷ��ʵ��������______��
��2�����շ�����ƣ��Լ�Z�������ǵ�����Һ��pH�������ɳ���b[Fe��OH��3]�����Լ���ҵ�ĽǶȣ�����Ϊ����______��������������______��
��3����֪NΪ������ʵ�����л���������ͼװ����ȡ���������а�����Ȫʵ�飮
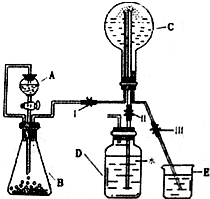
������A��������______��װ����A�ڲ���B�ڲ�֮����ͨ�����ܵ�������______��
�����ô�װ���Ʊ�N������A��ʢ��Ũ��ˮ����Bװ���еĹ����Լ�������ѡ�����е�______������ĸ��ţ���
a����ʯ��?b���ռ�?c������?d����ʯ��
��4�������£���a?mol?L-1�ģ�NH4��2SO4ˮ��Һ��pH=5��������ƽ��NH4++H2O?NH3?H2O+H+�����ƽ�ⳣ���ı���ʽΪ______���ú�����a�Ľ�Ϊ��ȷ�����ֱ���ʽ��ʾ�����ػ������������㣩��
�ο��𰸣���1������һ������Һaͨ�������M������������������̼�����ƿ�֪����Һa�к���ƫ�����������MΪ������̼�����Լ�XΪNaOH��Һ����ӦIΪ������������������Һ��Ӧ����ƫ��������ˮ�����ӷ���ʽΪ��Al2O3+2OH-�T2AlO2-+H2O��
ʵ����û��480mL����ƿ��Ӧѡ��500mL����ƿ������500mL1mol?L-1?NaOH����Һ��Ҫ���������У��ձ������������Լ�ƿ����ͷ�ιܡ�500mL����ƿ����ȱ��500mL����ƿ��
���������к͵ζ������Ա궨����NaOH��ҺŨ���Ƿ�ȷ��
�ʴ�Ϊ��NaOH��Al2O3+2OH-�T2AlO2-+H2O��500mL����ƿ���к͵ζ���
��2��������������Һcͨ�������N����������������������刺�֪����Һc�к��������ӡ�NΪ���������Լ�YΪ���ᣬ��Һb�к�����������������������PHֵ����������ת��Ϊ�������������˺�������Һ�м�������İ�ˮ���������ӣ�
�뷽��һ��Ƚϣ�����һ�����٣��������ʷ���һ��������
�ʴ�Ϊ������һ�������٣�������
��3���١�����A�Ƿ�Һ©����װ����A�ڲ���B�ڲ�֮����ͨ�����ܵ������ǣ�ƽ���Һ©������ѹǿ����ֹ��Һ©��������
�ʴ�Ϊ����Һ©����ƽ������ѹǿ����ֹ��Һ©��������
�ڡ�A��ʢ��Ũ��ˮ������ʯ�ҡ��ռ��ʯ�һ�ϣ��ų��������ȣ���Һ������������Ũ���������ð����ݳ������������İ�������ˮ�뵨����Ӧ����������ͭ���������ܲ�����������c���ܿ��ԣ�
�ʴ�Ϊ��c��
��4�������£���a?mol?L-1�ģ�NH4��2SO4ˮ��Һ��pH=5����Һ��c��H+��=10-5mol/L������Һ��c��OH-��=10-9mol/L�����ݵ���غ��У�c��NH4+��+c��H+��=c��OH-��+2c��SO42-������c��NH4+��+10-5mol/L=10-9mol/L+2amol/L����c��NH4+��=��2a+10-9-10-5��mol/L�����������غ������Һ��c��NH3?H2O��=2amol/L-��2a+10-9-10-5��mol/L=��10-5-10-9��mol/L����NH4++H2O?NH3?H2O+H+��ƽ�ⳣ���ı���ʽΪ10-5��(10-5-10-9)2a+10-9-10-5��
�ʴ�Ϊ��10-5��(10-5-10-9)2a+10-9-10-5��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ǿ�������·ֽ⣺4��NH4��2SO4=6NH3��+N2��+3SO2��+SO3��+7H2O�������ɵ�����ͨ���Ȼ�����Һ�У��õ��ij�������
A.BaSO3��BaSO4
B.BaS
C.BaSO3
D.BaSO4
�ο��𰸣�A
������������������ݷ�Ӧ���ɵIJ����������ʷ�����������������ˮ��ˮ��Ӧ���������ᣬ������������ˮ��ˮ��Ӧ�������ᣬ��������ˮ����һˮ�ϰ���������Ȼ�����Ӧ�������ᱵ������������Ͱ�ˮ��Ӧ����������泥�����ͨ���Ȼ�����Һ�У��ؼ��ֽⷴӦ���ɵ��������ʵ������м�������жϣ����ɳ����������ᱵ�����ᱵ��
��𣺷�Ӧ��Ļ������ͨ�뵽BaCL2��Һ�з������Ǹ��ֽⷴӦ
?SO2+H2O+2NH3=��NH4��2SO3
��NH4��2SO3+BaCl2=BaSO3��+2NH4Cl
SO3+H2O+2NH3 =��NH4��2SO4
��NH4��2SO4+BaCl2=BaSO4��+2NH4Cl
���ݷ�Ӧ������ϵ����Ϸֽ����ɵ��������ʵ�����֪����������ת��Ϊ������泥�1mol��������ת��Ϊ��������İ���2mol����4mol��ˮ��2mol��������Ӧ����������泥����Եõ��ij���Ϊ1mol���ᱵ��2mol�����ᱵ��ʣ���������������ᱵ��Ӧ�����������Ⱶ�����õ�����Ϊ1mol���ᱵ��1mol�����ᱵ����˵õ�����ΪBaSO3��BaSO4��
��ѡA��
���������⿼�������ʷ�Ӧ�Ķ������㼰�������ʵ��ۺ�Ӧ�ã��ؼ��Ƿ�����Ӧ���̷�Ӧ�жϳ������ɵ�ʵ�ʣ���Ŀ�Ѷ��еȣ�
�����Ѷȣ���
5��ѡ���� ������NH3ͨ��HNO3��AgNO3�Ļ����Һ�У����ɳ��������ʵ���(n)��ͨ��NH3�����(V)��ϵ(��ͼ��ʾ)��ȷ����
[? ]
A.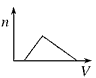
B.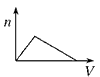
C.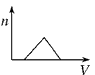
D.
�ο��𰸣�A
���������
�����Ѷȣ���