��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��12�֣�����ѧ����ѧ�뼼����
��������ҵ���������ɡ���������ȡ������ұ�������ļӹ��Ȼ��ڹ��ɡ�

��1����ҵ�ϲ��õ���������ͱ���ʯ(Na3AlF6)������ķ���ұ���õ���������2Al2O3 4Al��3O2����
4Al��3O2����
�������ʯ������Ϊ_______________________��
��2��������������������������������Fe��Si�����ʣ����õ�ⷽ����һ���ᴿ���õ����������ĵ缫��ӦʽΪ________�����п����������ϵ���______��
a������ b��ʯī c��Ǧ�� d������
��3������������ʹ���������������ܵ�����Ĥ����ϡ����Ϊ���Һ�������������ĵ缫��Ӧʽ_______________________�������������������У���Ҫ���ϵص�����ѹ��������_________________��
��4������˵����ȷ����__________________��
a������������Ӧ��ԭ���ԭ�����н������ϱ��洦���ļ���
b������������������ǿ������ľ�Ե����
c������������������߽���������Ͻ����ʴ�ԣ�����ĥ���½�
d��������������Ĥ������ԣ����к�ǿ���������ܣ�������Ⱦ�϶��ʸ�����ɫ
�ο��𰸣���1����Ҫ�ǽ���Al2O3���ۻ��¶� ��2�֣� ��2��Al��3e��=Al3����2�֣� d��2�֣� ��3��2Al ��6e����3H2O=Al2O3��6H����2�֣����������治�������������������Ϊ���ֵ����ȶ����費�������ѹ��2�֣���4��bd��2�֣�
�����������1��Al2O3���۵�ϸߣ�Ϊ�˽����ܺļ������ʯ�����ۼ������Ա���ʯ����Ҫ�����ǽ���Al2O3���ۻ��¶ȡ���2����������������Ӧ�����õĽ����ȷŵ磬Al �ϻ�������Al �ȷŵ磬�缫��ӦΪ��Al��3e��=Al3�������ڸù������ᴿAl������Ϊ�˼����������������ô�����ѡd����3��������Ϣ������������ʹ���������������ܵ�����Ĥ��֪����Al ��Ӧ������Al2O3����缫��ӦΪ��2Al ��6e����3H2O
�����Ѷȣ�����
2������� ��12�֣�6�����ڶ���������Ԫ�ص����λ�����±���MԪ��ԭ�Ӻ����������YԪ��ԭ�Ӻ����������2����WԪ��ԭ�ӵĴ�����������������������2�����û�ѧ����ش��������⣺
��1��Y�����ڱ��е�λ����________��
��2��X��Y��Z����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳����________��
��3��W��M��Q����Ԫ������������Ӧ��ˮ�����У�������ǿ������˳����________��
��4��W�������������Ժ�Z���⻯�ﷴӦ�����ø÷�Ӧ�ɿ�ʴ��������Ӧ�Ļ�ѧ����ʽ��________��
��5��X�ĺ�10�����ӵ���̬�⻯�����һ����Ҫ�Ļ���ԭ�ϡ��ĵ���ʽ�� ��ʵ�����Ʊ��Ļ�ѧ����ʽ��________��������X������������Ӧ��ˮ������Һ��Ӧ�������ң�����Һ�е�����Ũ���ɴ�С��˳���� ��X�ĺ�18�����ӵ���̬�⻯��������������һ�ֻ����ͼ���ȼ�ϵ�أ���ع���ʱ�������ĵ缫��Ӧ����ʽ�� ��
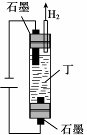
��6����ҵ������ͼ��ʾװ�õ��QԪ�ص�������Һ�������һ�ֺ�QԪ�ص����������÷�Ӧ�����ӷ���ʽ�� ��
�ο��𰸣���12�֣�
��1�������ڢ�A�壨1�֣�
��2��r(N)>r(O)>r(F)��1�֣�
��3��HClO4>H2SO4>H2SiO3��1�֣�
��4��SiO2+4HF===SiF4+2H2O��1�֣�
��5��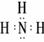 ��1�֣�,2NH4Cl+Ca(OH)2
��1�֣�,2NH4Cl+Ca(OH)2  CaCl2+2NH3��+2H2O��2�֣�
CaCl2+2NH3��+2H2O��2�֣�
c(NO3-)>c(NH4+)>c(H+)>c(OH-)��1�֣�
N2H4-4e-+4OH-===N2+4H2O��2�֣�
��6��Cl-+H2O ClO-+H2����2�֣�
ClO-+H2����2�֣�
���������XΪ����YΪ����Z����WΪ�裬MΪ��QΪ�ȡ���1����Ԫ���ڵڶ����ڢ�A�塣��2��ͬ����Ԫ��ԭ�Ӱ뾶�����Ҽ�С�����뾶˳��Ϊ��r(N)>r(O)>r(F)����3���ǽ�����Խǿ��������������Ӧ��ˮ��������Խǿ��ͬ����Ԫ�ش����ҷǽ�������ǿ������������ǿ��˳��Ϊ��HClO4>H2SO4>H2SiO3����4���������������ᷴӦ�����ķ������ˮ������ʽΪ��SiO2+4HF===SiF4+2H2O����5�������⻯��Ϊ����������ʽΪ�� ,ʵ�������Ȼ�狀��������Ʒ�Ӧ��ȡ������ʽΪ��2NH4Cl+Ca(OH)2
,ʵ�������Ȼ�狀��������Ʒ�Ӧ��ȡ������ʽΪ��2NH4Cl+Ca(OH)2 CaCl2+2NH3��+2H2O�����������ᷴӦ��������泥�����笠�����ˮ�⣬��Һ�Լ��ԣ���������˳��Ϊ��c(NO3-)>c(NH4+)>c(H+)>c(OH-)������18�����⻯��ΪN2H4����ԭ�����ʧȥ������������Ⱦ�ĵ������缫��ӦΪ��N2H4-4e-+4OH-===N2+4H2O����6������Ȼ�����Һ���������ɵ����������ɵ��������Ʒ�Ӧ���������Ȼ��ƺʹ������ƣ����Ե��Ľ��Ϊ��Cl-+H2O
CaCl2+2NH3��+2H2O�����������ᷴӦ��������泥�����笠�����ˮ�⣬��Һ�Լ��ԣ���������˳��Ϊ��c(NO3-)>c(NH4+)>c(H+)>c(OH-)������18�����⻯��ΪN2H4����ԭ�����ʧȥ������������Ⱦ�ĵ������缫��ӦΪ��N2H4-4e-+4OH-===N2+4H2O����6������Ȼ�����Һ���������ɵ����������ɵ��������Ʒ�Ӧ���������Ȼ��ƺʹ������ƣ����Ե��Ľ��Ϊ��Cl-+H2O ClO-+H2����
ClO-+H2����
���㣺Ԫ�����ڱ����ƶϣ�Ԫ�������ɣ�ʵ������ȡ���������ԭ����Ӧ��
�����Ѷȣ�����
3������� ��������(NaClO2)��һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ���ҵ�������NaClO2����Ҫ�������£�

��1��A�Ļ�ѧʽ�� ��װ��III��A�� ����������
��2��II�з�Ӧ�����ӷ���ʽ�� ��
��3��ͨ����ǰ������III�������ӵķ����Ͳ����� ��
��4��Ϊ��ֹII���Ʊ���NaClO2����ԭ��NaCl��Ӧѡ���ʵĻ�ԭ������˫��ˮ�⣬������ѡ��Ļ�ԭ���� (����ĸ���)��
a��Na2O2 b��FeCl2 c��Na2S
��5������ʱ��HClO2�ĵ���ƽ�ⳣ��Ka=1��07 10-2mol��L-1��II�з�Ӧ����NaClO2��Һ(������NaOH)��pH=13������Һ��
10-2mol��L-1��II�з�Ӧ����NaClO2��Һ(������NaOH)��pH=13������Һ�� = ��
= ��
��6������a��b������������Һ�ɹ���ȼ�ϵ�أ��øõ�ص��200 mL 0��5 mol��L-1��CuSO4��Һ������ͭ3��2 g����ʱ������Һ������Ũ���ɴ�С��˳����
�ο��𰸣���1��H2SO4 ��2�֣� ����2�֣�
��2��2ClO2��H2O2��2OH����2ClO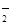 ��O2����2H2O ��3�֣�
��O2����2H2O ��3�֣�
��3��ȡ����������Һ�������Թ��У��ȼ�������ϡ���ᣬ�������ɣ��ټ���BaCl2��
Һ��������ɫ������֤������SO42�� ��3�֣�
��4��a��2�֣�
��5��1.07��1010mol��L��1 ��3�֣�
��6��c(H��)��c(SO42��)��c(Cu2��)��c(OH��) ��3�֣�
���������
��1����Ϊ�����������Һ�������ǵ��ˮ������2H++2e-=H2��������4OH--4e-=O2��+2H2O����һ�缫����NaOH����Ϊ�õ���Ϊ���Ӹ�Ĥ���أ�����AΪ���ᣬ��������������
��2�������з�Ӧ����������Ϣ��֪������NaClO2������һ����ClO2��NaClO2�����ϼ۽��ͣ�����ԭ����H2O2�ض�����������������������Ӧ��ClO2����������������ԭ��Ӧ��HCl�ǻ�ԭ��������������Ӧ�����ݵ���ת���غ��֪4n��ClO2��=n��HCl�������Է�Ӧ����ʽΪ��2NaOH+2ClO2+H2O2=2 NaClO2+2H2O+O2�������ӷ���ʽ��2ClO2+H2O2+2OH-=2ClO2-+O2��+2H2O��
��3��III��������ΪSO42?�����鷽��Ϊ��ȡ����������Һ�������Թ��У��ȼ�������ϡ���ᣬ�������ɣ��ټ���BaCl2��Һ��������ɫ������֤������SO42��
��4������FeCl2��Na2S��������ʣ���Na2O2��������µ����ʣ���a����ȷ��
��5��II�з�Ӧ����NaClO2��Һ(������NaOH)��pH=13���ɵ�c(H+)=1��10-13mol?L?1���� =
= =1.07��1010mol��L��1 ��
=1.07��1010mol��L��1 ��
��6���������ͭ��Һ�Ļ�ѧ����ʽΪ��2CuSO4+2H2O 2H2SO4+2Cu+O2��������ͭ3��2 g����Ӧ��CuSO4�����ʵ���Ϊ0.05mol������H2SO4�����ʵ���Ϊ0.05mol����������Һ��0.05mol��CuSO4��0.05mol��H2SO4��Cu2+ˮ������H+,��������Ũ���ɴ�С��˳��Ϊ��c(H��)��c(SO42��)��c(Cu2��)��c(OH��)��
2H2SO4+2Cu+O2��������ͭ3��2 g����Ӧ��CuSO4�����ʵ���Ϊ0.05mol������H2SO4�����ʵ���Ϊ0.05mol����������Һ��0.05mol��CuSO4��0.05mol��H2SO4��Cu2+ˮ������H+,��������Ũ���ɴ�С��˳��Ϊ��c(H��)��c(SO42��)��c(Cu2��)��c(OH��)��
�����Ѷȣ�һ��
4������� ͼΪ������ļס��������أ��Իش�

��1�����������õ��ԭ�������϶�������A��?����缫���ϣ����缫��Ӧʽ?��B��Ҫ��ͬA����?���缫��Ӧʽ?��Ӧѡ�õĵ������Һ��?��
��2���ҵ�����������������̪��Һ����ʼ���һ��ʱ�䣬����������?��C��������?��
��3����������������4.32g�����Ҳ��������Ϸų��������ڱ�״���µ������?��
��4�����ҵ�����ʣ����Һ��Ϊ400mL�������������Һ�����������ʵ����ʵ���Ũ��Ϊ?mol?L-1����Һ��pH����?��
�ο��𰸣���1������������Ag++e-�TAg������������Ag-e-�TAg+�� ��������Һ��
��2���죻dz����
��3��448mL
��4��0.1mol/L��13
�����������1���׳��ǵ�Ƴأ��������������������������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪAg++e-�TAg����������ʧ���ӷ���������Ӧ���缫��ӦʽΪAg-e-�TAg+���������ҺΪ�����Ե���������Һ��
��2�����ǵ��أ�̼�缫�������ӷŵ��������������缫�������ӷŵ�����������ͬʱ��Һ���������������ӣ��������缫������Һ�ʼ��ԣ���̪�Լ�������ɫ���������缫������Һ���ɫ��̼�缫������������������dz����ɫ���壬����ˮ��ʹ��Һ��dz����ɫ������C�缫������dz����ɫ��
��3���׳�������������������������������4.32g��ת�Ƶ��ӵ����ʵ���=4.32g��108g/mol=0.04mol���ҳ�����������������������1mol����ת�Ƶ��ӵ����ʵ�����2mol����ת��0.04mol����ʱ�������������ʵ���Ϊ0.02mol�����������=0.02mol��22.4L/mol=0.224L=448mL��
��4���ҳ��е�ط�ӦʽΪ2NaCl+2H2O H2��+Cl2��+2NaOH�������������������ƵĹ�ϵʽ֪������0.02mol����ʱͬʱ����0.04mol�������ƣ����������Ƶ����ʵ���Ũ��=0.04mol��0.4L=0.1mol/L������Һ��������Ũ��=10?14/0.1
H2��+Cl2��+2NaOH�������������������ƵĹ�ϵʽ֪������0.02mol����ʱͬʱ����0.04mol�������ƣ����������Ƶ����ʵ���Ũ��=0.04mol��0.4L=0.1mol/L������Һ��������Ũ��=10?14/0.1
mol/L=10-13 mol/L��������pH=13��
�����Ѷȣ�һ��
5��ѡ���� �ö��Ե缫���2L�����Ȼ�����Һ,����һ��ʱ���Ժ�,���Һ��pH������13
��Kw=10-14������������������Ϲ������������ڱ�״�������Ϊ
A��2.24L����
B��4.48L
C��1.12L����
D��11.2L
�ο��𰸣�B
�����������Һ��pH��13��˵����Һ��OH����Ũ����0.1mol/L�������������Ƶ����ʵ�����0.2mol�������2NaCl��2H2O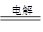 2NaOH��Cl2����H2����֪�����������������ʵ�������0.1mol�����Դ�ѡB��
2NaOH��Cl2����H2����֪�����������������ʵ�������0.1mol�����Դ�ѡB��
�����Ѷȣ�һ��