��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ϳɰ���ӦN2��g��+3H2��g�� 2NH3��g������Ӧ���̵������仯��ͼ��ʾ����֪N2��g����H2��g����Ӧ����17 g NH3��g�����ų�46.1 kJ��������
2NH3��g������Ӧ���̵������仯��ͼ��ʾ����֪N2��g����H2��g����Ӧ����17 g NH3��g�����ų�46.1 kJ��������
��ش��������⣺
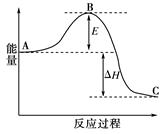
(1)�÷�Ӧͨ���������������Ӵ�����ʹͼ��E��_____�����С������E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ������Ӱ�죿_ _��������_________ ��
(2)ͼ�Ц�H��________kJ��mol��1��
(3)��ʼ����2mol��L��1 N2��5.5 mol��L��1 H2������50 min��NH3��Ũ��Ϊ1mol��L��1��
��v(N2)��____________mol��L��1��min��1��C(H2)��______________mol��L��1��
��֪NH3��g��= NH3 (l) ��H=��QkJ��mol-1����дN2��g��+3H2��g��=2NH3 (l)���Ȼ�ѧ����ʽ ________ ��
�ο��𰸣���1��С���ޡ���Hȡ���ڷ�Ӧ�������������������������(2)-92.2 ��3��0.01 4
��4��N2(g) + 3H2(g) ? 2NH3(g) ��H=-��92.2+Q��kJ��mol-1
�����������1���������������Խ��ͷ�Ӧ���E�����ԼӴ�����ʹͼ��E���С����Hȡ���ڷ�Ӧ�����������������������������E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ��û��Ӱ�졣
��2��NH3�����ʵ���Ϊ17g/17g��mol-1="1mol" ��H="2��-46.1" kJ="-92.2" kJ(�÷�ӦΪ���ȷ�Ӧ������Ϊ��)
��3��NH3�ı仯Ũ��Ϊ1mol��L��1ʱ�����ݷ�Ӧ�ȣ�N2��Ũ�ȱ仯��0.5mol��L��1��v(N2)��0.5mol��L��1/50 min="0.01" mol��L��1��NH3�ı仯Ũ��Ϊ1mol��L��1ʱ�����ݷ�Ӧ�ȣ�H2��Ũ�ȱ仯��1.5 mol��L��1��C(H2)��5.5 mol��L��1-1.5 mol��L��1="4" mol��L��1
��4��N2(g) + 3H2(g) ? 2NH3(g) ��H=-��92.2+Q��kJ��mol-1
���㣺�������ؿ����˻�ѧ��Ӧ�ȡ���ѧ��Ӧ���ʼ�������֪ʶ��
�����Ѷȣ�һ��
2������� (8��)�״���һ������ȼ�ϣ�������ȼ�ϵ�ء�

��1����ҵ�Ͽ����������ַ�Ӧ�Ʊ��״���
��CO(g) + 2H2(g)  CH3OH(g) ��H1 ��CO2(g)��3H2(g)
CH3OH(g) ��H1 ��CO2(g)��3H2(g) CH3OH(g) + H2O(g) ��H2
CH3OH(g) + H2O(g) ��H2
��֪����2H2(g)+ O2(g) �� 2H2O(g) ��H3����2CO(g)��O2(g)��2CO2(g) �ķ�Ӧ��
��H��______���æ�H1����H2����H3��ʾ����
��2�������״���ԭ��CO��H2��Դ�ڣ�CH4(g) + H2O(g)  CO(g) + 3H2(g) ��H4��
CO(g) + 3H2(g) ��H4��
һ��������CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼa����H4______0��P1_________P2
���<������>��������
ijʵ��С�������ͼb��ʾ�ļ״�ȼ�ϵ��װ�ã�����һ��ʱ�����Һ��PH (������ ��С������)�������ĵ缫��ӦʽΪ_______ ____��

��4����ͭ��������õ��Ĵ�ͭ������Fe��Ag��Au�Ƚ������ʣ����һ�����õ�ⷨ���ơ���ͭ���õ���ͭ�ĵĵ����У����������� ������������ ��������Ϊ��
�ο��𰸣���1��2��H1-2��H2+��H3�� ��2��>��<��
��3����С CH3OH-6e-+8OH-=CO32-+6H2O��4����ͭ����ͭ��Ag��Au
�����������1���١�2���ڡ�2+�ۣ������ɵ�2CO(g)��O2(g)��2CO2(g) ��H��2��H1-2��H2+��H3����20���������¶ȣ�CH4��ƽ��ת����������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ�����������Ӧ���������ȷ�Ӧ����H4>0;����ѹǿ��ƽ�������ƶ���CH4��ƽ��ת���ʽ��͡�����ͼʾ��֪P1<P2��3��ijʵ��С�������ͼb��ʾ�ļ״�ȼ�ϵ��װ�ã�����ԭ����2CH3OH+3O2+4KOH=2K2CO3+6H2O,�ɼ�����һ��ʱ�����Һ��pH��С�������ĵ缫��ӦʽΪCH3OH-6e-+8OH-=CO32-+6H2O����4����ͭ��������õ��Ĵ�ͭ������Fe��Ag��Au�Ƚ������ʣ����һ�����õ�ⷨ���ơ���ͭ���õ���ͭ�ĵĵ����У����������Ǵ�ͭ�����������Ǿ�ͭ����������Cu����Ա�Cuǿ�Ľ���Fe��ʧȥ���ӣ���Ϊ���������ӽ�����Һ������Ա�Cu���Ľ���Ag��Au�Ⱦͳ����������ײ㣬�׳������࣬����������ΪAg��Au��
���㣺�����˹���ɵ�Ӧ�á��¶ȡ�ѹǿ������ת���ʵ�Ӱ�졢ȼ�ϵ�صĸ���ԭ������Ƶ�֪ʶ��
�����Ѷȣ�����
3������� 2013�꣬���ӡ����ð�Сʱ���ع��˲���ҩ���ù�ҵ���Ѭ��ɽ�����Լ�û�й�Ч��ɽ����������ҩ�����а�����ҩ��������ҩ��������άC����Ƭ��άC����Ƭ���ع⡰������ҩ��ҩ��ҵ�����˾��ӣ��ں��º��������£�����Է�������ת�����䷴Ӧ���̺�������ϵ��ͼ1��ʾ������֪��2SO2��g��+O2��g��?2SO3��g������H=-196.6KJ/mol��

��ش��������⣺
��1��д���ܱ�ʾ�������ȼ���ȵ��Ȼ�ѧ����ʽ��______��
��2�����º���ʱ��lmol SO2��2mol O2��ַ�Ӧ���ų���������ֵ��|��H2|______�������С������ȡ���
��3�������еĻ������ͨ��������NaOH��Һ������NaOH�����ʵ���Ϊ______������Һ�з�����������ԭ��Ӧ����ù��̵����ӷ���ʽΪ______��
��4��ijSO2��g����O2��g����ϵ��ʱ��t1�ﵽƽ��ı�ijһ�����������Ӧ����v��ʱ��t�Ĺ�ϵ��ͼ2��ʾ�������ı�SO2��g����O2��g����������ͼ��t4ʱ����ƽ���ƶ�������������______��ͼ�б�ʾƽ��������SO3�İٷֺ�����ߵ�һ��ʱ����______��
��5������ƽ��ʱ��Ӧ��ƽ�ⳣ�����±���ʾ��
| t1-t2 | t3-t4 | t5-t6 | t6-t7
K1
K2
K3
K4
|
K1��K2��K3��K4֮��Ĺ�ϵΪ______��
�ο��𰸣���1��ȼ������ָ1mol��ȼ����ȫȼ�������ȶ���������ų������������ԣ�������ʵ���Ϊ1mol����ͼ1��֪1molS��s����ȫȼ�շų�������Ϊ297KJ�����ԣ����ȼ���ȵ��Ȼ�ѧ����ʽS��s��+O2��g���TSO2��g����H=-297 KJ?mol-1��
�ʴ�Ϊ��S��s��+O2��g���TSO2��g����H=-297 KJ?mol-1��
��2�����º���ʱ����ʼΪ1molSO2��2molO2 �뿪ʼΪ1molSO2��1molO2 ��ȣ�����������Ũ�ȣ�ƽ�������ƶ������Կ�ʼΪ1molSO2��2molO2 ��SO2ת���ʸߣ��ų���������ֵ��|��H2|��
�ʴ�Ϊ����
��3����Ӧ���õ������ƣ�������ԭ�ӡ���ԭ��ԭ���غ㣬n��NaOH��=2n��S��=2����0.2+0.8��mol=2mol��
������������ԭ��Ӧ������SO2��O2���������ӷ���ʽΪ2SO2+O2+4OH-�T2SO42-+2H2O��
�ʴ�Ϊ��2mol��2SO2+O2+4OH-�T2SO42-+2H2O��
��4��t2��t3���������ʶ��ӿ죬��v��������v���棩��ƽ�������ƶ���t4��t5���������ʶ��ӿ죬��v��������v���棩��ƽ�������ƶ����÷�ӦΪ�����С�ķ��ȷ�Ӧ���������¶ȣ�ƽ�������ƶ���������ѹǿ��ƽ�������ƶ�������t2��t3��Ϊ����ѹǿ��t4��t5��Ϊ�����¶ȣ�t2��t3��Ϊ����ѹǿ��ƽ�������ƶ���SO3�ĺ������ߣ���t3��t4ƽ��ʱ��������ߣ�
�ʴ�Ϊ�������¶ȣ�t3��t4��
��5���ɣ�4���ķ�����֪t2��t3��Ϊ����ѹǿ����K2=K1��t4��t5��Ϊ�����¶ȣ���K3��K2������K4=K3��K2=K1��
�ʴ�Ϊ��K4=K3��K2=K1��
���������
�����Ѷȣ���
4��ѡ���� �����Ȼ�ѧ����ʽ��ȷ���� �� ��
A�������ȼ����Ϊ890.3 kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ
CH4(g)��2O2(g)===CO2(g)��2H2O(g)����H����890.3 kJ��mol-1
B��500 �桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱ������г�ַ�Ӧ����NH3(g)������19.3 kJ�����Ȼ�ѧ����ʽΪN2(g)��3H2(g)  2NH3(g)����H����38.6 kJ��mol-1
2NH3(g)����H����38.6 kJ��mol-1
C����֪��101 kPa�£�1 g H2ȼ������ˮ�����ų�121 kJ���������Ȼ�ѧ����ʽΪ
H2(g)��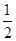 O2(g)===H2O(g)����H����242 kJ��mol-1
O2(g)===H2O(g)����H����242 kJ��mol-1
D��25 �棬101 kPaʱ��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ���к���Ϊ57.3 kJ��mol-1��������Һ������������Һ��Ӧ���к��ȵ��Ȼ�ѧ����ʽΪ