微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (3分)把 3mol A 和 2.5mol B 混合于 2L 的密闭容器中,使它们发生反应:
3A(气) + B(气) 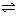 xC(气) + 2D(气)
xC(气) + 2D(气)
经5min后达到平衡生成1mol D,并测定C的平均速率为0.1 mol/L・min,则此反应中的B的转化率为________,C的系数为_______________,A的平衡浓度为_____________。
20%,2,? 0.75 mol /L
参考答案:
本题解析:3A?+ ?B ? xC? + ?2D
? xC? + ?2D
始n:? 3mol ?2.5mol ?0? 0
△n:?1.5mol?0.5mol?1mol? 1mol
平n:1.5mol?2mol?0.1×2×5?1mol
本题难度:一般
2、选择题 二氧化氮存在下列平衡:2NO2 ?N2O4?ΔH<0,在测定NO2的相对分子质量时,下列条件中较为适宜的是
?N2O4?ΔH<0,在测定NO2的相对分子质量时,下列条件中较为适宜的是
A.温度130 ℃、压强 3.03×105 Pa
B.温度130 ℃、压强5.05×104 Pa
C.温度25 ℃、压强1.01×105 Pa
D.温度0 ℃、压强5.05×104 Pa
参考答案:B
本题解析:测定NO2相对分子质量,应使平衡向逆反应方向移动,所以应选择高温、低压。
点评:根据题设考虑化学反应条件的控制。
本题难度:一般
3、选择题 温度为500℃时,反应4NH3+5O2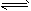 4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量浓度增加了0.3mol,则此反应的平均速率
4NO+6H2O在5L的密闭容器中进行,半分钟后NO的物质的量浓度增加了0.3mol,则此反应的平均速率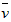 (x)为
(x)为
[? ]
A.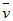 (O2)=0.01mol/(L・s)
(O2)=0.01mol/(L・s)
B.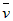 (NO)=0.08mol/(L・s)
(NO)=0.08mol/(L・s)
C.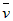 (H2O)=0.003mol/(L・s)
(H2O)=0.003mol/(L・s)
D.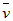 (NH3)=0.02mol/(L・s)
(NH3)=0.02mol/(L・s)
参考答案:C
本题解析:
本题难度:简单
4、填空题 (1)把a、b、c、d 四块金属片浸入稀H2SO4中,分别用导线两两相连可以组成原电池。a、b相连时,导线上电子由 a→b;c、d相连时,电流由 d→c; a、 c相连时 c极上产生大量气泡; b、 d相连时,d极发生氧化反应。这4种金属的活动性由强到弱的顺序是_______________
(2)王同学想在钥匙上镀上一层铜,设计电解实验时,钥匙应和电源的?极相连。
(3)碳作阳极,铜作阴极电解MgCl2溶液的离子方程式:?
碳作阴极,铜作阳极电解硫酸钠溶液的化学方程式:?
(4)用惰性电极电解饱和食盐水,当电源供给0.2mol电子时,停止通电。若此时溶液体积为2L,则所得电解液的pH是?。(不考虑气体的溶解)
(5)将含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1 L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,则另一个极上放出气体(标准状况下)为?L。
参考答案:(1)(2分)a>c>d>b?(2)(1分)负?
(3)(每空2分)Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑?
Mg(OH)2↓+H2↑+Cl2↑?
Cu+H2O Cu(OH)2+H2↑
Cu(OH)2+H2↑
(4)(2分)13
(5)(2分)5.6L
本题解析:(1)a、b相连时,导线上电子由 a→b,说明a比b活泼;c、d相连时,电流由 d→c,说明c比d活泼; a、 c相连时 c极上产生大量气泡,说明a比c活泼; b、d相连时,d极发生氧化反应,说明d比b活泼,故这4种金属的活动性由强到弱的顺序是a>c>d>b;(2)王同学想在钥匙上镀上一层铜,根据电解池的原理,钥匙应该作为电解池的阴极,阴极接电源的负极;3)碳作阳极,铜作阴极电解MgCl2溶液的离子方程式为:Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑,碳作阴极,铜作阳极电解硫酸钠溶液的化学方程式:Cu+H2O
Mg(OH)2↓+H2↑+Cl2↑,碳作阴极,铜作阳极电解硫酸钠溶液的化学方程式:Cu+H2O Cu(OH)2+H2↑;(4)用惰性电极电解饱和食盐水的反应式为:2NaCl+2H2O=Cl2↑+H2↑+2NaOH,该反应转移的电子数为2,所以当电源供给0.2mol电子时,生成的0.2molNaOH,即c(OH-)=0.2/2=0.1mol/L,c(H+)=10―13mol・L-1,所以pH=-lgc(H+)=13;(5)含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1 L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,电解该溶液时,在阴极上析出铜离子,在阳极是首先是氯离子放电,生产了氯气,接下来是氢氧根放电生产氧气,其电极方程式为:2Cl--2e-=Cl2↑,4OH--4e-=2H2O+O2↑,一个极析出0.3mol红色物质,即转移的电子数为0.6mol,所以生成了0.4/2=0.2mol的氯气和(0.6-0.4)/4=0.05mol的氧气,所以另一个极上放出气体(标准状况下)为(0.2+0.05)×22.4=5.6L。
Cu(OH)2+H2↑;(4)用惰性电极电解饱和食盐水的反应式为:2NaCl+2H2O=Cl2↑+H2↑+2NaOH,该反应转移的电子数为2,所以当电源供给0.2mol电子时,生成的0.2molNaOH,即c(OH-)=0.2/2=0.1mol/L,c(H+)=10―13mol・L-1,所以pH=-lgc(H+)=13;(5)含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1 L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,电解该溶液时,在阴极上析出铜离子,在阳极是首先是氯离子放电,生产了氯气,接下来是氢氧根放电生产氧气,其电极方程式为:2Cl--2e-=Cl2↑,4OH--4e-=2H2O+O2↑,一个极析出0.3mol红色物质,即转移的电子数为0.6mol,所以生成了0.4/2=0.2mol的氯气和(0.6-0.4)/4=0.05mol的氧气,所以另一个极上放出气体(标准状况下)为(0.2+0.05)×22.4=5.6L。
点评:本题考查了原电池、电解池、pH的计算,这些知识点为高考考查的重点,本题有一定的综合性,该题难度适中。
本题难度:一般
5、选择题 在2L密闭容器中,一定条件下发生反应A+3B==2C,在10秒内反应物A的浓度由1mol/L降到0.6mol/L,则用A浓度的变化表示的该反应在这段时间内的平均反应速率为
[? ]
A.0.04mol/(L・s)
B.0.02mol/(L・s)
C.0.4mol/(L・s)
D.0.2mol/(L・s)
参考答案:A
本题解析:
本题难度:简单