微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 用含有A12O3、SiO2和少量FeO・xFe2O3的铝灰制备A12(SO4)3・18H2O。工艺流程如下:
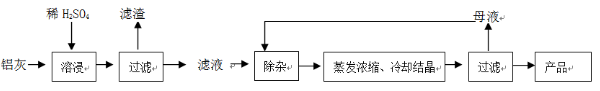 ?
?
(一定条件下,MnO4- 可与Mn2+反应生成MnO2)
已知: 生成氢氧化物沉淀的pH
?
| Al(OH)3
| Fe(OH)2
| Fe(OH)3
|
开始沉淀时
| 3.4
| 6.3
| 2.7
|
完全沉淀时
| 5.2
| 9.7
| 3.2
|
(1)H2SO4溶解A12O3的离子方程式是?;
(2)检验滤液中还存在Fe2+的方法是?(注明试剂、现象)。
(3)“除杂”环节有如下几个步骤:
(Ⅰ)向滤液中加入过量KMnO4溶液,调节溶液的pH为3.2;
(Ⅱ)加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
(Ⅲ)加入MnSO4至紫红色消失,过滤。
①步骤Ⅰ的目的?;调节溶液的pH为3.2的目的是?。
②向Ⅱ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是?,写出其反应方程式?;
③Ⅲ中加入MnSO4的目的是?。
(4)从多次循环使用后母液中可回收的主要物质是?(填化学式)。
参考答案:(1)Al2O3+6H+=2Al3++3H2O
(2)取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色
(3)①将Fe2+氧化为Fe3+;调节pH值使铁完全沉淀;
②有黄绿色气体生成;MnO2+4HCl ?MnCl2+ Cl2↑+2H2O
?MnCl2+ Cl2↑+2H2O
③除去过量的MnO4-。
(4)K2SO4。
本题解析:(1)硫酸溶解氧化铝生成硫酸铝和水,反应的离子方程式为:Al2O3+6H+=2Al3++3H2O;
(2)取少量滤液,滴加KMnO4溶液,KMnO4溶液褪色。
(3)①将Fe2+氧化为Fe3+,调节pH值使铁完全沉淀;
②加入浓盐酸与MnO2反应生成有黄绿色气体;MnO2+4HCl= MnCl2+ Cl2↑+2H2O
③MnO4-可与Mn2+反应生成MnO2,过滤除去,所以可以利用MnSO4的溶液和高锰酸钾溶液反应生成二氧化锰,把过量高锰酸根离子除去。
(4)多次循环的物质是K2SO4。
本题难度:一般
2、选择题 蛇纹石矿可看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制碱式碳酸镁的实验步骤如下:?
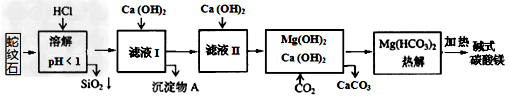
室温下,相关金属氢氧化物沉淀的KSP见下表1
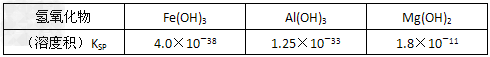
注:①?lg2=0.3,②离子的浓度小于1.0×10-5?mol・L-1时?,可认为该离子沉淀完全。下列说法不正确的是
[? ?]
A.在滤液I中,不能加过量的Ca(OH)2是为了防止Al(OH)3溶解和Mg2+沉淀
B.滤液I中,加Ca(OH)2后Al3+比Fe3+先沉淀完全
C.室温下,用Ca(OH)2把滤液I的pH调节到4.7时,Al3+刚好沉淀完全
D.称18.2g碱式碳酸镁【aMgCO3・b?Mg(OH)2・cH2O】高温加热分解得到6.6g?CO2和8.0g?MgO,由此可知a=3、b=1、c=3
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列物质之间的转化都能一步能实现的是
[? ]
A.Si→SiO2→H2SiO3→Na2SiO3
B.Al→Al2O3→Al(OH)3→NaAlO2
C.N2→NH3→NO→NO2→HNO3→NO2
D.S→SO3→H2SO4→SO2→Na2SO3→Na2SO4
参考答案:C
本题解析:
本题难度:简单
4、选择题 向明矾[KAl(SO4)2.12H2O]溶液中加入Ba(OH)2溶液,当SO42- 恰好沉淀完全时,这时铝元素的存在形式是
A.Al(OH)3沉淀
B.只有AlO2- 离子
C.Al(OH)3沉淀和Al3+
D.Al(OH)3沉淀和〔AlO2〕-离子
参考答案:B
本题解析:向明矾[KAl(SO4)2.12H2O]溶液中加入Ba(OH)2溶液,当SO42- 恰好沉淀完全时发生反应:Al3++ 2SO42-+ 2Ba2++4OH-= 2BaSO4↓+2H2O+ AlO2-.因此这时铝元素的存在形式AlO2- 离子。故选项为B。
本题难度:一般
5、选择题 把a?g铁铝合金粉末溶于足量盐酸中,加入过量NaOH?溶液.过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a?g,则原合金中铁的质量分数为( )
A.70%
B.52.4%
C.47.6%
D.30%
参考答案:由铁铝合金粉末溶于足量盐酸中,加入过量NaOH?溶液,沉淀为氢氧化铁,则经洗涤、干燥、灼烧,得到红棕色粉末为氧化铁,
则agFe、Al→agFe2O3,
合金中铝的质量等于氧化铁中氧元素的质量,
则合金中铁的质量分数等于氧化铁中铁的质量分数,
原合金中铁的质量分数为56×256×2+16×3×100%=70%,
故选A.
本题解析:
本题难度:一般