��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��13�֣����ڳ��о���ʹ�õĹܵ�ú������Ҫ�ɷ���H2��CO������CH4��H2��CO��CH4��ȼ�����������±�
����
| H2
| CO
| CH4
|
ȼ���ȣ�kJ?mol-1��
| 285.8
| 283.0
| 890.3
|
��1����д��H2��CO��CH4ȼ�յ��Ȼ�ѧ����ʽ��
_________________________________________________��
_________________________________________________��
_________________________________________________��
��2����Ϊ�����������������乤�̵���Ҫ�ɾͣ�������Ȼ����ȫ������Ϻ������վ��ڣ�½����Ϊ���о���ʹ�õ���Ҫ��Դ��ʹ�ùܵ�ú���û�������Ȼ����Ӧ������߽��������ţ�������_____�������������Ȼ�������Ľ����������_____�������������Ȼ�������Ľ�������
�ο��𰸣���1��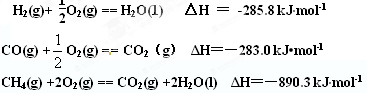
��2������?��Ȼ��
�����������1��ȼ��������һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų��������� ���Ը���ȼ���ȿ�֪�ֱ�д����������ȼ�յ��Ȼ�ѧ����ʽ��
��2����Ȼ������Ҫ�ɷ��Ǽ��飬�����к������ܸߣ�����������ͬ�������£�����ȼ�����ĵ������࣬���ԸĽ��ķ�������������Ľ������������Ȼ���Ľ�������
�����Ѷȣ�һ��
2������� ��16�֣����ؿ���ΪH2O2���ȶ����壬����һ�ֹ�̬���ʹ��桢�������������������������������������[CO(NH2)2��H2O2]����ϳɹ����������£�

��ش��������⣺
��1������I��II�����Ʒֱ���______��_______��CO(NH2)2��H2O2���������غ�������֮����________��ϣ��������������������غ�������˫�����ʡ�
��2����ҵ���������������ԭ����������Ȼ����ˮ��Ӧ�Ʊ�����֪��
�ټ��顢������ȼ���ȷֱ�Ϊ890��3KJ/mol��285��8kJ/mol
��
д��CH4��ˮ������������CO2��H2���Ȼ�ѧ����ʽ��_______________��
��3���ϳɹ����������ؼ�����ȶ���������ˮ���ᡢ��ʯ��ȡ���ʯ�����ʽΪC4H6O6����˴Ź�������ֻ��3�ַ棬ֻ���Ȼ����ǻ����ֹ����ţ����ʯ��Ľṹ��ʽΪ_____��
��4��Ϊ�ⶨ��Ʒ��H2O2�ĺ�������ȡ������Ʒ12��0g���250mL��Һ��ȡ25��00mL
����ƿ�У��������������ữ����0��20mol/LKMnO4����Һ�ζ������εζ�ƽ������KMnO4��Һ20��00mL����KMO4��Һ�����ز���Ӧ����
����ɲ���ƽ����ʽ�� MnO4-+
MnO4-+  ?H2O2+
?H2O2+  ?_________=Mn2++
?_________=Mn2++ O2��+
O2��+ ___��
___��
�ڼ������Ʒ��H2O2����������Ϊ_______��
��5��������صķ�ˮ�ȿ��Դ�����ˮ���ֿ��Ƶô��⣬���ԭ����ͼ��ʾ�������и�Ĥ����ֹ����ͨ����B������Ϊ���Ե缫��B�����ӵ�Դ��____������
�������������������缫��Ӧ����Ϊ_____________��

�ο��𰸣���16�֣�
��1���������������ˣ�2�֣�?�����1�֣�
��2��CH4(g)��2H2O(g)==CO2(g)��4H2(g)?DH��+164��9?kJ/mol��3�֣�
��3��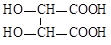 ��2�֣�
��2�֣�
��4����2MnO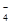 ?��5H2O2��6H��==2Mn2+��5O2����8H2O��2�֣�? ��28��3?%��2�֣�
?��5H2O2��6H��==2Mn2+��5O2����8H2O��2�֣�? ��28��3?%��2�֣�
��5������2�֣�? CO(NH2)2��6e����8OH�� == N2����CO ?��6H2O��2�֣�
?��6H2O��2�֣�
�����������1����Ϊ���������ؾ������غ�������˫�����ʣ������ֽ⣬����Ӧʹ��Һ�ڽϵ��¶�����������˲���I��II�����Ʒֱ��ǵ������������ˣ�CO(NH2)2��H2O2���������غ������ⶼ�Ѿ��ﵽ�ȶ��ṹ������֮��Ľ����������Ӧ��Ϊ�����
��2������д��CH4��H2O��Ӧ�Ļ�ѧ����ʽ��ע��״̬��Ȼ����ݸ�˹�������ʱ䣬?H=��890��3kJ?mol?1+4��285��8kJ?mol?1��2��44kJ?mol?1 =+164��9?kJ?mol?1���ɵ��Ȼ�ѧ����ʽ��
��3����ʯ��ֻ���Ȼ����ǻ����ֹ����ţ����ݲ����Ͷȣ�Ӧ����2���Ȼ���2���ǻ����˴Ź�������ֻ��3�ַ棬˵��Hԭ��λ��ֻ��3�֣�Ϊ�Գƽṹ�����Խṹ��ʽΪ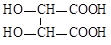
��4���ٸ���������ԭ��Ӧ�У����ϼ����ߵļ����ͽ�����ȣ�MnO4?��MnԪ�ؽ���5�ۣ�H2O2��OԪ������1�ۣ�����MnO4?��Mn2+��ϵ��Ϊ2��H2O2��O2��ϵ��Ϊ5��Ȼ�����ù۲취��ƽ��ѧ����ʽ��
�ڸ��ݷ�ӦʱKMnO4��H2O2�����ʵ���֮��Ϊ2:5���ɵò�Ʒ��H2O2����������=0��2mol/L��0��02L��5/2��10��34g/mol��12g��100% =28��3%
��5������ͼʾ��B������H+�õ�������H2������BΪ���������ӵ�Դ�ĸ���������CO(NH2)2ʧȥ����ת��ΪN2����Ϊ���Һ��KOH�����Ե缫����ʽΪ��CO(NH2)2��6e����8OH�� == N2����CO ��6H2O
��6H2O
�����Ѷȣ�һ��
3��ѡ���� ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ���Ȼ�ѧ����ʽΪH+��aq��+OH-��aq���TH2O��l����H=-57.3kJ?mol-1�����ᡢŨ���ᡢϡ����ֱ���0.1mol?L-1NaOH��Һǡ����ȫ��Ӧ�ų�������������NaOH��Һ������Ĺ�ϵ��ͼ��ʾ��������������ȷ���ǣ�������
A��A��ʾϡ������NaOH��Һ�ķ�Ӧ
B��B��ʾ������NaOH��Һ��Ӧ
C��b=5.73
D��C��ʾŨ������NaOH��Һ��Ӧ