��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ö��Ե缫�ʹ�����·����������ʵ�ˮ��Һ����NaCl,?��NaNO3,?��CuCl2,?��AgNO3������ͬʱ������������������(ͬ��ͬѹ�²ⶨ)���������ɶൽ�ٵ�˳����?
[? ]
A���٢ڢۢܡ�������������
B���ܢ٢ڢ�
C���ڢ٢ۢ�?
D���٢ڢܢ�
�ο��𰸣�A
���������
�����Ѷȣ�һ��
2������� ������һ�ֿ��Է�����硢�ŵ��װ�á���һ�������ڳ��ͷŵ�ʱ�����ķ�Ӧ�ǣ�
NiO2+Fe+2H2O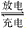 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
(1)�������طŵ�ʱ���õ��ijһ�缫������ԭ��Ӧ��������________(�����)��
A��NiO2 B��Fe C��Fe(OH)2 D��Ni(OH)2
(2)�ô����طֱ�������������Һ�������·��ת����0.02 mol e-���ҵ��صĵ缫��Ϊ���Ե缫��
�Իش��������⣺
�ٵ��M(NO3)x��Һʱijһ�缫������a g M�������M�����ԭ������Ϊ____________(�ú���a��x���ı���ʽ��ʾ)��
�ڵ�⺬��0.01 mol CuSO4��0.01 mol NaCl�Ļ����Һ100 mL�����������������ڱ�״���µ������________L�����������Һ��ˮϡ����1 L����ʱ��Һ��pH��____________________��
�ο��𰸣�(1)A��
(2)��50ax����0.168��2
���������
�����Ѷȣ�һ��
3��ѡ���� ��Fe2+��NO3-��Fe3+��NH4+��H2O��H+�������ӣ��ֱ�����ͬһ������ԭ��Ӧ�еķ�Ӧ����������������������ǣ�������
A���������뻹ԭ�������ʵ���֮��Ϊ1��8
B����ԭ����ΪNH4+
C������1molNO3-�μӻ�ԭ��Ӧ��ת��8mole-
D�����Ѹ÷�Ӧ���Ϊԭ��أ���������ӦΪFe2+-e-�TFe3+
�ο��𰸣�Fe2+���л�ԭ�ԣ�NO3-�����������¾���ǿ�����ԣ����������ȷ������Ԫ�صĻ��ϼ����ߣ�NԪ�صĻ��ϼ۽��ͣ�������Ӧ8Fe2++NO3-+10H+=8Fe3++NH4++H2O��
A���ɷ���ʽ��֪�÷�Ӧ����������NO3-���뻹ԭ����Fe2+�����ʵ���֮��Ϊ1��8����A��ȷ��
B����Ӧ��NԪ�صĻ��ϼ���NO3-��+5�۽���ΪNH4+��-3�ۣ�NH4+�ǻ�ԭ�����B��ȷ��
C����Ӧ��NԪ�صĻ��ϼ���NO3-��+5�۽���ΪNH4+��-3�ۣ�������lmolNO3- ������ԭ��Ӧ��ת�Ƶ�����Ϊ1mol��[5-��-3��]=8mol����C��ȷ��
D��ԭ��ظ�������������Ӧ��Fe2+�ڸ����ŵ�����Fe3+�����Ѹ÷�Ӧ��Ƴ�ԭ��أ�������ӦΪFe2+-e-=Fe3+����D����
��ѡ��D��
���������
�����Ѷȣ���
4��ѡ���� �Զ��Ե缫���CuSO4��Һ����������������0.01mol��������������CuΪ
[? ]
A��0.64g
B��1.28g
C��2.56g
D��5.12g
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5��ѡ���� ���������У���ʹ���ܽ⣬�ֲ����ɳ������������
A.ϡ����
B.NaCl��Һ
C.��������Һ
D.��������Һ
�ο��𰸣�D
���������ϡ������Fe��Ӧ�������塢��������Һ��Fe��Ӧ���ɹ�������NaCl��Һ��Fe����Ӧ��Fe2(SO4)3��Fe��Ӧ����FeSO4����û�г�����Ҳû���������ɣ�
�����Ѷȣ���