微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 已知:A、F为金属单质,D、E为气态单质,其余均为化合物,其中C的焰色反应呈黄色;B为黑色粉末,J为蓝色沉淀。各物质间的转化关系如下图所示(部分生成物已略去):
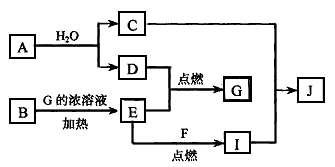
(1)A的原子结构示意图为 ________________, B的化学式为_______________。
(2)写出反应C+I→J的离子方程式:________________________。
(3)写出E+F→I的化学反应方程式为______________,D在E中点燃时的现象为_________________。
参考答案:(1)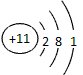 ; MnO2
; MnO2
(2)Cu2+ + 2OH-=Cu(OH)2↓
(3)Cu + Cl2 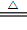 CuCl2?; 产生苍白色火焰
CuCl2?; 产生苍白色火焰
本题解析:
本题难度:一般
2、填空题 (14分)A、B、C、D都是中学化学常见物质或离子,其中A、B、C均含有同一种元素,在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去,其他产物都已列出)。请按要求回答下列问题:
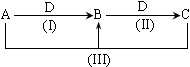
(1)若D为金属单质,且D是用量最大、用途最广的金属,若加热蒸干B的溶液没有得到B的盐,则B的化学式可能为_____________________。(4)若D是酸,则一定是多元酸,所以ABCD 分别是
(2)若A常用作致冷剂,B和D为空气的主要成分,则反应(III)的化学方程式为__________。
(3)若D为氯碱工业的重要产品,反应(III)的离子方程式为____________________________。
(4)若D为酸或酸性气体,也能实现上面的转化,请按A、B、C、D顺序写出合理的任意一组物质的化学式。
①当D为酸时,A________、B_________、C_________、D__________。
②当D为酸性气体时,A________、B_________、C_________、D__________。
参考答案:(1)FeCl3(2分)? (2)4NH3+6NO 5N2+6H2O(2分)
5N2+6H2O(2分)
(3)Al3++3AlO2-+6H2O==4Al(OH)3↓(2分)
(4)①Ba(OH)2、Ba3(PO4)2、BaHPO4或Ba(H2PO4)2、H3PO4(4分)
②NaOH、Na2CO3、NaHCO3、CO2(其他合理答案给分)(4分)
本题解析:(1)用量最大、用途最广的金属是铁,即D是铁。铁具有还原性且属于变价金属,A、B、C均含有同一种元素,加热蒸干B的溶液没有得到B的盐,说明该盐是盐酸盐,即A、B、C含有的同一种元素是氯元素。则ABC分别是氯气、氯化铁和氯化亚铁。
(2)B和D为空气的主要成分,则二者为氧气和氮气,A常用作致冷剂,是氨气,氨气氧化生成N2,N2氧化生成NO。
(3)D为氯碱工业的重要产品,D是氢氧化钠。ABC属于铝的化合物之间的转化,即A是铝盐,B是氢氧化铝,C是偏铝酸盐。
(4)若D是酸,则一定是多元酸,所以ABCD 分别是Ba(OH)2、Ba3(PO4)2、BaHPO4或Ba(H2PO4)2、H3PO4;若D为酸性气体时,也应该是多元酸对应的酸酐,例如二氧化碳、硫化氢、二氧化硫等。
本题难度:一般
3、填空题 A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体.而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊.D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体.请回答下列问题:
(1)写出A、B、C、D、E、F的化学式______
(2)写出F和H反应的化学方程式______.
(3)写出下列反应的离子方程式:
①D+盐酸______.
②B+水______.
参考答案:因焰色反应为黄色,说明五种物质都含有钠元素,
根据钠及其化合物的性质,可推知各物质.
E为氯化钠,
可燃气体是氢气,B为钠,
无色无味气体H能使澄清石灰水变浑浊,则H为二氧化碳,
F和H也可反应生成C和另一种无色无味气体,则无色无味气体为氧气,F为过氧化钠,C为碳酸钠
?C、D与盐酸反应生成一种无色无味气体H,D和A可反应生成C,则D为碳酸氢钠,A为氢氧化钠,
?故答案:(1)NaOH、Na、Na2CO3、NaHCO3、NaCl、Na2O2
?(2)2 Na2O2+2CO2=2Na2CO3+O2
(3)①HCO3-+H+=CO2↑+H2O
?②2Na+2H2O=2Na++2OH-+H2↑
本题解析:
本题难度:一般
4、填空题 (10分)以海水中常见物质A为原料可以发展很多种工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题:
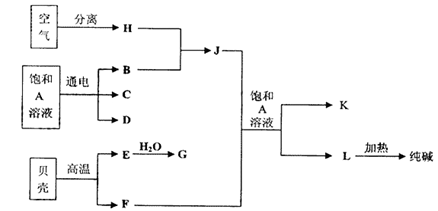
(1)电解A溶液反应的离子方程式为?;
(2)写出C与D制取消毒剂的化学方程式?;
(3)若要使工业合成J反应的平衡向生成J的方向移动,可采取的措施有?
A.升高温度? B.增大压强? C.使用催化剂? D.液化分离J
(4)将F和J通入A的饱和溶液中的顺序为?
A.先通入F后通入J ?B.先通入J后通入F
C.同时通入? D.没有先后顺序要求
(5)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。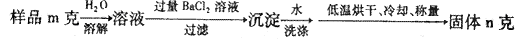
则计算样品中NaCl的质量分数的数学表达式为:??
参考答案:(1)2H2O+2Cl- ?Cl2↑+H2↑+2OH-?(2)Cl2 + NaOH="=NaClO" +NaCl +H2O?
?Cl2↑+H2↑+2OH-?(2)Cl2 + NaOH="=NaClO" +NaCl +H2O?
(3)B D?(4)B?(5)(1-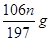 )
)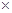 100%
100%
本题解析:(1)海水中含有氯化钠,所以A是氯化钠,电解的方程式为
2H2O+2Cl- Cl2↑+H2↑+2OH-。
Cl2↑+H2↑+2OH-。
(2)氯气溶于氢氧化钠溶液中甲生成消毒剂,方程式为Cl2 + NaOH="=NaClO" +NaCl +H2O。
(3)J是氨气,合成氨是体积减小的放热的可逆反应,所以BD可以是平衡向正反应方向移动。升高温度,平衡向逆反应方向移动。催化剂不能改变平衡状态,答案选BD。
(4)由于CO2在水中的溶解度不大,所以应该先通入氨气,然后再通入CO2,答案选B。
(5)n固体是碳酸钡,所以根据原子守恒可知,样品中碳酸钠的质量是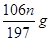 。样品中NaCl的质量分数的数学表达式为(1-
。样品中NaCl的质量分数的数学表达式为(1-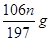 )
) 100%
100%
本题难度:一般
5、简答题 如图所示的是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去.已知X、Y、Z是日常生活中常见金属单质,X由地壳中含量最高的金属元素组成;D、E是常见气态非金属单质,其中D呈黄绿色.A的焰色反应呈紫色(透过蓝色钴玻璃),F的稀溶液呈蓝色.
请回答下列问题:
(1)C的电子式为______.
(2)I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,该反应的化学方程式为______.
(3)X与C溶液反应的离子方程式为______.
(4)写出J与Y反应的化学方程式,并标出电子转移的方向和数目:______.
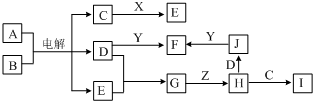
参考答案:X、Y、Z是日常生活中常见金属单质,X由地壳中含量最高的金属元素组成,则X为Al;D、E是常见气态非金属单质,其中D呈黄绿色,则D为Cl2,与Y反应得到F,且F的稀溶液呈蓝色,含有Cu2+,则Y为Cu、F为CuCl2,A的焰色反应呈紫色(透过蓝色钴玻璃),含有K元素,A与B在电解条件下得到C、D(氯气)、E,可推知A为KCl、C为KOH、E为H2,由转化关系可知,G为HCl,与金属Z反应得到H、H能被氯气氧化得到J,金属Z为变价金属,可推知Z为Fe,故H为FeCl2,J为FeCl3,(2)中I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,则I为Fe(OH)2,
(1)C为KOH,电子式为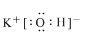 ,
,
故答案为: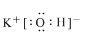 ;
;
(2)I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,该反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)X与C溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)标出J与Y反应的电子转移的方向和数目为: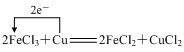 ,
,
故答案为: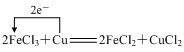 .
.
本题解析:
本题难度:一般